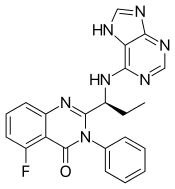
 Структура иделалисиба Структура иделалисиба | ||
| Клинические данные | ||
|---|---|---|
| Произношение | . | |
| Торговые наименования | Zydelig | |
| Другие наименования | GS-1101, CAL-101 | |
| AHFS / Drugs.com | Монография | |
| MedlinePlus | a614040 | |
| Данные лицензии | ||
| Беременность. категория |
| |
| Способы применения. | Устно (таблетки ) | |
| код ATC | ||
| Правовой статус | ||
| Правовой статус |
| |
| Pha rmacokinetic данные | ||
| Связывание с белками | >84% | |
| Метаболизм | Альдегидоксидаза (~ 70%), CYP3A4 (~ 30%); UGT1A4 (второстепенный) | |
| Метаболиты | GS-563117 (неактивные in vitro) | |
| Начало действия | Tмакс = 1,5 часа | |
| Период полувыведения | 8,2 часа | |
| Экскреция | Кал (78%), моча (14%) | |
| Идентификаторы | ||
Название ИЮПАК
| ||
| Номер CAS | ||
| PubChem CID | ||
| DrugBank | ||
| ChemSpider | ||
| UNII | ||
| KEGG | ||
| ChEBI | ||
| ChEMBL |
| |
| ECHA InfoCard | 100.235.089 | |
| Химические и физические данные | ||
| Формула | C22H18FN7O | |
| Молярная масса | 415,432 г · моль | |
| 3D-модель (JSmol ) | ||
УЛЫБКИ
| ||
InChI
| ||
Иделалисиб, продается под торговая марка Zydelig - это лекарство, используемое для лечения некоторых рака крови.
. Вещество действует как ингибитор фосфоинозитид-3-киназы ; более конкретно, он блокирует P110δ, дельта-изоформу фермента фосфоинозитид-3-киназы. Он был разработан Gilead Sciences. Годовой объем продаж Idelalisib составил 168 миллионов долларов (USD ) в 2016 году по сравнению со 132 миллионами долларов (USD) в 2015 году.
Иделалисиб препарат второго ряда для пациентов, у которых хронический лимфолейкоз (ХЛЛ) рецидивировал. Иделалисиб, применяемый в сочетании с ритуксимабом, должен применяться у пациентов, для которых применение ритуксимаба в отдельности может считаться подходящей терапией из-за других существующих медицинских состояний. Он оказался эффективным и приводит к улучшению лимфаденопатии и спленомегалии. Однако при приеме иделалисиба количество лимфоцитов снижается до нормального уровня. Он не рекомендуется в качестве лечения первой линии.
Он также одобрен для лечения фолликулярной B-клеточной неходжкинской лимфомы (FL) и рецидивирующей малой лимфоцитарной лимфомы (SLL), оба у пациентов, которые ранее получали как минимум два системных лечения.
Клинические симптомы включают диарею, лихорадку, утомляемость, тошнота, кашель, пневмония, боль в животе, озноб и сыпь. Лабораторные отклонения могут включать: нейтропению, гипертриглицеридемию, гипергликемию и повышенные уровни ферментов печени. Безопасность и эффективность иделалисиба для лечения рецидивов ФЛ и рецидивов SLL были установлены в клиническом исследовании с участием 123 участников с медленно растущими (вялотекущими) неходжкинскими лимфомами. Все участники получали иделалисиб, и их оценивали на предмет полного или частичного исчезновения рака после лечения (частота объективного ответа, или ЧОО). Результаты показали, что у 54% участников с рецидивом FL и у 58% участников с SLL наблюдалась ЧОО.
На этикетке иделалисиба в США есть предупреждение в рамке с описанием токсичности, которая может быть серьезной и смертельной, включая токсичность для печени, тяжелая диарея, воспаление толстой кишки, воспаление легочной ткани (пневмонит ) и перфорация кишечника, и от производителя требовалось внедрить Стратегию оценки и смягчения рисков (REMS), в рамках которой можно было бы управлять риском токсичности.
В марте 2016 года, когда были получены отчеты из трех текущих Клинические испытания серьезных нежелательных явлений и смертей, в основном из-за инфекций, Европейское агентство по лекарственным средствам открыло обзор препарата и его рисков. 21 марта 2016 г. Gilead Sciences (производитель идеалализиба) предупредила медицинских работников о снижении общей выживаемости и повышенном риске серьезных инфекций у пациентов с ХЛЛ и вялотекущей неходжкинской лимфомой (iNHL), получавших иделалисиб. Компания также сообщила, что прекратила шесть клинических испытаний с участием пациентов с ХЛЛ, SLL и iNHL из-за увеличения частоты нежелательных явлений, включая летальные исходы. В 2016 году EMA рекомендовало людям, принимающим иделалисиб, давать лекарства против легочной инфекции Pneumocystis jirovecii pneumonia, и это следует продолжать до 6 месяцев после прекращения приема иделалисиба. Кроме того, людей следует контролировать на предмет признаков инфекции.
Киназа PI3Kδ экспрессируется в нормальных и злокачественных B-клетках. Подавляя его, иделалисиб вызывает апоптоз и предотвращает пролиферацию клеточных линий, полученных из злокачественных В-клеток, и клеток первичной опухоли. Он также подавляет несколько сигнальных путей клеток, включая передачу сигналов B-клеточного рецептора (BCR) и передачу сигналов CXCR4 и CXCR5, которые являются участвует в перемещении и перемещении B-клеток в лимфатические узлы и костный мозг.
Иделалисиб является конкурентным ингибитором 96>АТФ сайт связывания каталитического домена PI3Kδ . Его активность и селективность in vitro по сравнению с другими изоформами PI3K класса I следующие:
| PI3K на основе изоформы | IC50, nM | IC50, PI3Kδ-кратная селективность |
|---|---|---|
| PI3Kα | 8600 | 453 |
| PI3Kβ | 4,000 | 211 |
| PI3Kγ | 2,100 | 110 |
| PI3Kδ | 19 | 1 |
В июле 2014 года FDA и EMA одобрили иделалисиб для лечения различных типов лейкемии. FDA также одобрило иделалисиб для лечения пациентов с рецидивирующей фолликулярной B-клеточной неходжкинской лимфомой и рецидивирующей малой лимфоцитарной лимфомой. Idelalisib предназначен для использования у пациентов, которые ранее получали как минимум два системных лечения.