A антагонист каннабиноидных рецепторов, также известный как антагонист каннабиноидов или антиканнабиноид представляет собой тип каннабиноидергического препарата, который связывается с каннабиноидными рецепторами (CBR) и предотвращает их активацию эндоканнабиноидами. Они включают антагонисты, обратные агонисты и антитела CBR. Открытие эндоканнабиноидной системы привело к разработке антагонистов CB1рецептора. Первый антагонист CBR, римонабант, был описан в 1994 году. Римонабант селективно блокирует рецептор CB 1, и было показано, что он снижает потребление пищи и регулирует увеличение массы тела. Распространенность ожирения во всем мире резко растет и оказывает большое влияние на общественное здоровье. Отсутствие эффективных и хорошо переносимых лекарств для лечения ожирения привело к повышенному интересу к исследованиям и разработке антагонистов CBR. Каннабидиол (CBD), природный каннабиноид, неконкурентоспособный CB <240 Антагонист рецептора>1 / CB 2. И Δ-тетрагидроканнабиварин (THCV), природный каннабиноид, модулирующий эффекты THC посредством прямой блокады каннабиноидных рецепторов CB 1, таким образом, ведя себя как первые- обратные агонисты рецептора CB 1 поколения, такие как римонабант. CBD представляет собой лиганд CB 1 с очень низким сродством, который, тем не менее, может косвенно влиять на активность рецептора CB 1 in vivo, в то время как THCV представляет собой CB 1 с высоким сродством. рецепторный лиганд и сильный антагонист in vitro, но лишь изредка вызывает эффекты in vivo в результате антагонизма CB 1 рецептора. THCV также имеет высокое сродство к рецепторам CB 2 и сигнализирует как частичный агонист, в отличие от CBD и римонабанта.
 Растение каннабис
Растение каннабис На протяжении веков гашиш и марихуана из индийской конопли Cannabis sativa L. использовались в лечебных и рекреационных целях. В 1840 году Шлезингер С. был, по-видимому, первым исследователем, получившим активный экстракт из листьев и цветов конопли. Несколько лет спустя, в 1848 году, Декуртив Э. описал приготовление этанольного экстракта, который при испарении растворителя давал темную смолу, которую он назвал «каннабином». В 1964 г. в лаборатории Мехулама был выделен и синтезирован основной активный компонент C. sativa L., Δ-тетрагидроканнабинол (THC ). Два типа каннабиноидных рецепторов, CB 1 и CB 2, ответственных за эффекты THC, были обнаружены и клонированы в начале 1990-х годов. После открытия каннабиноидных рецепторов стало важным установить, встречаются ли их агонисты в организме в естественных условиях. Этот поиск привел к открытию первого эндогенного каннабиноида (эндоканнабиноида), анандамида (арахидоноилэтаноламида). Позже были обнаружены другие эндоканнабиноиды, например 2-AG (2-арахидоноилглицерин). Эти результаты подняли дополнительные вопросы о фармакологической и физиологической роли каннабиноидной системы. Это возродило исследования антагонистов каннабиноидных рецепторов, которые должны были помочь ответить на эти вопросы. Использование каннабиноидного агониста ТГК во многих его препаратах для повышения аппетита - хорошо известный факт. Этот факт привел к логическому выводу, что блокирование каннабиноидных рецепторов может быть полезно для снижения аппетита и потребления пищи. Затем было обнаружено, что блокирование рецептора CB 1 представляет собой новую фармакологическую мишень. Первым специфическим антагонистом рецептора CB 1 / обратным агонистом был римонабант, открытый в 1994 году.
эндогенная каннабиноидная система включает каннабиноидные рецепторы, их эндогенные лиганды (эндоканнабиноиды) и ферменты для их синтеза и деградации.
Существует два основных типа рецепторов, связанных с эндоканнабиноидной сигнальной системой: каннабиноидный рецептор 1 (CB 1) и 2 (CB2 ). Оба рецептора представляют собой 7-трансмембранные рецепторы, связанные с G-белком (GPCR ), которые ингибируют накопление циклического аденозинмонофосфата внутри клеток. Рецепторы CB 1 присутствуют в наибольшей концентрации в головном мозге, но также могут быть обнаружены на периферии. CB 2 рецепторы в основном расположены в иммунной и гематопоэтической системе.
Эндоканнабиноиды - это эйкозаноиды, действующие как агонисты каннабиноидных рецепторов, и они встречаются естественно в теле. Процессы, связанные с каннабиноидными рецепторами, например, участвуют в познании; объем памяти; беспокойство; контроль аппетита; рвота ; двигательное поведение; сенсорный, вегетативный, нейроэндокринный и иммунный ответы; и воспалительные эффекты. Есть два хорошо охарактеризованных эндоканнабиноида, расположенных в головном мозге и на периферии. Первым идентифицированным был анандамид (арахидоноилэтаноламид), а вторым - 2-AG (2-арахидоноилглицерин ). Дополнительные эндоканнабиноиды включают виродамин (O-арахидоноилэтаноламин), простой эфир ноладина (2-арахидоноилглицериловый эфир) и NADA (N-арахидоноилдофамин ).
 Рисунок 1 Гипотетическая модель метаболических эффектов антагонистов рецепторов CB 1 (ECS = эндоканнабиноидная система)
Рисунок 1 Гипотетическая модель метаболических эффектов антагонистов рецепторов CB 1 (ECS = эндоканнабиноидная система) CB1рецепторы связаны через белки G i / o и ингибируют аденилилциклаза и активируют митоген-активированный протеин (MAP) киназу. Кроме того, рецепторы CB 1 ингибируют пресинаптические кальциевые каналы N- и P / Q-типов и активируют внутренне выпрямляющие калиевые каналы. Антагонисты CB 1 вызывают обратные каннабимиметические эффекты, противоположные по направлению тем, которые производятся агонистами этих рецепторов.
CB1рецепторы высоко экспрессируются в области гипоталамуса, которые участвуют в центральном контроле приема пищи и пищевого поведения. Это убедительно указывает на то, что каннабиноидная система напрямую задействована d в регулировании кормления. Эти области также связаны с мезолимбическим дофаминовым путем, так называемой системой «вознаграждения». Следовательно, антагонисты CB 1 могут косвенно ингибировать дофамин-опосредованные полезные свойства пищи. Периферические рецепторы CB 1 расположены в желудочно-кишечном тракте (GI), печени и в жировой ткани. В GI рецепторы CB 1 расположены на нервных окончаниях в кишечнике. Эндоканнабиноиды действуют на рецепторы CB 1, усиливая чувство голода и способствуя кормлению, и предполагается, что они уменьшают кишечную перистальтику и опорожнение желудка. Таким образом, антагонизм к этим рецепторам может обратить эти эффекты. Кроме того, в периферических тканях антагонизм рецепторов CB 1 увеличивает чувствительность к инсулину и окисление жирных кислот в мышцах и печени. Гипотетическая схема метаболических эффектов антагонистов рецептора CB 1 показана на рисунке 1.
Первым подходом к разработке антагонистов каннабиноидов в конце 1980-х годов был изменить структуру THC, но результаты разочаровали. В начале 1990-х годов было обнаружено новое семейство каннабиноидных агонистов из НПВП (нестероидное противовоспалительное) лекарство правадолин, что привело к открытию антагонистов аминоалкилиндола с некоторым, но ограниченным успехом.. Поскольку поиск, основанный на структуре агонистов, разочаровал, неудивительно, что первый мощный и селективный антагонист каннабиноидов принадлежал к совершенно новому химическому семейству. В 1994 году первый селективный антагонист каннабиноидов, SR141716 (римонабант), был представлен Sanofi, принадлежащим к семейству 1,5-диарилпиразолов.
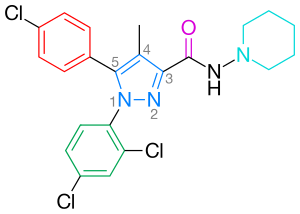 Рисунок 2 Химическая структура римонабанта
Рисунок 2 Химическая структура римонабанта 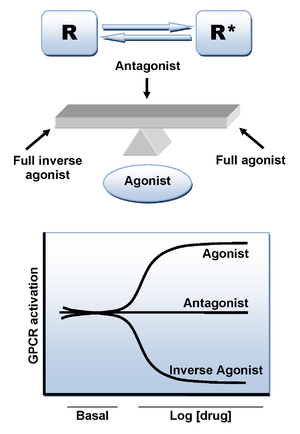 Рисунок 3 Схематическое изображение модели с двумя состояниями активации рецептора CB 1, в которой рецепторы находятся в равновесии между двумя состояниями, активный и неактивный (R * и R)
Рисунок 3 Схематическое изображение модели с двумя состояниями активации рецептора CB 1, в которой рецепторы находятся в равновесии между двумя состояниями, активный и неактивный (R * и R) 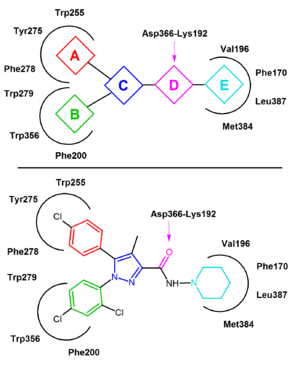 Фиг.4 Общая модель фармакофоров обратного агониста рецептора CB 1. Показаны предполагаемые остатки аминокислотной боковой цепи рецептора CB 1 во взаимодействии рецептор-лиганд. Ниже в качестве репрезентативного примера взят римонабант. Нанесенные цвета указывают на общие свойства с общим CB 1 фармакофором
Фиг.4 Общая модель фармакофоров обратного агониста рецептора CB 1. Показаны предполагаемые остатки аминокислотной боковой цепи рецептора CB 1 во взаимодействии рецептор-лиганд. Ниже в качестве репрезентативного примера взят римонабант. Нанесенные цвета указывают на общие свойства с общим CB 1 фармакофором римонабантом, также известным под систематическим названием [N- (пиперидин-1-ил) -5- (4-хлорфенил) -1. - (2,4-дихлорфенил) -4-метил-1H-пиразол-3-карбоксамидгидрохлорид)], является антагонистом рецептора 1,5-диарилпиразола CB 1 (рис. 2). Римонабант является не только мощным и высокоселективным лигандом рецептора CB 1, но он также активен при пероральном приеме и противодействует большинству эффектов агонистов каннабиноидов, таких как THC, как in vitro, так и in vivo. Римонабант продемонстрировал явную клиническую эффективность для лечения ожирения.
Связывание агонистического лиганда с рецептором CB 1 вызывает конформационные изменения и приводит к активному состояние рецептора, ответственного за передачу сигнала. Однако существует дополнительный механизм, который может привести к активному состоянию в отсутствие лиганда. Как и многие другие GPCR, рецептор CB 1 проявляет высокий уровень конститутивной активности и, таким образом, он может спонтанно принимать активное конформационное состояние в отсутствие связывания агониста, поддерживая повышенные базальные уровни внутриклеточной передачи сигналов. Это можно объяснить моделью двух состояний активации рецептора, в которой рецепторы находятся в равновесии между двумя состояниями, активным и неактивным (R * и R). Агонист стабилизирует активное состояние, ведущее к активации, нейтральный антагонист одинаково связывается с активным и неактивным состояниями, тогда как обратный агонист предпочтительно стабилизирует неактивное состояние (рисунок 3). 104>
Во многих случаях сообщалось о том, что римонабант ведет себя как обратный агонист, а не как нейтральный антагонист, и вполне вероятно, что он предпочтительно связывается с неактивным состоянием CB 1, тем самым уменьшая активация сигнального пути. Ключевым связывающим взаимодействием является водородная связь, образованная между карбонильной группой римонабанта и остатком Lys192 рецептора CB 1. Эта связь стабилизирует солевой мостик Lys192-Asp366 внутриклеточного конца трансмембранных спиралей 3 и 6 (Фиг.4). Этот специфический солевой мостик присутствует в неактивном состоянии рецептора, но отсутствует в активном состоянии.
В неактивном состоянии CB 1 римонабант связывается в трансмембранном-3-4-5 -6 ароматический микродомен. Связывание римонабанта включает прямые ароматические взаимодействия между его 2,4-дихлорфенильным кольцом и остатками Trp279 / Phe200 / Trp356 с одной стороны и пара-хлорфенильным кольцом и остатками Tyr275 / Trp255 / Phe278 с другой стороны. Липофильный пиперидинил фрагмент хорошо вписывается в полость, образованную аминокислотными остатками Val196 / Phe170 / Leu387 и Met384 (рис. 4).
Most CB 1 антагонистов, о которых сообщалось до настоящего времени, являются близкими аналогами или изостерами римонабанта. Общая модель CB 1 обратного агониста фармакофор может быть извлечена из общих черт этих аналогов, диарилпиразолов (Фиг.4). Этот фармакофор содержит циклическое ядро C (например, пиразол в римонабанте), замещенное двумя ароматическими фрагментами, A и B. А блок акцептора водородной связи, D, соединяет C с циклической липофильной частью E. в некоторых случаях блок E напрямую соединяется с C. На рисунке 4 в качестве примера используется римонабант. Элемент A представляет собой 4-хлорфенильную группу, а элемент B - 2,4-дихлорфенильное кольцо. Единица C представляет собой центральное кольцо пиразола, а звено D представляет собой карбонильную группу, которая служит акцептором водородной связи. Единица E представляет собой липофильный аминопиперидинильный фрагмент.
Для оптимального связывания в рецепторе CB 1 требуется пара-замещенное фенильное кольцо в 5-положении пиразола. 5-заместитель пиразола участвует в распознавании рецептора и антагонизме. Пара-заместитель фенильного кольца может быть хлором, бромом или йодом, но было показано, что алкильная цепь также может быть допустимой. Нумерация центрального пиразольного кольца показана на фиг. 2.
2,4-дихлорзамещенное фенильное кольцо в положении пиразола 1 является предпочтительным как сродством, так и с точки зрения активности. Было показано, что дополнительные галогены на этом фенильном кольце снижают аффинность.
Также благоприятно иметь замещение в кольце у 3-карбоксамидной группы, такой как 1-пиперидинильная группа в римонабант. Замена аминопиперидинильного заместителя на алкил амиды, простые эфиры, кетоны, спирты или алканы в основном привело к снижению аффинности. Замена пиперидинила на пентил или гептильную цепь придает соединениям агонистические свойства. На основании этих результатов был сделан вывод, что положение пиразола 3, по-видимому, участвует в агонизме, тогда как положения 1, 4, 5, по-видимому, участвуют в антагонизме.
Исследования показали, что отсутствие кислорода карбоксамида приводит к снижению сродства. Кроме того, присутствие кислорода карбоксамида способствует приданию свойств обратного агониста, тогда как аналоги, лишенные этого кислорода, как обнаружено, являются нейтральными антагонистами. Эти результаты подтверждают гипотезу о том, что кислород карбоксамида образует водородную связь с остатком Lys192 на рецепторе CB 1.
Аналоги SR141716 (римонабанта) недавно были описанные несколькими группами, что привело к хорошему пониманию взаимосвязи структура-активность (SAR) в этой химической группе. Хотя большинство описанных соединений менее эффективны, чем SR141716, два из них заслуживают упоминания, SR147778 и AM251, хотя оба могут также действовать на мю-опиоидные рецепторы.
SR147778 (surinabant ), антагонист второго поколения, имеет более длительную продолжительность действия, чем римонабант, и повышенную пероральную активность. Такая увеличенная продолжительность действия, вероятно, связана с наличием более метаболически стабильной этильной группы в 4-м положении пиразольного кольца. Другим изменением является замена 5-фенилхлорного заместителя бромом.
Было описано производное диарилпиразола, AM251, в котором заместитель хлора был заменен на йод в пара-положении 5-фенильного кольца. Это производное оказалось более сильным и селективным, чем римонабант.
Был синтезирован 21 аналог, содержащий либо алкиламид, либо алкил гидразид различной длины в положении 3. Было замечено, что сродство увеличивается с увеличением длины углеродной цепи до пяти атомов углерода. Аналоги амида также обладают более высоким сродством, чем аналоги гидразида. Однако ни один из этих аналогов не обладал значительно большей аффинностью, чем римонабант, но, тем не менее, они были немного более селективными, чем римонабант, в отношении рецептора CB 1 по сравнению с рецептором CB 2.
Было предпринято несколько попыток повысить сродство производных диарилпиразола путем придания жесткости структуре римонабанта. В терминах общей модели фармакофоров единицы A, B и / или C связаны дополнительными связями, ведущими к жестким молекулам. Например, конденсированный полициклический пиразол NESS-0327 показал в 5000 раз большее сродство к рецептору CB 1, чем римонабант. Однако это соединение имеет низкую центральную биодоступность.
. Другое соединение, производное индазола, можно рассматривать как аналог римонабанта, в котором его 5-арильная группа конденсирована с пиразольным фрагментом. Однако эта структурная модификация привела к 67-кратному снижению сродства к рецептору CB 1.
Эти диарилпиразольные производные римонабанта сведены в таблицу 1.
 |  |
| SR147778 | AM251 |
 | 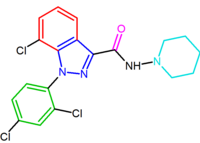 |
| NESS-0327 |
Структурно отличные от 1,5-диарилпиразолов химические ряды 3,4-диарилпиразолинов. В эту серию входит SLV-319 (ибипинабант ), мощный антагонист CB 1, который примерно в 1000 раз более селективен для CB 1 по сравнению с CB 2 и проявляет in vivo активность, аналогичную римонабанту.
Другой подход, использованный для разработки аналогов римонабанта, заключался в замене центрального пиразольного кольца другим гетероциклом. Примером этого подхода являются 4,5-диарилимидазолы и 1,5-диарилпиррол-3-карбоксамиды.
Сообщалось о большом количестве конденсированных бициклических производных диарилпиразола и имидазолов. Примером этого является производное пурина, в котором кольцо пиримидина конденсировано с кольцом имидазола. Отенабант (CP-945,598) является примером конденсированного бициклического соединения. производное, разработанное Pfizer.
Несколько исследовательских групп изучали шестичленные кольцевые пиразолы биоизостеры. Например, было показано, что одно производное 2,3-диарилпиридина является сильным и селективным обратным агонистом CB 1. Структура этого соединения демонстрирует возможность того, что амидная часть римонабанта может быть разделена на липофильную (бензилокси) и полярную (нитрильную) функциональность. Другими аналогами с шестичленным кольцом являются, например, пиримидины и пиразины.
. Помимо аналогов с пяти- и шестичленным кольцом, существуют другие циклические производные, такие как азетидины. Одним из примеров является производное азетидина метилсульфонамида, которое имеет 1,1-диарильную группу, которая имитирует 1,5-диарильную группу диарилпиразолов. сульфонильная группа служит акцептором водородной связи. 1,1-диарильная группа также присутствует в производных, таких как бензодиоксолы и гидантоины..
Также сообщалось об ациклических аналогах. Эти аналоги содержат 1,2-диарильный мотив, который соответствует 1,5-диарильным заместителям римонабанта. Примером ациклического аналога является таранабант (MK-0364), разработанный Merck.
. Представители этих аналогов приведены в Таблице 2.
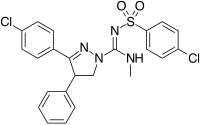 |  |  | |
| Тип. производного | 3,4-диарилпиразолина (ибипинабант ) | 4,5-диарилимидазол | 1,5-диарилпиррол-3-карбоксамиды |
 |  | 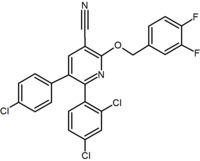 | |
| Тип. производного | Пурина (пиримидиновое кольцо., конденсированное с имидазольным кольцом) | Производное пурина (Отенабант ) | 2,3-Диарилпиридин |
 |  | 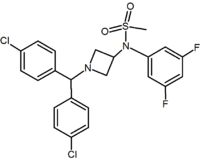 | |
| Тип. производного | Пиримидин | Пиразин | Метилсульфонамид. азетидин |
 | 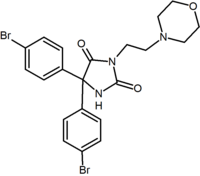 | 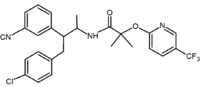 | |
| Тип. производного | Бензодиоксол | Гидантоин | Ациклическое производное. (Таранабант ) |
Антитела против рецептора CB 1 разработаны и внедрены в клиническую практику в России. К ним относятся (Русский : Бризантин®) и (Русский : Диетресса®). Бризантин показан для лечение никотиновой отмены и отказ от курения и диетотерапия показаны для потери веса. Dietressa доступна без рецепта в России.
Римонабант (Acomplia) одобрен в Европейском Союзе (ЕС) с июня 2006 г. для лечения ожирения. 23 октября 2008 г. Европейское агентство по лекарственным средствам (EMEA) рекомендовало приостановить действие разрешения на продажу Acomplia от Sanofi-Aventis на территории ЕС из-за риска серьезных психических расстройств. 5 ноября 2008 г. Санофи-Авентис объявила о прекращении программы клинической разработки римонабанта.
Санофи-Авентис также прекратила разработку суринабанта (SR147778), антагониста рецептора CB 1 для прекращения курения (31 Октябрь 2008 г.).
Компания Merck заявила в своем пресс-релизе от 2 октября 2008 г., что не будет добиваться одобрения регулирующих органов на таранабант (MK-0364) для лечения ожирения и прекратит свою программу клинических разработок Фазы III. Данные клинического исследования фазы III показали, что более высокая эффективность и больше побочных эффектов были связаны с более высокими дозами таранабанта, и было определено, что общий профиль таранабанта не поддерживает дальнейшее развитие лечения ожирения.
Другая фармацевтическая компания, Компания Pfizer прекратила программу разработки фазы III своего соединения otenabant от ожирения (CP-945,598), селективного антагониста рецептора CB 1. Согласно Pfizer, их решение было основано на изменении нормативных позиций в отношении профиля риска / пользы класса CB 1 и возможных новых нормативных требованиях для утверждения.
Был опубликован ряд инициатив, направленных на разрабатывают антагонисты CB1, которые нацелены только на периферические рецепторы CB1, ограничивая их способность преодолевать гематоэнцефалический барьер. Среди этих инициатив 7TM Pharma сообщила о разработке TM38837. В настоящее время опубликован обзор подходов и соединений, которые используются в качестве периферически ограниченных блокаторов рецепторов CB 1.