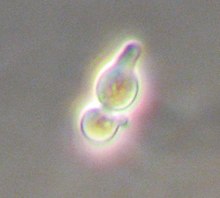
 Saccharomyces cerevisiae, скрещивающий а с shmoo, отвечающий на альфа-фактор
Saccharomyces cerevisiae, скрещивающий а с shmoo, отвечающий на альфа-фактор Дрожжи Saccharomyces cerevisiae - это простой одноклеточный эукариот с диплоидным и гаплоидным способами существования. Спаривание дрожжей происходит только между гаплоидами, который может быть либо или α (альфа) типа спаривания и, таким образом, отобразить простую половую дифференциацию. Тип Спаривание определяется одним локусом, MAT, который в свою очередь регулирует сексуальное поведение обоих гаплоидных и диплоидных клеток. Посредством генетической рекомбинации гаплоидные дрожжи могут переключать тип спаривания так часто, как каждый клеточный цикл.
S. cerevisiae (дрожжи) могут стабильно существовать как диплоид, так и гаплоид. И гаплоидные, и диплоидные дрожжевые клетки размножаются путем митоза, при этом дочерние клетки отпочковываются от материнских клеток. Гаплоидные клетки способны спариваться с другими гаплоидными клетками противоположного типа спаривания ( a- клетка может спариваться только с α-клеткой, и наоборот) с образованием стабильной диплоидной клетки. Диплоидные клетки, обычно сталкиваясь со стрессовыми условиями, такими как истощение питательных веществ, могут претерпевать мейоз с образованием четырех гаплоидных спор : двух а-спор и двух α-спор.
 Два гаплоидных дрожжа противоположных типов спаривания выделяют феромоны, отростки и спариваются.
Два гаплоидных дрожжа противоположных типов спаривания выделяют феромоны, отростки и спариваются. а клетки продуцируют « в -фактор», матовый феромон, который сигнализирует присутствие в клетку в соседние клетки альфа. клетки реагируют на альфа-фактора, то α клетки спаривание феромона, выращивая выступ (известный как Shmoo, из - за его характерной формы, напоминающей Аль Capp мультипликационный персонаж Shmoo ) в сторону источника альфа-фактора. Аналогично, альфа - клетки продуцируют альфа-фактор, и реагировать на них в -фактор, выращивая выступ по направлению к источнику феромона. Ответ гаплоидных клеток только на феромоны спаривания противоположного типа спаривания позволяет спариваться между a и α клетками, но не между клетками того же типа спаривания.
Эти фенотипические различия между а- и альфа-клетками обусловлены разным набором генов, которые активно транскрибируются и репрессируются в клетках двух типов спаривания. а клетки активируют гены, которые производят в -фактор и производят рецептор клеточной поверхности (Ste2), который связывается с альфа-фактором и триггера сигнализации внутри клетки. а клетки также подавляют гены, связанные с α будучи клеткой. Аналогично, amp; alpha ; клетки активируют гены, которые производят альфа-фактор и производят рецептор клеточной поверхности (STE3), который связывает и реагирует на -фактор, а также альфа - клетки подавляют гены, связанные с будучи клетками.
Различные наборы транскрипционной репрессии и активации, которые характеризуют и альфа клетки вызваны наличием одного из двух аллелей одного локуса называемых МАТ: MAT а или MATα, расположенный на хромосоме III. Локус MAT обычно делится на пять регионов (W, X, Y, Z1 и Z2) на основе последовательностей, общих для двух типов спаривания. Разница заключается в области Y (Y a и Yα), которая содержит большинство генов и промоторов.
МАТ аллель MAT кодирует ген, называемый 1, который в гаплоидах направлять транскрипцию в -специфической транскрипционной программе (например, экспрессирующие Ste2 и подавляя STE3), которая определяет в клетку. MATα аллель MAT кодирует amp; alpha ; 1 и amp; alpha ; 2 генов, которые в гаплоидах направлять транскрипцию транскрипционной программы альфа-специфического (например, экспрессирующие STE3, подавляя Ste2), который вызывает клеточный быть α клеткой. S.cerevisiae, имеет более 2 ген без видимой функции, которая разделяет большую часть своей последовательности с amp; alpha ; 2; однако другие дрожжи, такие как Candida albicans, действительно обладают функциональным и отличным геном MAT a 2.
Гаплоидные клетки относятся к одному из двух типов спаривания ( а или а) и отвечают на феромон спаривания, продуцируемый гаплоидными клетками противоположного типа спаривания, и могут спариваться с клетками противоположного типа спаривания. Гаплоидные клетки не могут подвергаться мейозу. Диплоидные клетки не производят и не реагируют на феромоны спаривания и не спариваются, но могут пройти мейоз с образованием четырех гаплоидных клеток.
Подобно различиям между гаплоидными a и α-клетками, различные паттерны репрессии и активации генов ответственны за фенотипические различия между гаплоидными и диплоидными клетками. В дополнение к специфическим паттернам транскрипции a и α, гаплоидные клетки обоих типов спаривания разделяют гаплоидный паттерн транскрипции, который активирует гаплоид-специфические гены (такие как HO) и репрессирует диплоид-специфические гены (такие как IME1). Точно так же диплоидные клетки активируют диплоид-специфические гены и репрессируют гаплоид-специфические гены.
Различные паттерны экспрессии генов гаплоидов и диплоидов снова связаны с локусом MAT. Гаплоидные клетки содержат только одну копию каждой из 16 хромосом и, следовательно, могут обладать только одним аллелем MAT ( MAT a или MATα), который определяет их тип спаривания. Диплоидные клетки являются результатом спаривания a- клетки и α-клетки и, таким образом, обладают 32 хромосомами (в 16 парах), включая одну хромосому, несущую аллель MAT a, и другую хромосому, несущую аллель MATα. Комбинация информации, кодируемой аллелем MAT a ( ген a 1) и аллелем MATα (гены α1 и α2), запускает программу диплоидной транскрипции. Точно так же присутствие только одного аллеля MAT, будь то MAT a или MATα, запускает гаплоидную программу транскрипции.
Аллели, присутствующие в локусе MAT, достаточны для программирования поведения клетки при спаривании. Например, с помощью генетических манипуляций, A МАТ аллель может быть добавлен к MATα гаплоидных клетки. Несмотря на наличие гаплоидного набора хромосом, клетка теперь имеет аллели MAT a и MATα и будет вести себя как диплоидная клетка: она не будет производить феромоны спаривания и не реагировать на них, а при голодании будет пытаться пройти мейоз с фатальными результатами.. Точно так же делеция одной копии локуса MAT в диплоидной клетке, оставляющая только один аллель MAT a или MATα, приведет к тому, что клетка с диплоидным набором хромосом будет вести себя как гаплоидная клетка.
Спаривание у дрожжей стимулируется присутствием феромона, который связывается либо с рецептором Ste2 (в α-клетках), либо с рецептором Ste3 (в α-клетках). Связывание этого феромона затем приводит к активации гетеротримерного G-белка. Димерная часть этого G-белка рекрутирует Ste5 (и связанные с ним компоненты каскада MAPK ) на мембрану и в конечном итоге приводит к фосфорилированию Fus3.
Механизм переключения возникает в результате конкуренции между белком Fus3 (белок MAPK) и фосфатазой Ptc1. Оба эти белка пытаются контролировать 4 сайта фосфорилирования Ste5, каркасного белка с Fus3, пытающегося фосфорилировать фосфозиты, и Ptc1, пытающегося их дефосфорилировать.
Присутствие α-фактора индуцирует рекрутирование Ptc1 на Ste5 через мотив из 4 аминокислот, расположенный внутри фосфозитов Ste5. Затем Ptc1 дефосфорилирует Ste5, что в конечном итоге приводит к диссоциации комплекса Fus3-Ste5. Fus3 диссоциирует подобно переключателю в зависимости от состояния фосфорилирования 4 фосфозитов. Все 4 фосфозита должны быть дефосфорилированы для диссоциации Fus3. Способность Fus3 конкурировать с Ptc1 снижается по мере привлечения Ptc1, и, таким образом, скорость дефосфорилирования увеличивается в присутствии феромона.
Kss1, гомолог Fus3, не влияет на shmooing и не способствует принятию решения о спаривании, подобном переключению.
У дрожжей спаривание, а также производство шму происходит по механизму «все или ничего». Этот механизм, похожий на переключатель, позволяет дрожжевым клеткам избегать неразумных действий в очень сложной процедуре. Однако решение о спаривании должно быть не только консервативным (во избежание потери энергии), но и быстрым, чтобы не потерять потенциального партнера.
Решение о спаривании является чрезвычайно деликатным. Есть 3 способа поддержания этой сверхчувствительности:
[a и α дрожжи имеют один и тот же путь реакции спаривания, с той лишь разницей, что тип рецептора есть у каждого типа спаривания. Таким образом, приведенное выше описание, данное для дрожжей a-типа, стимулированных α-фактором, одинаково хорошо работает для дрожжей α-типа, стимулированных a-фактором.]
 Гаплоидные дрожжи делятся и подвергаются переключению типа спаривания, что позволяет спариваться и образовывать диплоиды.
Гаплоидные дрожжи делятся и подвергаются переключению типа спаривания, что позволяет спариваться и образовывать диплоиды. Гаплоидные дрожжи дикого типа способны переключать тип спаривания с а на а. Следовательно, даже если одна гаплоидная клетка данного типа спаривания обнаруживает колонию дрожжей, переключение типа спаривания приведет к тому, что в популяции будут присутствовать клетки как типа спаривания, так и типа спаривания. В сочетании с сильным стремлением гаплоидных клеток к спариванию с клетками противоположного типа спаривания и образованию диплоидов, переключение типа спаривания и последующее спаривание приведет к тому, что большинство клеток в колонии будут диплоидными, независимо от того, основала ли гаплоидная или диплоидная клетка колония. Подавляющее большинство штаммов дрожжей , изученных в лабораториях, были изменены таким образом, что они не могут выполнять переключение типа спаривания (путем делеции гена HO ; см. Ниже); это позволяет стабильное распространение гаплоидных дрожжей, а гаплоидные клетки типа спаривания останутся клетки (и альфа - клетка будет оставаться α клетки), и не будут образовывать диплоиды.
 Расположение молчаливых локусов HML и HMR и активного локуса MAT на хромосоме III дрожжей.
Расположение молчаливых локусов HML и HMR и активного локуса MAT на хромосоме III дрожжей. Гаплоидные дрожжи переключают тип спаривания, заменяя информацию, присутствующую в локусе MAT. Например, a- клетка переключится на α-клетку, заменив аллель MAT a аллелем MATα. Эта замена одного аллель MAT для другого возможна потому, что дрожжевые клетки несут дополнительный Silenced копию как MAT а и MATα аллелей: в ЧОЛЕ ( ч omothallic м живать л EFT) локус обычно несет с глушителем копией из MATα аллели, и ГМР ( ч omothallic м живать г РАВО) локус обычно несет с глушителем копию из ВС аллели. Молчаливые H и HMR локусы часто называют немые сопрягаемые кассетами, в качестве информации, присутствующей там «» считывается в активный MAT локуса.
Эти дополнительные копии информации о типе спаривания не вмешиваться в функции от любой аллель присутствует в MAT локус, потому что они не выражены, поэтому гаплоидные клетки с MAT аллель присутствует в активном MAT локусе еще клетка, несмотря на наличие (заглушенной) копии аллеля MATα, присутствующей в HML. Транскрибируется только аллель, присутствующий в активном локусе MAT, и, таким образом, только аллель, присутствующий в MAT, будет влиять на поведение клетки. Локусы скрытого типа спаривания эпигенетически подавляются белками SIR, которые образуют гетерохроматиновый каркас, который предотвращает транскрипцию из молчащих кассет спаривания.
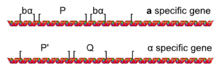 Структура промотора дрожжевого спаривающего типа
Структура промотора дрожжевого спаривающего типа Процесс смены типа спаривания - это событие конверсии гена, инициированное геном HO. HO ген представляет собой ген, жестко регулируется гаплоидными конкретным, который активируется только в гаплоидных клетках во время G 1 фазы от клеточного цикла. Белок, кодируемый HO гена представляет собой ДНК - эндонуклеазой, которая расщепляет ДНК физически, но только в MAT локус (за счет последовательности ДНК специфичности эндонуклеазы HO).
Как только HO разрезает ДНК в MAT, экзонуклеазы притягиваются к разрезанным концам ДНК и начинают разрушать ДНК по обе стороны от сайта разреза. Эта деградация ДНК экзонуклеазами устраняет ДНК, кодирующую аллель MAT ; однако образующийся разрыв в ДНК восстанавливается путем копирования генетической информации, присутствующей в HML или HMR, заполняя новый аллель гена MAT a или MATα. Таким образом, молчащие аллели MAT a и MATα, присутствующие в HML и HMR, служат источником генетической информации для восстановления вызванных HO повреждений ДНК в активном локусе MAT.
Ремонт локуса MAT после разрезания эндонуклеазой HO почти всегда приводит к переключению типа спаривания. Когда a- клетка разрезает аллель MAT a, присутствующий в локусе MAT, разрез в MAT почти всегда будет исправлен путем копирования информации, представленной в HML. Это приводит к тому, что MAT восстанавливается до аллеля MATα, изменяя тип спаривания клетки с a на α. Точно так же α-клетка, аллель MATα которой разрезан эндонуклеазой HO, почти всегда восстанавливает повреждение, используя информацию, представленную в HMR, копируя ген MAT a в локус MAT и переключая тип спаривания α-клетки на a.
Это результат действия энхансера рекомбинации (RE), расположенного на левом плече хромосомы III. Удаление этого региона вызывает клетку неправильного ремонта с использованием HMR. В течение клеток, Mcm1 связывается с RE и способствует рекомбинации области HML. В α-клетках фактор α2 связывается с RE и устанавливает репрессивный домен над RE, так что рекомбинация маловероятна. Врожденная предвзятость означает, что поведение по умолчанию - восстановление с помощью HMR. Точные механизмы этих взаимодействий все еще исследуются.
Ruderfer et al. проанализировали происхождение природных штаммов S. cerevisiae и пришли к выводу, что спаривания, включающие ауткроссинг, происходят только примерно один раз на каждые 50 000 делений клеток. Таким образом, оказывается, что в природе спаривание чаще всего происходит между близкородственными дрожжевыми клетками. Спаривание происходит, когда гаплоидные клетки противоположного типа спаривания MAT a и MATα вступают в контакт. Ruderfer et al. указал, что такие контакты между близкородственными дрожжевыми клетками часты по двум причинам. Первый заключается в том, что клетки противоположного типа спаривания присутствуют вместе в одном аске, мешочке, который содержит клетки, непосредственно продуцируемые одним мейозом, и эти клетки могут спариваться друг с другом. Вторая причина заключается в том, что гаплоидные клетки одного типа спаривания при делении клеток часто производят клетки противоположного типа спаривания, с которыми они могут спариваться (см. Раздел «Переключение типа спаривания» выше). Относительная редкость в природе мейотических событий, возникающих в результате ауткроссинга, по-видимому, несовместима с идеей о том, что производство генетической изменчивости является первичной селективной силой, поддерживающей способность к спариванию в этом организме. Однако это открытие согласуется с альтернативной идеей, что первичная селективная сила, поддерживающая способность к спариванию, - это усиленная рекомбинационная репарация повреждений ДНК во время мейоза, поскольку это преимущество реализуется во время каждого мейоза после спаривания, независимо от того, происходит ли ауткроссинг или нет.
Schizosaccharomyces pombe - это факультативные половые дрожжи, которые могут спариваться при ограничении питательных веществ. Воздействие на S. pombe перекиси водорода, агента, вызывающего окислительный стресс, приводящего к окислительному повреждению ДНК, сильно индуцирует спаривание, мейоз и образование мейотических спор. Это открытие предполагает, что мейоз, и особенно мейотическая рекомбинация, может быть адаптацией для восстановления повреждений ДНК. Общая структуралокуса MAT сходна с таковой у S. cerevisiae. Система переключения сопряженного типа аналогична, но развивалась независимо.
Cryptococcus neoformans - это базидиомицетный гриб, который растет как почкующиеся дрожжи в культуре и на инфицированном хозяине. C. neoformans вызывает опасный для жизни менингоэнцефалит у пациентов с ослабленным иммунитетом. Он претерпевает нитевидный переход во время полового цикла с образованием спор, предполагаемого инфекционного агента. Подавляющее большинство экологических и клинических изолятов C. neoformans относятся к типу спаривания α. Нити обычно имеют гаплоидные ядра, но они могут подвергаться процессу диплоидизации (возможно, посредством эндодупликации или стимулированного ядерного слияния) с образованием диплоидных клеток, называемых бластоспорами. Затем диплоидные ядра бластоспор могут подвергаться мейозу, включая рекомбинацию, с образованием гаплоидных базидиоспор, которые затем могут диспергироваться. Этот процесс называется монокариотическим плодоношением. Для этого процесса необходим ген, обозначенный dmc1, консервативный гомолог генов RecA у бактерий и RAD51 у эукариот. DMC1 опосредует гомологичные хромосомы спаривания в мейозе и ремонта двунитевых разрывов в ДНК (см мейоза ; также Michodдр.). Lin et al. предположили, что одним из преимуществ мейоза у C. neoformans может быть содействие репарации ДНК в среде, повреждающей ДНК, которая может включать защитные реакции инфицированного хозяина.