 | |
 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Бутанал | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| 3DMet | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.004.225 |
| Номер EC |
|
| KEGG | |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| номер ООН | 1129 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C4H8O |
| Молярная масса | 72,11 г / моль |
| Внешний вид | бесцветная жидкость |
| Запах | резкий, альдегидный запах |
| Плотность | 0,8016 г / мл |
| Температура плавления | -96,86 ° C (-142,35 ° F; 176,29 K) |
| Температура кипения | 74,8 ° C (166,6 ° F; 347,9 K) |
| Растворимость в воде | 7,6 г / 100 мл (20 ° C) |
| Растворимость | смешивается с органические растворители |
| log P | 0,88 |
| Магнитная восприимчивость (χ) | -46,08 · 10 см / моль |
| Показатель преломления (nD) | 1,3766 |
| Вязкость | 0,45 сП (20 ° C) |
| Дипольный момент | 2,72 D |
| Термохимия | |
| Стандартная энтальпия. горения (ΔcH298) | 2470,34 кДж / моль |
| Опасности | |
| Паспорт безопасности | Sigma-Aldrich |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Формулировки опасности GHS | H225, H319 |
| Меры предосторожности GHS | P280, P304 + 340, P302 + 352, P210, P305 + 351 + 338 |
| NFPA 704 (огненный алмаз) |  3 3 0 3 3 0 |
| Температура вспышки | −7 ° C (19 ° F; 266 K) |
| Температура самовоспламенения. | 230 ° C (446 ° F; 503 K)) |
| Пределы взрываемости | 1,9–12,5% |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 2490 мг / кг (крыса, перорально) |
| Родственные соединения | |
| Связанный альдегид de | Пропионовый альдегид. Пентаналь |
| Родственные соединения | Бутан-1-ол. Масляная кислота, изобутиральдегид |
| Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
Бутиральдегид, также известный как бутанал, представляет собой органическое соединение с формулой CH 3 (CH 2)2CHO. Это соединение является альдегидным производным бутана. Бесцветная легковоспламеняющаяся жидкость с неприятным запахом. Смешивается с большинством органических растворителей.
Бутиральдегид получают почти исключительно путем гидроформилирования пропилена :
Традиционно гидроформилирование катализировалось комплексами карбонил кобальта, а позднее родиевыми комплексами трифенилфосфина. Доминирующая технология включает использование родиевых катализаторов на основе водорастворимого лиганда tppts. Водный раствор родиевого катализатора превращает пропилен в альдегид, который образует более легкую несмешивающуюся фазу. При гидроформилировании ежегодно производится около 6 миллиардов килограммов. Важным применением является его преобразование в 2-этилгексанол для производства пластификаторов.
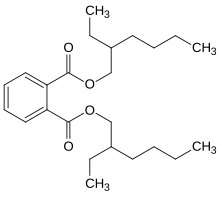 . Основное применение бутиральдегида - производство бис (2-этилгексил) фталата, основной пластификатор.
. Основное применение бутиральдегида - производство бис (2-этилгексил) фталата, основной пластификатор. Бутиральдегид может быть получен каталитическим дегидрированием н-бутанола. Когда-то его производили в промышленности путем каталитического гидрирования кротонового альдегида, который получают из ацетальдегида.
. При длительном воздействии воздуха, бутиральдегид окисляется с образованием масляной кислоты.