 | |
| Names | |
|---|---|
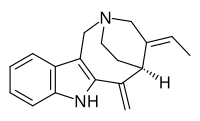
| IUPAC name (2R, 4E, 5S) -4-Этилиден-6-метилиден-1,3,4,5,6,7-гексагидро-2,5-этаноазоцино [4,3-b] индол | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| 3DMet | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| KEGG | |
| PubChem CID | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C18H20N2 |
| Молярная масса | 264,372 г · моль |
| Плотность | 0,945875 |
| log P | 3,404 |
| Кислотность (pK a) | 8,37 |
| Ref индекс активности (nD) | 1,665 |
| Дипольный момент | 0,552121 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Аппарицин - это монотерпеноид индольный алкалоид. Он назван в честь Аппарисио Дуарте, бразильского ботаника, изучавшего виды Aspidosperma, из которых был впервые выделен аппарицин. Это был первый член группы алкалоидов, который был выделен и его структура была установлена, впервые опубликованная в 1965 году. Он также известен под синонимами гомезин, перикалин и табернощизин .
 биосинтез аппарицина и аналогичный путь.
биосинтез аппарицина и аналогичный путь. Алкалоид был выделен из семи видов Aspidosperma. Это основной алкалоид, обнаруженный в каллусе Tabernaemontana elegans, а также был идентифицирован у других видов Tabernaemontana, включая T. africana, Т. divaricata, T. orientalis и T. пахисифон. В исследованиях T. pachysiphon было обнаружено, что содержание алкалоидов, включая аппарицин, было наибольшим в молодых листьях и листьях, получающих большую тень, и варьировалось в зависимости от возраста листа, возраста растения и происхождения.
Исследования Aspidosperma pyricollum привело к открытию того, что аппарицин биосинтезируется из триптофана за счет «потери C-2 и удержания C-3». Биосинтез аппарицина требует изменения обычной триптамина боковой цепи с потерей C-1.
Его структура была установлена с помощью методы химического разложения и возникающего поля разделения ядерного магнитного резонанса (ЯМР) с использованием изотопа H водорода. Ультрафиолетовая спектроскопия в видимой области спектра показали, что аппарицин имеет аналогичное УФ-поглощение, и их хромофоры оказались идентичными.
Эксперименты по разделению ЯМР показали, что аппарицин не имеет сигнала N-метила и имеет один метиленовый атом углерода между атомом азота и индольными кольцами, что позволяет исследователям отличить его от улеина. Это было заметное раннее использование разделения ЯМР для определения химической структуры. Было обнаружено, что его углеродный скелет связан с улеином, но отличается от него, а структуры валлезамина и O-ацетил-валлезамина связаны с аппарицином.
Дегидрирование аппарицина с последующим окисление с помощью перманганата допускает расположение двух углеродных заместителей в кольце пиперидин.
Апарицин может иметь несколько потенциальных применений. В клеточных культурах он показал цитотоксичность в отношении экспериментальной лимфоцитарной лейкемии P388 линии клеток. Он проявляет сильную активность против полиовируса типа 3 (PV3) и от умеренной до сильной активности против некоторых человеческих патогенов. Он также активен в отношении опиоидных рецепторов и имеет микромолярное сродство к аденозиновым рецепторам. Аппарицин имеет местные анальгетические свойства.