| глутаминаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
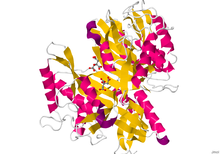 Кристаллографическая структура димерной протеин-глутаминазы из Chryseobacterium proteolyticum. Кристаллографическая структура димерной протеин-глутаминазы из Chryseobacterium proteolyticum. | |||||||||
| Идентификаторы | |||||||||
| EC номер | 3.5.1.2 | ||||||||
| номер CAS | 9001-47-2 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme просмотреть | ||||||||
| KEGG | запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология генов | AmiGO / QuickGO | ||||||||
| |||||||||
| Глутаминаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 вероятная глутаминаза из bacillus subtilis в комплексе с 6-диазо-5-оксо-1-норлейцином вероятная глутаминаза из bacillus subtilis в комплексе с 6-диазо-5-оксо-1-норлейцином | |||||||||
| Идентификаторы | |||||||||
| Символ | Глютаминаза | ||||||||
| Pfam | PF04960 | ||||||||
| Pfam clan | CL0013 | ||||||||
| InterPro | IPR015868 | ||||||||
| SCOPe | 1mki / SUPFAM | ||||||||
| |||||||||
глутаминаза (EC 3.5.1.2, глутаминаза I, L-глутаминаза, глутаминогидролаза) представляет собой фермент амидогидролаза , который генерирует глутамат из глутамина. Глутаминаза имеет тканеспецифические изоферменты. Глутаминаза играет важную роль в глиальных клетках.
Глутаминаза катализирует следующую реакцию:
Глютамин + H 2 O → глутамат + NH 3
Глутаминаза экспрессируется и активна в перипортальных гепатоцитах, где она генерирует NH 3 (аммиак) для синтеза мочевины, как и глутаматдегидрогеназа. Глутаминаза также экспрессируется в эпителиальных клетках почечных канальцев, где произведенный аммиак выводится в виде ионов аммония. Выведение ионов аммония является важным механизмом кислотно-щелочной регуляции почек. Во время хронического ацидоза в почках индуцируется глутаминаза, что приводит к увеличению количества выводимых ионов аммония. Глутаминаза также может быть обнаружена в кишечнике, при этом уровень аммиака воротной вены печени может достигать 0,26 мМ (по сравнению с аммиаком артериальной крови 0,02 мМ).
Одна из наиболее важных ролей глутаминазы обнаруживается в терминалях аксонов нейронов в центральной нервной системе. Глутамат является наиболее часто используемым возбуждающим нейромедиатором в ЦНС. После высвобождения в синапс для нейротрансмиссии глутамат быстро поглощается ближайшими астроцитами, которые превращают его в глутамин. Затем этот глутамин доставляется в пресинаптические терминалы нейронов, где глутаминазы превращают его обратно в глутамат для загрузки в синаптические пузырьки. Хотя глутаминазы «почечного» (GLS1) и «печеночного» (GLS2) типа экспрессируются в головном мозге, GLS2 существует только в клеточных ядрах нейронов ЦНС.
АДФ. является сильнейшим адениннуклеотидным активатором глутаминазы. Исследования также показали, что АДФ снижает Km для глутамина и увеличивает V max. Они обнаружили, что эти эффекты усиливались еще больше, когда присутствовал АТФ.
Предполагается, что активированная фосфатом митохондриальная глутаминаза (GLS1) связана с повышенным метаболизмом, уменьшением внутриклеточных активных форм кислорода (ROS) и общее снижение окисления ДНК как в нормальных, так и в стрессовых клетках. Предполагается, что контроль GLS2 уровней ROS способствует «способности p53 защищать клетки от накопления геномных повреждений и позволяет клеткам выживать после легкого и поддающегося восстановлению генотоксического стресса».
структура глутаминазы была определена с помощью дифракции рентгеновских лучей с разрешением до 1,73 Å. Имеется 2 цепи, содержащие 305 остатков, которые составляют длину этого димерного белка. На каждой цепи 23% аминокислот, или 71 остаток, находятся в 8 спиралях. Двадцать один процент, или 95 остатков, составляют 23 цепи бета-листов.
Люди экспрессируют 4 изоформы глутаминазы. GLS кодирует 2 типа глутаминазы почечного типа с высокой активностью и низким Km. GLS2 кодирует 2 формы глутаминазы печеночного типа с низкой активностью и аллостерической регуляцией.
|
| ||||||||||||||||||||||||||||||||||||||||||||
Глутаминазы принадлежат к большему семейству, которое включает серинзависимые бета-лактамазы и пенициллин-связывающие белки. Многие бактерии имеют два изофермента. Эта модель основана на выбранных известных глутаминазах и их гомологах в прокариотах, за исключением высокопроизводных (длинноразветвленных) и архитектурно различающихся гомологов, чтобы добиться консервативного назначения. Резкое падение оценок происходит на ниже 250, и пороговые значения устанавливаются соответственно. Фермент превращает глутамин в глутамат с высвобождением аммиака. Члены, как правило, описываются как глутаминаза A (glsA), где B (glsB) неизвестен и может не быть гомологичным (как в Rhizobium etli; некоторые виды имеют два изофермента, которые могут быть обозначены как A (GlsA1 и GlsA2).
Многие виды рака зависят от глутаминазы, поэтому для лечения рака были предложены ингибиторы глутаминазы. По состоянию на июль 2018 года некоторые ингибиторы глутаминазы находятся на промежуточной стадии клинических испытаний.