Деметилирование - это химический процесс, приводящий к удалению метильной группы (CH 3) из молекулы. Распространенным способом деметилирования является замена метильной группы на атом водорода, что приводит к чистой потере одного атома углерода и двух атомов водорода.
Аналог деметилирования - метилирование.
В биохимических системах процесс деметилирования катализируется деметилазами. Эти ферменты окисляют N-метильные группы, которые присутствуют в гистонах и некоторых формах ДНК:
Одним из таких семейств окислительных ферментов является цитохром P450. Альфа-кетоглутарат-зависимые гидроксилазы активны в деметилировании ДНК, действуя аналогичным путем. В этих реакциях используется слабая связь C-H, прилегающая к аминам.
 Превращение 5-метилцитозина в 5-гидроксиметилцитозин ферментом TET плюс α-кетоглутарат и Fe (II)
Превращение 5-метилцитозина в 5-гидроксиметилцитозин ферментом TET плюс α-кетоглутарат и Fe (II) В частности, 5-метилцитозины в ДНК могут быть деметилированы с помощью ферментов TET, как показано на рисунке. Во время эмбриогенеза у мыши около 20 миллионов 5-метилцитозинов деметилируются в течение шести часов сразу после оплодотворения яйцеклетки спермой с образованием зиготы. Ферменты ТЕТ представляют собой диоксигеназы из семейства альфа-кетоглутарат-зависимых гидроксилаз. Фермент ТЕТ представляет собой альфа-кетоглутарат (α-KG) -зависимую диоксигеназу, которая катализирует реакцию окисления путем включения одного атома кислорода из молекулярного кислорода (O 2) в свой субстрат, 5 -метилцитозин в ДНК (5mC), чтобы произвести продукт 5-гидроксиметилцитозин в ДНК. Это преобразование сочетается с окислением вспомогательного субстрата α-KG до сукцината и диоксида углерода (см. Рисунок).
Первый этап включает связывание α-KG и 5-метилцитозина с активным сайтом фермента ТЕТ. Каждый из ферментов TET имеет основной каталитический домен с двухцепочечной β-спиральной складкой, которая содержит важные металлсвязывающие остатки, обнаруженные в семействе Fe (II) / α-KG-зависимых оксигеназ. α-KG координируется как бидентатный лиганд (связанный в двух точках) с Fe (II) (см. рисунок), в то время как 5mC удерживается нековалентной силой В непосредственной близости. Активный сайт TET содержит высококонсервативный мотив триады, в котором каталитически важный Fe (II) удерживается двумя остатками гистидина и одним остатком аспарагиновой кислоты (см. Рисунок). Триада связывается с одной стороной центра Fe, оставляя три лабильных сайта, доступных для связывания α-KG и O 2 (см. Рисунок). Затем TET превращает 5-метилцитозин в 5-гидроксиметилцитозин, в то время как α-кетоглутарат превращается в сукцинат и CO 2.
Деметилирование обычно относится к расщеплению простых эфиров., особенно ариловые эфиры, хотя есть некоторые исключения, например см. «дезипрамин ».
Арилметиловые эфиры широко распространены в лигнине и многих производных соединениях. Деметилирование этих материалов потребовало больших усилий. Для реакции обычно требуются суровые условия или жесткие реагенты. Например, метиловый эфир в ванилине можно удалить нагреванием до 250 ° C с сильным основанием. Более сильные нуклеофилы, такие как диорганофосфиды (LiPPh 2), также расщепляют ариловые эфиры в более мягких условиях. Другие использованные сильные нуклеофилы включают соли тиолатов, такие как EtSNa.
Также можно использовать кислотные условия. Исторически сложилось так, что арилметиловые эфиры, включая натуральные продукты, такие как кодеин (O-метилморфин), деметилировали путем нагревания вещества в расплавленном гидрохлориде пиридина (т.пл.144 ° C) при 180-220 ° C, иногда с избытком хлористого водорода в процесс, известный как расщепление эфира Цейзеля – Прей. Количественный анализ ароматических метиловых эфиров может быть выполнен аргентометрическим определением образовавшегося хлорида N-метилпиридиния. Механизм этой реакции начинается с переноса протона от иона пиридиния к арилметиловому эфиру, что является крайне неблагоприятной стадией (K < 10) that accounts for the harsh conditions required, given the much weaker acidity of pyridinium (pKa= 5,2) по сравнению с протонированным арилметиловым эфиром (ионом арилметилоксония, pK a = –6,7 для арил = Ph). За этим следует атака S N 2 иона арилметилоксония по метильной группе либо пиридином, либо ионом хлорида (в зависимости от субстрата) с образованием свободного фенола и, в конечном итоге, хлорида N-метилпиридиния, либо непосредственно или путем последующего переноса метила от хлористого метила к пиридину.

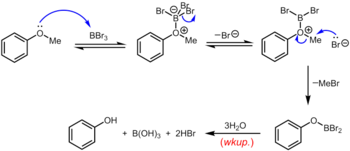
Другой классический (но опять-таки суровый) метод удаления метильной группы арилметилового эфира заключается в нагревании эфира с обратным холодильником в растворе бромистого водорода или водорода. йодид в уксусной кислоте (точка кипения 118 ° C) или концентрированной бромистоводородной или йодистоводородной кислоте. Расщепление простых эфиров бромистоводородной или йодистоводородной кислотой происходит по очень похожему механизму, в котором высококислотный HBr или HI служит для протонирования эфира с последующим замещением бромидом или йодидом, оба из которых являются отличными нуклеофилами. В несколько более мягких условиях используется циклогексилиодид (CyI, 10,0 экв.) В N, N-диметилформамиде для образования небольшого количества иодистого водорода in situ. Трибромид бора, который можно использовать при комнатной температуре или ниже, представляет собой более специализированный реагент для деметилирования арилметиловых эфиров. Механизм деалкилирования эфира протекает через начальное обратимое образование аддукта кислота-основание Льюиса между сильно кислотным по Льюису BBr 3 и основным эфиром Льюиса. Этот аддукт Льюиса может обратимо диссоциировать с образованием дибромоборилоксониевого катиона и Br. Разрыв простой эфирной связи происходит в результате последующей нуклеофильной атаки оксониевых частиц со стороны Br с образованием арилоксидибромоборана и бромистого метила. По завершении реакции фенол высвобождается вместе с борной кислотой (H 3BO3) и бромистоводородной кислотой (водный HBr) при гидролизе производного дибромоборана во время водной обработки.
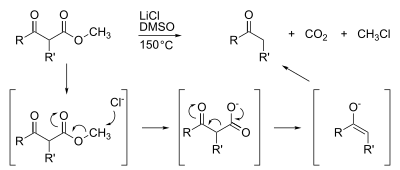
. Метиловые эфиры также подвержены деметилированию, которое обычно достигается омылением. Широко распространено высокоспециализированное деметилирование, такое как декарбоксилирование Крапчо :
N-деметилирование 3 ° аминов по реакции фон Брауна, в которой используется BrCN в качестве реагента для получения соответствующих нор- производных. Был разработан современный вариант реакции Фон Брауна, в котором BrCN был заменен на этилхлорформиат. Получение паксила из ареколина является применением этой реакции, а также, например, для синтеза GSK-372,475.