 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Бромистый водород | |||
| Систематическое название ИЮПАК Броман | |||
| Идентификаторы | |||
| Количество CAS | |||
| 3D модель ( JSmol ) | |||
| Ссылка на Beilstein | 3587158 | ||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.090 | ||
| Номер ЕС | |||
| КЕГГ | |||
| MeSH | Бромистоводородная + кислота | ||
| PubChem CID | |||
| Номер RTECS | |||
| UNII | |||
| Номер ООН | 1048 | ||
| Панель управления CompTox ( EPA) | |||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
| Химическая формула | HBr | ||
| Молярная масса | 80,91 г / моль | ||
| Появление | Бесцветный газ | ||
| Запах | Едкий | ||
| Плотность | 3,307 г / мл (25 ° С) | ||
| Температура плавления | -86,9 ° С (-124,4 ° F, 186,2 К) | ||
| Точка кипения | -66,8 ° С (-88,2 ° F, 206,3 К) | ||
| Растворимость в воде | 221 г / 100 мл (0 ° C) 204 г / 100 мл (15 ° C) 193 г / 100 мл (20 ° C) 130 г / 100 мл (100 ° C) | ||
| Растворимость | Растворим в спирте, органических растворителях | ||
| Давление газа | 2,308 МПа (при 21 ° C) | ||
| Кислотность (p K a) | -8,8 (± 0,8); ~ −9 | ||
| Основность (p K b) | ~ 23 | ||
| Конъюгированная кислота | Бромоний | ||
| Основание конъюгата | Бромид | ||
| Показатель преломления ( n D) | 1,325 | ||
| Структура | |||
| Молекулярная форма | Линейный | ||
| Дипольный момент | 820 мД | ||
| Термохимия | |||
| Теплоемкость ( C) | 350,7 мДж / (К г) | ||
| Стандартная мольная энтропия ( S | 198,696–198,704 Дж / (К моль) | ||
| Std энтальпия формации (Δ F H ⦵298) | −36,45...− 36,13 кДж / моль | ||
| Опасности | |||
| Паспорт безопасности | hazar.com | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| Положения об опасности GHS | H314, H335 | ||
| Меры предосторожности GHS | P261, P280, P305 + 351 + 338, P310 | ||
| NFPA 704 (огненный алмаз) |  3 0 0 COR 3 0 0 COR | ||
| Смертельная доза или концентрация (LD, LC): | |||
| ЛК 50 ( средняя концентрация ) | 2858 частей на миллион (крыса, 1 час ) 814 частей на миллион (мышь, 1 час) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (Допустимо) | TWA 3 частей на миллион (10 мг / м 3) | ||
| REL (рекомендуется) | TWA 3 частей на миллион (10 мг / м 3) | ||
| IDLH (Непосредственная опасность) | 30 частей на миллион | ||
| Родственные соединения | |||
| Родственные соединения | Фтористый водород Хлороводород Йодистый водород Астатид водорода | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| | |||
| Ссылки на инфобоксы | |||
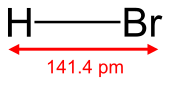
Бромистый водород - это неорганическое соединение с формулой H Br. Это галогенид водорода, состоящий из водорода и брома. Бесцветный газ, он растворяется в воде, образуя бромистоводородную кислоту, насыщенность которой составляет 68,85% HBr по массе при комнатной температуре. Водные растворы, которые содержат 47,6% HBr по массе, образуют постоянно кипящую азеотропную смесь, которая кипит при 124,3 ° C. При кипячении менее концентрированных растворов выделяется H 2 O до тех пор, пока не будет достигнут состав смеси с постоянным кипением.
Бромистый водород и его водный раствор являются обычно используемыми реагентами для получения бромидных соединений.
Бромистый водород и бромистоводородная кислота являются важными реагентами в производстве броморганических соединений. В свободнорадикальной реакции HBr присоединяется к алкенам:
Полученные алкилбромиды являются полезными алкилирующими агентами, например, в качестве предшественников производных жирных аминов. Связанные присоединения свободных радикалов к аллилхлориду и стиролу дают 1-бром-3-хлорпропан и фенилэтилбромид соответственно.
Бромистый водород реагирует с дихлорметаном с образованием бромхлорметана и дибромметана, последовательно:
Эти реакции метатезиса иллюстрируют потребление более сильной кислоты (HBr) и высвобождение более слабой кислоты (HCl).
Аллилбромид получают обработкой аллилового спирта HBr:
HBr присоединяется к алкинам с образованием бромалкенов. Стереохимия этого типа того, как правило, анти:
Кроме того, HBr добавляет эпоксиды и лактоны, что приводит к размыканию кольца.
С трифенилфосфином HBr дает бромид трифенилфосфония, твердый «источник» HBr.
Ванадий бромид (III) и молибдена (IV), бромид были получены обработкой высших хлоридов с HBr. Эти реакции протекают через окислительно-восстановительные реакции:
Бромистый водород (вместе с бромистоводородной кислотой) получают путем объединения водорода и брома при температурах от 200 до 400 ° C. Реакция обычно катализируется платиной или асбестом.
HBr может быть получен перегонкой раствора бромида натрия или бромида калия с фосфорной или серной кислотой :
Концентрированная серная кислота менее эффективна, поскольку окисляет HBr до брома :
Кислота может быть получена:
Безводный бромистый водород также может быть получен в небольшом масштабе термолизом трифенилфосфонийбромида в кипящем с обратным холодильником ксилоле.
Бромистый водород, полученный указанными выше способами, может быть загрязнен Br 2, который можно удалить, пропустив газ через раствор фенола при комнатной температуре в тетрахлорметане или другом подходящем растворителе (с получением 2,4,6-трибромфенола и образованием большего количества HBr в процесс) или через медную стружку или медную сетку при высокой температуре.
HBr вызывает сильную коррозию и раздражает при вдыхании.