 | ||
 | ||
| Клинические данные | ||
|---|---|---|
| Произношение | de FER a sir ox | |
| Торговые наименования | Exjade, Jadenu | |
| Другие названия | CGP-72670, ICL-670A, IC L670 | |
| AHFS / Drugs.com | Монография | |
| Данные лицензии |
| |
| Беременность. категория |
| |
| Способы введения. | Устно | |
| Код ATC | ||
| Правовой статус | ||
| Юридический статус | ||
| фармакокинетика данные | ||
| Биодоступность | 70% | |
| Связывание с белками | 99% | |
| Метаболизм | Печень глюкуронизация | |
| Период полувыведения | от 8 до 16 часов | |
| Экскреция | Кал (84%) и почки (8%) | |
| Идентификаторы | ||
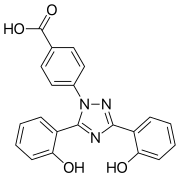
Название ИЮПАК
| ||
| Номер CAS | ||
| PubChem CID | ||
| DrugBank | ||
| ChemSpider | ||
| UNII | ||
| KEGG | ||
| ChEBI | ||
| ChEMBL |
| |
| ECHA InfoCard | 100.211.077 | |
| Химические и физические данные | ||
| Формула | C21H15N3O4 | |
| Молярная масса | 373,368 г · моль | |
| 3D модель (JSmol ) | ||
| Плотность | 1,4 ± 0,1 г / см | |
УЛЫБКИ
| ||
InChI
| ||
| (что это?) | ||
Деферасирокс, продаваемый, среди прочего, под торговой маркой Exjade, представляет собой пероральный хелатор железа хелатор. Его основное применение - уменьшить хроническую перегрузку железом у пациентов, длительно получающих переливание крови при таких состояниях, как бета- талассемия и другие хронические анемии. Это первое пероральное лекарство, одобренное для этой цели в США.
Оно было одобрено Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США в ноябре 2005 г. По данным FDA (май 2007), почечная недостаточность и цитопения были зарегистрированы у пациентов, получавших пероральные таблетки суспензии деферасирокса. Он одобрен в Европейском Союзе Европейским агентством по лекарственным средствам (EMA) для детей шести лет и старше при хронической перегрузке железом в результате повторных переливаний крови.
В июле 2020 года Teva решила прекратить деферасирокс. Он доступен как непатентованный препарат.
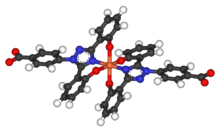 Две молекулы деферасирокса связывают железо
Две молекулы деферасирокса связывают железо Период полувыведения деферасирокса составляет от 8 до 16 часов с учетом дозировки один раз в день. Две молекулы деферасирокса способны связываться с 1 атомом железа, которые впоследствии выводятся с калом. Его низкий молекулярный вес и высокая липофильность позволяют принимать препарат перорально, в отличие от дефероксамина, который необходимо вводить внутривенно (внутривенная инфузия). Вместе с деферипроном деферасирокс, по-видимому, способен удалять железо из клеток (сердечных миоцитов и гепатоцитов), а также удалять железо из крови.
Деферазирокс может быть получен из простых коммерчески доступных исходных материалов (салициловая кислота, салициламид и 4-гидразинобензойная кислота) в следующей двухстадийной последовательности синтеза:

Конденсация салицилоила хлорид (образованный in situ из салициловой кислоты и тионилхлорида) с салициламидом в условиях реакции дегидратации приводит к образованию 2- (2-гидроксифенил) -1,3 (4H) -бензоксазин-4-она. Этот промежуточный продукт выделяют и подвергают взаимодействию с 4-гидразинобензойной кислотой в присутствии основания с получением 4- (3,5-бис (2-гидроксифенил) -1,2,4-триазол-1-ил) бензойной кислоты (деферазирокс).
Деферасирокс был препаратом №2 в списке «Наиболее частые подозреваемые препараты в зарегистрированных случаях смерти пациентов», составленном Институтом безопасной медицинской практики в 2009 году. Было зарегистрировано 1320 смертей, возможно, это объясняется обновлением данных ADE компании Novartis и новым предупреждением в рамке о желудочно-кишечном кровотечении, а также почечной и печеночной недостаточности.