| |||
 | |||
| Названия | |||
|---|---|---|---|
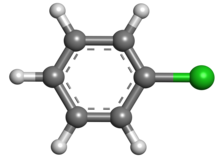
| Предпочтительное название IUPAC Хлорбензол | |||
| Другие названия Фенилхлорид | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| 3DMet | |||
| Сокращения | PhCl | ||
| Ссылка Beilstein | 605632 | ||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.003.299 | ||
| Номер EC |
| ||
| Справочник Гмелина | 26704 | ||
| KEGG | |||
| PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1134 | ||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
SMILES
| |||
| Свойства | |||
| Химическая формула | C6H5Cl | ||
| Молярная масса | 112,56 г / моль | ||
| Ap внешний вид | бесцветная жидкость | ||
| Запах | миндальный | ||
| Плотность | 1,11 г / см, жидкость | ||
| Точка плавления | -45 ° C (-49 ° F; 228 K) | ||
| Температура кипения | 131 ° C (268 ° F; 404 K) | ||
| Растворимость в воде | 0,5 г в воде при 20 ° C | ||
| Растворимость в других растворителях | растворим в большинстве органических растворителей | ||
| Давление пара | 9 мм рт. Ст. | ||
| Магнитная восприимчивость (χ) | -69,97 · 10 см / моль | ||
| Опасности | |||
| Данные по безопасности лист | См.: страница данных | ||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Предупреждение | ||
| Краткая характеристика опасности GHS | H226, H315, H332, H411 | ||
| Меры предосторожности GHS | P210, P233, P240, P241, P242, P243, P261, P264, P271, P273, P280, P302 + 352, P303 + 361 + 353, P304 + 312, P304 + 340, P312, P321, P332 + 313, P362, P370 + 378, P391, P403 + 235, P501 | ||
| NFPA 704 (огненный алмаз) |  3 2 0 3 2 0 | ||
| Температура вспышки | 29 ° C (84 ° F; 302 K) | ||
| Взрывоопасно пределы | 1,3% -9,6% | ||
| Летальная доза или концентрация (LD, LC): | |||
| LD50(средняя доза ) | 2290 мг / кг (крыса, перорально). 2250 мг / кг (кролик, перорально). 2300 мг / кг (мышь, перорально). 2250 мг / кг (морская свинка, перорально) | ||
| LCLo(самый низкий опубликованный ) | 8000 ppm (кошка, 3 часа) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (допустимый) | TWA 75 ppm (350 мг / м) | ||
| REL (рекомендуется) | нет | ||
| IDLH (непосредственная опасность) | 1000 ppm | ||
| родственные соединения | |||
| родственные Галобензолы | Фторбензол. Бромбензол. Йодбензол | ||
| Родственные соединения | бензол. 1,4-дихлорбензол | ||
| Страница дополнительных данных | |||
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. Д. | ||
| Термодинамические. данные | Фазовое поведение. твердое тело – жидкость – газ | ||
| Спектральный данные | UV, IR, ЯМР, MS | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Хлорбензол представляет собой ароматическое органическое соединение wi химическая формула C 6H5Cl. Эта бесцветная легковоспламеняющаяся жидкость является обычным растворителем и широко используемым промежуточным продуктом при производстве других химикатов.
хлорбензол используется в основном в качестве промежуточного продукта при производстве таких товаров, как гербициды, красители и каучук. Хлорбензол также используется в качестве высококипящего растворителя во многих промышленных применениях, а также в лаборатории. Хлорбензол нитруют в крупном масштабе с получением смеси 2-нитрохлорбензола и 4-нитрохлорбензола, которые разделяют. Эти мононитрохлорбензолы превращаются в родственный 2-нитрофенол, 2-нитроанизол, бис (2-нитрофенил) дисульфид и 2-нитроанилин путем нуклеофильного замещения хлорида, соответственно с гидроксид натрия, метоксид натрия, дисульфид натрия и аммиак. Конверсии 4-нитропроизводного аналогичны.
Хлорбензол когда-то использовался при производстве некоторых пестицидов, в первую очередь ДДТ, путем реакции с хлорал (трихлорацетальдегид), но это применение сократилось из-за сокращения использования ДДТ. Когда-то хлорбензол был основным прекурсором для производства фенола :
. Побочным продуктом реакции также была соль. Реакция известна как процесс Доу, при котором реакцию проводят при 350 ° C с использованием конденсированного гидроксида натрия без растворителя. Эксперименты по маркировке показывают, что реакция протекает путем удаления / добавления с использованием бензина в качестве промежуточного соединения.
Впервые было описано в 1851 году. Хлорбензол получают путем хлорирования бензола в присутствии каталитического количества Кислота Льюиса, такая как хлорид железа, дихлорид серы и безводный хлорид алюминия :

. Катализатор увеличивает электрофильность хлора. Поскольку хлор электроотрицателен, C 6H5Cl проявляет несколько пониженную чувствительность к дальнейшему хлорированию. Промышленно реакция проводится как непрерывный процесс, чтобы минимизировать образование дихлорбензолов.
Хлорбензол получают из анилина через хлорид бензолдиазония, иначе известная как реакция Сандмейера.
Хлорбензол проявляет токсичность от "низкой до умеренной", на что указывает его LD50 2,9 г / кг. Управление по охране труда установило допустимый предел воздействия на уровне 75 частей на миллион (350 мг / м3) в течение восьми часов, взвешенных по времени, для рабочих, работающих с хлорбензолом.
Хлорбензол может сохраняться в почве в течение нескольких месяцев, в воздухе около 3,5 дней и в воде менее одного дня. Люди могут подвергаться воздействию этого агента при вдыхании зараженного воздуха (в основном в результате профессионального воздействия), употреблении загрязненной пищи или воды или при контакте с загрязненной почвой (обычно вблизи мест хранения опасных отходов). Однако, поскольку он был обнаружен только на 97 из 1177 участков опасных отходов NPL, он не считается широко распространенным загрязнителем окружающей среды. Бактерия Rhodococcus phenolicus разлагает хлорбензол как единственный источник углерода.
Попадая в организм, обычно через загрязненный воздух, хлорбензол выводится как через легкие, так и через мочевыводящую систему.
В 2015 году научная группа SAM объявила, что марсоход Curiosity сообщил о доказательствах более высоких концентраций хлорбензола в осадочной породе., названный «Камберленд », на Марсе. Команда предположила, что хлорбензол мог образоваться при нагревании образца в камере для отбора проб. Нагревание вызвало бы реакцию органических веществ в марсианской почве, которая, как известно, содержит перхлорат.