 | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.013.764 |
| Номер ЕС |
|
| Номер E | E930 (глазури,...) |
| Справочник Гмелина | 674257 |
| KEGG | |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| номер ООН | 1457 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
| Химическая формула | CaO 2 |
| Молярная масса | 72,0768 г / моль |
| Внешний вид | белый или желтоватый порошок |
| Запах | без запаха |
| Плотность | 2,91 г / см |
| Температура плавления | ~ 355 ° C (671 ° F; 628 K) (разлагается) |
| Растворимость в воде | разлагает |
| Кислотность (pK a) | 12,5 |
| Магнитная восприимчивость (χ) | -23,8 · 10 см / моль |
| Показатель преломления (nD) | 1,895 |
| Структура | |
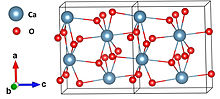
| Кристаллическая структура | Орторомбическая |
| Пространственная группа | Pna2 1 |
| Координационная геометрия | 8 |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнал GHS word | Предупреждение |
| Формулировки опасности GHS | H272, H315, H319, H335 |
| Меры предосторожности GHS | P210, P220, P221, P261, P264, P271, P280, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P370 + 378, P403 + 233, P405, P501 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | >5000 мг / кг (перорально, крыса).>10000 мг / кг (кожный, крыса) |
| Родственные соединения | |
| Другие анионы | Оксид кальция |
| Другие катионы | Пероксид стронция. Пероксид бария. Пероксид натрия |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Пероксид кальция или диоксид кальция - это неорганическое соединение с формулой CaO 2. Это пероксид (O2) соль Ca. Коммерческие образцы могут быть желтоватыми, но чистое соединение - белым. Практически нерастворим в воде.
В твердом виде, он относительно устойчив к разложению. Однако при контакте с водой он гидролизуется с выделением кислорода. При обработке кислотой образуется пероксид водорода.
Пероксид кальция получают путем объединения солей кальция и пероксида водорода <228.>Ca (OH) 2 + H 2O2→ CaO 2 + 2 H 2O Октагидрат выпадает в осадок при реакции гидроксида кальция с разбавленным перекись водорода. При нагревании он обезвоживается. Он в основном используется в качестве окислителя для увеличения извлечения драгоценных металлов из их руд. Во втором основном применении он используется как пищевая добавка под номером E E930, он используется как отбеливающий агент и улучшающий агент. В сельском хозяйстве используется для предпосевных обработок. Также пероксид кальция нашел применение в аквакультуре для насыщения кислородом и дезинфекции воды. В экологической восстановительной промышленности он используется для обработки почв. Пероксид кальция используется аналогично пероксиду магния в программах восстановления окружающей среды. Он используется для восстановления почвы и грунтовых вод, загрязненных нефтью, с помощью процесса усиленной биоремедиации на месте. . Он также используется для отверждения полимеров на основе простого политиоэфира путем окисления концевых тиоловых групп до дисульфидных мостиков.