| Белки-регуляторы апоптоза, семейство Bcl-2 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
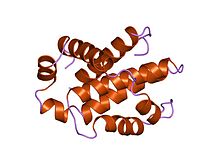 Структура человеческого Bcl-xL, ингибитора запрограммированной гибели клеток. Структура человеческого Bcl-xL, ингибитора запрограммированной гибели клеток. | |||||||||
| Идентификаторы | |||||||||
| Символ | Bcl-2 | ||||||||
| Pfam | PF00452 | ||||||||
| InterPro | IPR002475 | ||||||||
| SMART | SM00337 | ||||||||
| PROSITE | PDOC00829 | ||||||||
| SCOPe | 1maz / SUPFAM | ||||||||
| суперсемейство OPM | 40 | ||||||||
| белок OPM | 2l5b | ||||||||
| Мембранома | 232 | ||||||||
| |||||||||
Семейство Bcl-2 (TC # 1.A.21 ) состоит из ряда эволюционно сохраняемых белки, которые имеют общие домены Bcl-2 гомологии (BH). Семейство Bcl-2 наиболее известно своей регуляцией апоптоза, формы запрограммированной гибели клеток, в митохондрии. Белки семейства Bcl-2 состоят из членов, которые либо способствуют, либо ингибируют апоптоз и контролируют апоптоз, управляя проницаемостью внешней мембраны митохондрий (MOMP), которая является ключевым этапом внутреннего пути апоптоза. К 2008 г. было идентифицировано всего 25 генов семейства Bcl-2.
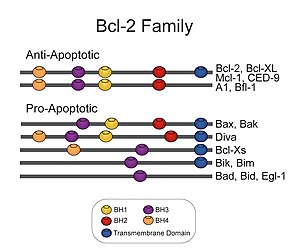 Домены семейства Bcl-2
Домены семейства Bcl-2 Белки семейства Bcl-2 имеют общую структуру, состоящую из гидрофобной α-спирали, окруженной амфипатическими α-спиралями. Некоторые члены этого семейства имеют трансмембранные домены на своем С-конце, которые в первую очередь функционируют для их локализации в митохондрии.
Bcl-x (L) имеет длину 233 аминоацильных остатка (aas) и демонстрирует один очень гидрофобный предполагаемый трансмембранный α-спиральный сегмент (остатки 210-226) в мембране. Гомологи Bcl-x включают белки Bax (крыса; 192 аминокислотных остатка) и Bak (мышь; 208 аминокислотных остатков), которые также влияют на апоптоз. Структура с высоким разрешением мономерной растворимой формы человеческого Bcl-x (L) была определена как с помощью рентгеновской кристаллографии, так и ЯМР.
Структура состоит из двух центральных преимущественно гидрофобных α-спиралей, окруженных амфипатическими спиралями.. Расположение α-спиралей в Bcl-X (L) напоминает таковое для дифтерийного токсина и колицинов. Токсин дифтерии образует трансмембранную пору и перемещает токсичный каталитический домен в цитоплазму животных клеток. Колицины также образуют поры в липидных бислоях. Следовательно, структурная гомология предполагает, что члены семейства Bcl-2, которые содержат домены BH1 и BH2 (Bcl-X (L), Bcl-2 и Bax), действуют аналогичным образом.
Члены семейства Bcl-2 разделяют один или несколько из четырех характерных доменов гомологии, названных гомологией Bcl-2. (BH) домены (названные BH1, BH2, BH3 и BH4) (см. Рисунок). Известно, что домены BH имеют решающее значение для функции, поскольку делеция этих доменов посредством молекулярного клонирования влияет на выживаемость / скорость апоптоза. Белки против апоптоза Bcl-2, такие как Bcl-2 и Bcl-xL, сохраняют все четыре домена BH. Домены BH также служат для подразделения проапоптотических белков Bcl-2 на белки с несколькими доменами BH (например, Bax и Bak) или на те белки, которые имеют только домен BH3 (например, Bim Bid и BAD )
Все белки, принадлежащие к семейству Bcl-2, содержат домен BH1, BH2, BH3 или BH4. Все антиапоптотические белки содержат домены BH1 и BH2, некоторые из них содержат дополнительные N-концевой домен BH4 (Bcl-2, Bcl-x (L) и Bcl-w), который также наблюдается в некоторых проапоптотических белках, таких как Bcl-x (S), Diva, Bok-L и Bok-S. С другой стороны, все проапоптотические белки содержат домен BH3, необходимый для димеризации с другими белками семейства Bcl-2 и решающий для их киллинговой активности, некоторые из них также содержат домены BH1 и BH2 (Bax и Bak) Домен BH3 также присутствует в некоторых антиапоптотических белках, таких как Bcl-2 или Bcl-x (L). Три функционально важных области гомологии Bcl-2 (BH1, BH2 и BH3) находятся в непосредственной пространственной близости. сформировать удлиненный ключ t, который может обеспечивать сайт связывания для других членов семейства Bcl-2.
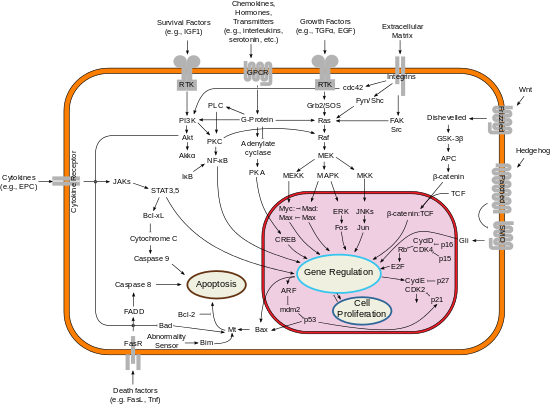 Обзор путей передачи сигнала, участвующих в апоптозе.
Обзор путей передачи сигнала, участвующих в апоптозе.Регулируемая гибель клеток (апоптоз ) индуцируется такими событиями, как фактор роста синдром отмены и токсины. Он контролируется регуляторами, которые либо оказывают ингибирующее действие на запрограммированную гибель клеток (антиапоптотические), либо блокируют защитный эффект ингибиторов (проапоптотические). Многие вирусы нашли способ противодействовать защитному апоптозу, кодируя собственные антиапоптозные гены, не позволяя своим клеткам-мишеням умирать слишком рано.
Bcl-x является доминантным регулятором запрограммированной гибели клеток в клетках млекопитающих. Длинная форма (Bcl-x (L), демонстрирует активность репрессора гибели клеток, но короткая изоформа (Bcl-x (S)) и β-изоформа (Bcl-xβ) способствуют гибели клеток. Bcl -x (L), Bcl-x (S) и Bcl-xβ - три изоформы, полученные альтернативным сплайсингом РНК.
Существует ряд теорий относительно того, как семейство генов Bcl-2 проявляют свой про- или антиапоптотический эффект. Важный из них утверждает, что это достигается путем активации или инактивации внутренней поры перехода проницаемости митохондрий, которая участвует в регуляции матрицы Ca, pH и напряжения Также считается, что некоторые белки семейства Bcl-2 могут индуцировать (проапоптотические члены) или ингибировать (антиапоптотические члены) высвобождение цитохрома с в цитозоль, который, оказавшись там, активирует каспазу-9 и каспазу-3, что приводит к апоптозу. Хотя Замзами и др. предполагают, что высвобождение цитохрома с косвенно опосредуется порой PT на внутренней митохондриальной мембране, убедительные доказательства указывают на наличие уха Более важное значение поры MAC на внешней мембране.
Другая теория предполагает, что белки Rho играют роль в активации Bcl-2, Mcl-1 и Bid. Ингибирование Rho снижает экспрессию антиапоптотических белков Bcl-2 и Mcl-1 и увеличивает уровни проапоптотических белков Bid, но не влияет на уровни Bax или FLIP. Ингибирование Rho вызывает каспазу-9 и каспазу-3-зависимый апоптоз культивируемых эндотелиальных клеток человека.
Эти белки локализованы на внешней митохондриальной мембране клетки животного, где они и находятся Предполагается, что они образуют комплекс с зависимым от напряжения анионным каналом порином (VDAC). Взаимодействие Bcl-2 с VDAC1 или пептидами, полученными из VDAC3, защищает от гибели клеток, ингибируя высвобождение цитохрома c. Было продемонстрировано прямое взаимодействие Bcl-2 с двухслойно восстановленным очищенным VDAC, при этом Bcl-2 снижает проводимость канала.
Внутри митохондрий присутствуют апоптогенные факторы (цитохром c, Smac / гомолог Diablo, Оми), которые, если их высвободить, активируют исполнителей апоптоза, каспаз. В зависимости от их функции, после активации белки Bcl-2 либо способствуют высвобождению этих факторов, либо удерживают их в митохондриях. В то время как активированные проапоптотические Bak и / или Bax будут формировать MAC и опосредовать высвобождение цитохрома c, антиапоптотический Bcl-2 будет его блокировать, возможно, посредством ингибирования Bax и / или Bak. 7>
Белки семейства Bcl-2 также присутствуют в перинуклеарной оболочке и широко распространены во многих тканях организма. Их способность образовывать олигомерные поры в искусственных липидных бислоях документально подтверждена, но физиологическое значение порообразования неясно. Каждый из этих белков имеет отличительные свойства, в том числе некоторую степень ионной селективности.
Обобщенная транспортная реакция, предложенная для заключенных в мембрану олигомерных членов семейства Bcl-2:
Подмножество только BH3 семейства белков Bcl-2 содержит только один BH3-домен. Члены, содержащие только BH3, играют ключевую роль в развитии апоптоза. Члены семейства только для BH3 - это Bim, Bid, BAD и другие. Различные стимулы апоптоза вызывают экспрессию и / или активацию определенных членов семейства, содержащих только BH3, которые перемещаются в митохондрии и инициируют Bax / Bak-зависимый апоптоз.
Известно, что содержащиеся протеины эти домены включают позвоночных Bcl-2 (альфа- и бета-изоформы) и Bcl-x (изоформы Bcl-x (L).
На данный момент в этой статье используется контент из «1.A.21 Семейство Bcl-2 (Bcl-2)», который лицензирован таким образом, чтобы разрешить повторное использование в соответствии с Непортированная лицензия Creative Commons Attribution-ShareAlike 3.0, но не в соответствии с GFDL. Необходимо соблюдать все соответствующие условия.