| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC 1H-Phosphole | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChemSpider | |||
| PubChem CID | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | C4H5P | ||
| Молярная масса | 84,058 г · моль | ||
| Родственные соединения | |||
| Родственные соединения | Пиррол, бисмол, arsole, stibole | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Фосфол - это органическое соединение с химической формулой C4H4PH; это фосфорный аналог пиррола. Термин "фосфол" также относится к замещенным производным исходного гетероцикла. Эти соединения имеют теоретическое значение остальное, но также служат лигандами для переходных металлов и предшественниками более сложных фосфорорганических соединений.
В отличие от родственных 5-членных гетероциклов пиррол, тиофен и фуран, ароматичность фосфолов снижается, что отражает сопротивление фосфора делокализации своей неподеленной пары. Основным признаком этого различия является пирамидизация фосфора. На отсутствие ароматичности также указывает реакционная способность фосфол. Фосфолы подвергаются различным реакциям циклоприсоединения, координационные свойства фосфолов также хорошо изучены.
Исходный фосфол был впервые описан в 1983 году. Он был получен путем низкотемпературного протонирования фосфолида лития. Пентафенилфосфол был описан в 1953 году. Один путь к фосфолам - через реакцию МакКормака, включающую добавление 1,3- диена к фосфонному хлориду (RPCl 2) с последующим дегидрогалогенированием. Фенилфосфолы могут быть получены через цирконциклопентадиены реакцией с PhPCl 2.
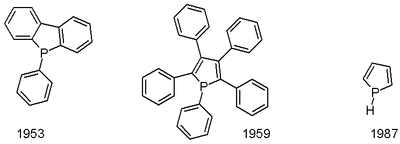
Поведение вторичных фосфолов, имеющих связь P-H, определяется реакционной способностью этой группы. Родительский фосфол легко перестраивается путем миграции H от P к углероду-2 с последующей димеризацией.
Большинство фосфолов являются третичными, обычно Р-метил или Р-фенил. Неароматичность этих фосфолов проявляется в их реакционной способности, но связи P-C остаются нетронутыми. Например, они претерпевают реакции Дильса-Альдера с электрофильными алкинами. Они являются основными в положении P, выступая в качестве лигандов.
2,5-дифенилфосфолы могут быть функционализированы путем депротонирования с последующим P-ацилированием, затем равновесие фосфолидов 1H, 2H, 3H, приводящее к сдвигу 1: 3 ацильная группа. Фосфолы также могут быть превращены в β-функциональные фосфабензолы (фосфинины или фосфорин ) посредством функционализации имидоилхлоридом и внедрения.