 | |
| Клинические данные | |
|---|---|
| Произношение | mi GAL a stat |
| Торговые наименования | Galafold |
| Другие названия | DDIG, AT1001, 1-дезоксигалактоноджиримицин |
| AHFS / Drugs.com | Монография |
| Данные лицензии | |
| Беременность. категория |
|
| Способы введения. | Внутрь (капсулы ) |
| Код АТС | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | 75% |
| Связывание с белками | Нет |
| Метаболиты | O-глюкурониды (<15%) |
| Период полувыведения | 3– 5 часов (разовая доза) |
| Экскреция | Моча (77%), кал (20%) |
| Идентификаторы | |
Название ИЮПАК
| |
| Номер CAS |
|
| PubChem CID | |
| Dr ugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL |
|
| Формула | C6H13NO4 |
| Молярная масса | 163,173 г · моль |
| 3D-модель (JSmol ) | |
SMILES
| |
InChI
| |
Мигаластат, продаваемый под торговой маркой Галафолд, представляет собой лекарство для лечения болезни Фабри, редкого генетического заболевания. Он был разработан Amicus Therapeutics. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) предоставило ему статус орфанного препарата в 2004 году, а Европейская комиссия последовала его примеру в 2006 году. Комитет Европейского агентства по лекарственным средствам для лекарственных препаратов для человека Использование (CHMP) предоставило лекарству разрешение на продажу под названием Galafold в мае 2016 года.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США считает его первым в мире препаратом. -класс лекарств.
Мигаластат используется для длительного лечения болезни Фабри у взрослых и подростков в возрасте 16 лет и старше с поддающейся изменению мутацией фермента альфа-галактозидаза A (α-GalA). «Поддающаяся» мутация - это мутация, которая приводит к неправильному свертыванию фермента, но в противном случае не приведет к значительному ухудшению его функции.
На основании теста in vitro, Amicus Therapeutics опубликовала список из 269 поддающихся лечению и почти 600 не поддающихся лечению мутаций. Примерно от 35 до 50% людей с Фабри имеют поддающуюся мутации.
Наиболее частым побочным эффектом в клинических исследованиях была головная боль (примерно в 10% случаев). люди берущие). Менее распространенные побочные эффекты (от 1 до 10% людей) включали неспецифические симптомы, такие как головокружение, усталость и тошноту, а также депрессию. Возможные редкие побочные эффекты не могли быть оценены из-за небольшого числа субъектов в клинических испытаниях, в которых были измерены побочные эффекты.
В сочетании с внутривенным агалсидаза альфа или бета, которые являются рекомбинантными версиями фермента α-GalA, мигаластат увеличивает тканевые концентрации функционального α-GalA по сравнению с агалсидазой, вводимой отдельно. Это ожидаемый и желаемый эффект.
Мигаластат не ингибирует и не индуцирует цитохром P450 ферменты печени или белки-переносчики и, следовательно, ожидается, что он имеет низкий потенциал взаимодействия с другими лекарствами.
Болезнь Фабри - это генетическое заболевание, вызванное различными мутациями фермента α-GalA, который отвечает за расщепление сфинголипида глоботриаозилцерамида (Gb3), среди других гликолипидов и гликопротеинов. Некоторые из этих мутаций приводят к неправильной укладке α-GalA, которая впоследствии не контролирует качество белка в эндоплазматическом ретикулуме и разлагается. Недостаток функциональной α-GalA приводит к накоплению Gb3 в кровеносных сосудах и других тканях с широким спектром симптомов, включая проблемы с почками, сердцем и кожей.
Мигаластат является мощным, доступным перорально ингибитором α-GalA (IC50 : 4 мкМ ). Связываясь с дефектной α-GalA, он сдвигает поведение сворачивания в сторону правильной конформации, что приводит к функциональному ферменту при условии, что мутация поддается изменению. Молекулы с этим типом механизма называются фармакологическими шаперонами.
. Когда фермент достигает своего пункта назначения, лизосома, мигаластат диссоциирует из-за низкого pH и относительного количества Gb3 и другие субстраты, оставляя α-GalA свободным для выполнения своей функции. В зависимости от мутации EC50 составляет от 0,8 мкМ до более 1 мМ в клеточных моделях.

Фермент альфа-галактозидаза A (α-GalA)
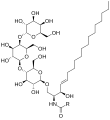
Глоботриаозилцерамид (Gb3), субстрат α-GalA, имеет концевую D-галактозу, структурно подобную мигаластату.
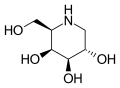
Мигаластат (вид «сверху»)
Мигаластат практически полностью всасывается из кишечника; прием препарата вместе с пищей снижает его абсорбцию примерно на 40%. Общая биодоступность составляет около 75% при приеме без еды. Вещество не связывается с белками плазмы крови .
Метаболизируется лишь небольшая часть дозы мигаластата, в основном до трех дегидрогенизированных O- глюкуронидов (4% доза) и ряд неуточненных метаболитов (10%). Препарат выводится в основном с мочой (77%) и в меньшей степени с фекалиями (20%). Практически все метаболиты выводятся с мочой. Период полувыведения составляет от трех до пяти часов после однократного приема.
 D-Галактоза, для сравнения
D-Галактоза, для сравнения Мигаластат используется в форме гидрохлорид, который представляет собой белое кристаллическое твердое вещество, растворимое в воде. Молекула имеет четыре асимметричных атома углерода с такой же стереохимией, что и сахар D-галактоза, но в ней отсутствует первая гидроксильная группа. Он имеет атом азота в кольце вместо кислорода, что делает его иминосахаром.
Структура формально происходит от ноджиримицина.
Мигаластат был выделен в виде продукт ферментации бактерии Streptomyces lydicus (штамм PA-5726) в 1988 году и названный 1-дезоксигалактоноджиримицин. В 2004 году FDA США присвоило ему статус орфанного препарата для лечения болезни Фабри, а в 2006 году Европейский CHMP сделал то же самое. Спонсорство препарата передавалось несколько раз в течение следующих лет: от Amicus Therapeutics к Shire Pharmaceuticals в 2008 году, обратно к Amicus в 2010 году, к Glaxo в 2011 году и снова к Amicus. в 2014 году.
В период с 2009 по 2015 год были проведены два клинических испытания фазы III с участием около 110 субъектов, в одном двойном слепом препарат сравнивался с плацебо, и одно сравнение его с рекомбинантной α-GalA без ослепления. Мигаластат стабилизировал сердце и функцию почек за 30-месячный период этих исследований.
В сентябре 2015 года Amicus объявил, что подаст новую заявку на лекарство (NDA) для ускоренного утверждения мигаластата в FDA до конца 2015 года. CHMP рекомендовал одобрение в апреле 2016 года, но FDA отклонило заявку в ноябре из-за недостаточности данных в ноябре 2016 года. Европейский Союз в мае 2016 года. Германия была первой страной, где был запущен мигаластат. После того, как Скотт Готлиб стал уполномоченным FDA в 2017 году, генеральный директор Amicus начал лоббировать его напрямую, чтобы FDA приняло NDA, и в феврале 2018 года FDA приняло его и пообещало ответ к августу 2018 года.