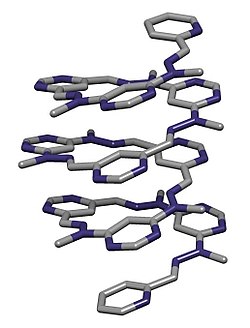
 Кристаллическая структура фолдамера, о которой сообщил Лен и его коллеги в Helv. Чим. Acta, 2003, 86, 1598–1624.
Кристаллическая структура фолдамера, о которой сообщил Лен и его коллеги в Helv. Чим. Acta, 2003, 86, 1598–1624.  Воспроизвести медиа Динамическое представление альфа-бета фолдамера
Воспроизвести медиа Динамическое представление альфа-бета фолдамера В химии фолдамер представляет собой дискретную цепочку молекула или олигомер, которая сворачивается в конформационно упорядоченное состояние в растворе. Это искусственные молекулы, которые имитируют способность белков, нуклеиновых кислот и полисахаридов складывать в четко определенные конформации, такие как спирали и β-листы. Структура фолдамера стабилизируется нековалентными взаимодействиями между несмежными мономерами. Фолдамеры изучаются с основной целью создания больших молекул с предсказуемой структурой. Изучение фолдамеров связано с темами самосборки молекул, молекулярного распознавания и химии хозяин-гость.

Фолдамеры могут различаться по размеру, но они определяются наличием нековалентных, несмежных взаимодействий. Это определение исключает такие молекулы, как поли (изоцианаты) (обычно известные как (полиуретан )) и поли (пролины), поскольку они надежно складываются в спирали из-за смежных ковалентных взаимодействий. Фолдамеры имеют реакция динамического сворачивания [развернутый → свернутый], в которой крупное макроскопическое сворачивание вызвано сольвофобными эффектами (гидрофобный коллапс), в то время как конечное энергетическое состояние свернутого фолдамера обусловлено нековалентными взаимодействиями. Эти взаимодействия работают совместно, чтобы сформировать наиболее стабильную третичную структуру, поскольку полностью свернутое и развернутое состояния более стабильны, чем любое частично сложенное состояние.
Структура фолдамера часто может можно спрогнозировать на основе его первичной последовательности. Этот процесс включает динамическое моделирование равновесия сворачивания на атомном уровне при различных условиях. Этот тип анализа может быть применен и к небольшим белкам, однако вычислительная технология не может моделировать все последовательности, кроме самых коротких.
Путь сворачивания фолдамера может быть определен путем измерения отклонения от экспериментально определенного благоприятная структура при различных термодинамических и кинетических условиях. Изменение структуры измеряют путем вычисления среднеквадратичного отклонения от атомарного положения основной цепи предпочтительной структуры. Структура фолдамера в различных условиях может быть определена расчетным путем, а затем подтверждена экспериментально. Изменения температуры, вязкости растворителя, давления, pH и концентрации соли могут дать ценную информацию о структуре фолдамера. Измерение кинетики складывания, а также равновесия складывания позволяет наблюдать влияние этих различных условий на структуру фолдамера.
Растворитель часто влияет на складывание. Например, путь сворачивания, включающий гидрофобный коллапс, будет сворачиваться по-другому в неполярном растворителе. Это различие связано с тем фактом, что разные растворители стабилизируют разные промежуточные продукты пути сворачивания, а также различные конечные структуры фолдамеров на основе межмолекулярных нековалентных взаимодействий.
Нековалентные межмолекулярные взаимодействия, хотя и небольшие по отдельности, их суммирование существенно изменяет химические реакции. Ниже перечислены общие межмолекулярные силы, которые химики использовали для создания фолдамеров.
Фолдамеры подразделяются на три разные категории: пептидомиметические фолдамеры, нуклеотидомиметические фолдамеры и абиотические фолдамеры. Пептидомиметические фолдамеры - это синтетические молекулы, имитирующие структуру белков, а нуклеотидомиметические фолдамеры основаны на взаимодействиях в нуклеиновых кислотах. Абиотические фолдамеры стабилизируются ароматическими взаимодействиями и взаимодействиями с переносом заряда, которые обычно не встречаются в природе. Три описанные ниже конструкции отклоняются от строгого определения фолдамера Муром, которое исключает спиральные фолдамеры.
Пептидомиметические фолдамеры часто нарушают ранее упомянутое определение фолдамеров, поскольку они часто принимают спиральные структуры. Они представляют собой важную веху в исследованиях фолдамеров. е их дизайну и возможностям. Самые большие группы пептидомиметиков состоят из β - пептидов, γ - пептидов и δ - пептидов, а также возможных мономерных комбинаций. аминокислоты этих пептидов различаются только одним (β), двумя (γ) или тремя (δ) атомами углерода в метилене, однако структурные изменения были значительными. Эти пептидные последовательности хорошо изучены, поскольку контроль последовательности приводит к надежному предсказанию сворачивания. Кроме того, с несколькими метиленовыми атомами углерода между карбоксильными и амино концами фланкирующих пептидных связей могут быть созданы боковые цепи различных R-групп. Один из примеров новизны β-пептидов можно увидеть в исследованиях Райзера и его коллег. Используя гетеролигопептид, состоящий из α-аминокислот и цис-β-аминоциклопропанкарбоновых кислот (цис-β-ACC), они обнаружили образование спиральных последовательностей в олигомерах длиной всего семь остатков и определенной конформации в пяти остатках; качество, уникальное для пептидов, содержащих циклические β-аминокислоты.
Нуклеотидомиметики обычно не квалифицируются как фолдамеры. Большинство из них предназначены для имитации отдельных оснований ДНК, нуклеозидов или нуклеотидов для неспецифического воздействия на ДНК. Они имеют несколько различных медицинских применений, включая противораковые, противовирусные и противогрибковые применения.
 Сворачивание и координация олигопиррола
Сворачивание и координация олигопиррола Абиотические фолдамеры снова представляют собой органические молекулы, предназначенные для динамического сворачивания. Они используют одно или несколько известных ключевых межмолекулярных взаимодействий, оптимизированных их конструкцией. Одним из примеров является то, что они организуются путем связывания анионов, таких как хлорид, посредством водородных связей (см. Рисунок). Сворачивание индуцируется в присутствии аниона: в противном случае конформационные ограничения полипиррольных групп незначительны.