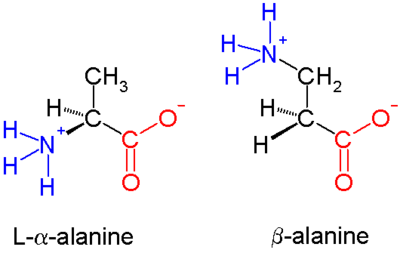
β-пептиды состоят из β-аминокислот, аминогруппа которых связана с β-углерод, а не α-углерод, как в 20 стандартных биологических аминокислотах. Единственная обычная встречающаяся в природе β-аминокислота - это β-аланин ; Хотя он используется в качестве компонента более крупных биологически активных молекул, β-пептиды в целом не встречаются в природе. По этой причине антибиотики на основе β-пептида исследуются как способы избежать устойчивости к антибиотикам. Ранние исследования в этой области были опубликованы в 1996 году группой Дитера Зеебаха и Сэмюэля Геллмана.
В α-аминокислотах (молекула слева) обе карбоновые кислоты группа (красная) и группа амино (синий) связаны с одним и тем же углеродным центром, называемым α углеродом (

Химический синтез β-аминокислот может быть сложной задачей, особенно с учетом разнообразия функциональных групп, связанных с β-углеродом, и необходимости поддержания хиральности. В показанной молекуле аланина β-углерод является ахиральным; однако большинство более крупных аминокислот имеют хиральный атом 
Существуют два основных типа β-пептидов: с органическим остатком (R), следующим к амину называются β-пептидами, а те, которые находятся рядом с карбонильной группой, называются β-пептидами.
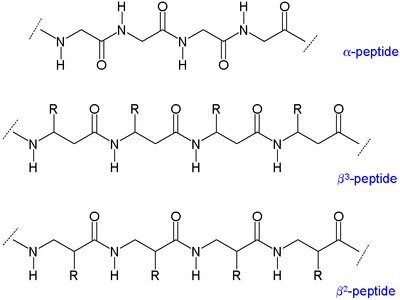
Поскольку скелеты β-пептидов длиннее, чем у пептидов., которые состоят из α-аминокислот, β-пептиды образуют различные вторичные структуры. алкил заместители в положениях α и β в β-аминокислоте благоприятствуют гош-конформации связи между α-углеродом и β-углеродом. Это также влияет на термодинамическую устойчивость конструкции.
Сообщалось о многих типах спиральных структур, состоящих из β-пептидов. Эти типы конформации различаются количеством атомов в кольце с водородными связями, которое образуется в растворе; Сообщалось о 8-спиралях, 10-спиралях, 12-спиралях, 14-спиралях и 10/12 спиралях. Вообще говоря, β-пептиды образуют более стабильную спираль, чем α-пептиды.
β-пептиды устойчивы к протеолитической деградации in vitro и in vivo, что является важным преимуществом перед природными пептидами при получении лекарственных препаратов на основе пептидов. β-Пептиды использовались для имитации природных пептидных антибиотиков, таких как магаинины, которые являются очень сильнодействующими, но их трудно использовать в качестве лекарств, поскольку они расщепляются протеолитическими ферментами в организме.
Существует 8 бета-форм: аланин, лейцин, лизин, аргинин, глутамат, глутамин, фенилаланин, формы тирозина. Аспарагиновая кислота рассматривается как бета- и альфа-формы, хотя бета-форма содержится в микроцистинах.