 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 2,5- Диметилфуран | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.009.923 |
| Номер EC |
|
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C6H8O |
| Молярная масса | 96,13 |
| Внешний вид | Жидкость |
| Плотность | 0,8897 г / см |
| Точка плавления | -62 ° C (-80 ° F; 211 K) |
| Точка кипения | 92-94 ° C (198-201 ° F; от 365 до 367 K) |
| Растворимость в воде | Нерастворимый |
| Магнитная восприимчивость (χ) | -66 0,37 · 10 см / моль |
| Показатель преломления (nD) | 1,44 - 1,442 |
| Опасности | |
| Основные опасности | Очень легковоспламеняющиеся, вредные |
| Температура вспышки | −1 ° C ( 30 ° F; 272 K) |
| Температура самовоспламенения. | 285,85 ° C (546,53 ° F; 559,00 K) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
2,5-диметилфуран является гетероциклическим соединение с формулой (CH 3)2C4H2O. Хотя его часто называют сокращенно DMF, его не следует путать с диметилформамидом. Производное фуран, это простое соединение является потенциальным биотопливом, получаемым из целлюлозы.
Фруктоза может быть преобразована в 2,5-диметилфуран в каталитической биомассе- в жидкость процесс. Превращение фруктозы в ДМФА происходит через гидроксиметилфурфурол.
Фруктозу получают из глюкозы, строительного блока целлюлозы.
ДМФ имеет ряд преимуществ в качестве биотоплива. Его удельная энергия на 40% выше, чем у этанола, что делает его сопоставимым с бензином (бензин). Он также химически стабилен и, поскольку нерастворим в воде, не впитывает влагу из атмосферы. Испарение диметилфурана в процессе производства также требует примерно на треть меньше энергии, чем испарение этанола, хотя его точка кипения примерно на 14 ° C выше при 92 ° C по сравнению с 78 ° C для этанола.
Способность эффективно и быстро производить диметилфуран из фруктозы, содержащейся в фруктах и некоторых корнеплодах, или из глюкозы, которая может быть получена из крахмала и целлюлоза - все они широко доступны в природе - усиливают привлекательность диметилфурана, хотя необходимо изучить вопросы безопасности. Биоэтанол и биодизель в настоящее время являются ведущими видами жидкого биотоплива.
стехиометрическое соотношение воздух / топливо диметилфурана составляет 10,72 по сравнению с этанолом при 8,95 и бензином 14,56. Это означает, что для сжигания диметилфурана требуется примерно на 33% меньше воздуха, чем для того же количества бензина, но примерно на 20% больше воздуха, чем для такого же количества этанола.
теплотворная способность жидкого диметилфурана составляет 33,7 МДж / кг по сравнению с 26,9 МДж / кг для этанола и 43,2 МДж / кг для бензина. октановое число (RON) по исследованиям диметилфурана составляет 119. скрытая теплота испарения при 20 ° C составляет 31,91 кДж / моль. Недавние испытания одноцилиндрового бензинового двигателя показали, что термический КПД при сжигании диметилфурана аналогичен таковому у бензина.
2,5-диметилфуран служит в качестве поглотителя для синглетного кислорода, свойство, которое использовалось для определения синглетного кислорода в природных водах. Механизм включает реакцию Дильса-Альдера с последующим гидролизом, что в конечном итоге приводит к перекиси водорода в виде продуктов. Совсем недавно для той же цели был использован фурфуриловый спирт. 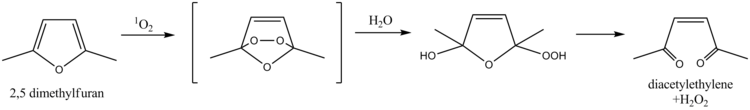
2,5-диметилфуран также был предложен в качестве внутреннего стандарта для ЯМР-спектроскопии. 2,5-Диметилфуран имеет синглеты в спектре ЯМР 1Н при δ 2,2 и 5,8; синглеты обеспечивают надежную интеграцию, в то время как положения пиков не мешают многим аналитам. Соединение также имеет подходящую температуру кипения 92 ° C, что предотвращает потери при испарении, но легко удаляется.
2,5-диметилфуран образуется при термическом разложении некоторых сахаров и был идентифицирован в следовых количествах как компонент карамелизированных сахаров.
2,5-диметилфуран играет роль в механизме нейротоксичности гексана в организме человека. Вместе с гексан-2,5-дионом и 4,5-дигидрокси-2-гексаноном он является одним из основных метаболитов гексана.
2,5 -Диметилфуран был идентифицирован как один из компонентов сигарного дыма с низкой цилиарной токсичностью (способность отрицательно влиять на реснички в дыхательных путях, которые отвечают за удаление посторонних частиц). Его концентрация в крови может использоваться в качестве биомаркера для курения.
Сравнение паспортов безопасности показывает, что обращение с 2,5-диметилфураном человеком примерно так же опасно, как обращение с бензином.