| Редукция Вольфа-Кишнера | |
|---|---|
| Назван в честь | Людвиг Вольф. Николай Кишнер |
| Тип реакции | Органическая окислительно-восстановительная реакция |
| Идентификаторы | |
| Портал органической химии | редукция Вольфа-Кишнера |
| RSC ID онтологии | RXNO: 0000226 |
Редукция Вольфа – Кишнера представляет собой реакцию, используемую в органической химии для преобразования карбонильных функциональных групп в метиленовые группы. В контексте синтеза сложных молекул его наиболее часто используют для удаления карбонильной группы после того, как она выполнила свою синтетическую цель активации промежуточного соединения на предыдущей стадии. Таким образом, для этой реакции нет очевидного ретрона. Первоначально описанный Николаем Кишнером в 1911 году и Людвигом Вольфом в 1912 году, он был применен для полного синтеза скопадульциевой кислоты B, аспидоспермидина и дизидиолида.

В общем, реакция Механизм сначала включает образование in situ гидразона путем конденсации гидразина с кетоном или альдегидным субстратом. Однако иногда выгодно использовать предварительно образованный гидразон в качестве субстрата (см. модификации ). Стадия, определяющая скорость реакции, представляет собой депротонирование гидразона алкоксидным основанием с образованием диимид-аниона посредством согласованной стадии протонирования / депротонирования, опосредованной растворителем. Коллапс этого алкилдиимида с потерей N 2 приводит к образованию алкиланиона, который может быть протонирован растворителем с получением желаемого продукта.

Поскольку восстановление Вольфа – Кишнера требует очень основных условий, оно не подходит для оснований, чувствительных к основанию. В некоторых случаях образование необходимого гидразона не будет происходить в пространственно затрудненных карбонильных группах, что препятствует реакции. Однако этот метод может превосходить родственное восстановление Клемменсена для соединений, содержащих чувствительные к кислоте функциональные группы, такие как пирролы, и для высокомолекулярных соединений.
The Wolff - Восстановление Кишнера было независимо открыто Н. Кишнером в 1911 году и Людвигом Вольфом в 1912 году. Кишнер обнаружил, что добавление предварительно образованного гидразона к горячему гидроксиду калия, содержащему измельченную платинированную пористую пластину, приводит к образование соответствующего углеводорода. Обзор под названием «Инвалидность, деспотизм, дезоксигенация - от изгнания к академику: Николай Матвеевич Кижнер», описывающий жизнь и деятельность Кишнера, был опубликован в 2013 году.

Позже Вольф достиг того же результата, нагревая этанольный раствор семикарбазоны или гидразоны в запаянной пробирке до 180 ° C в присутствии этилата натрия.
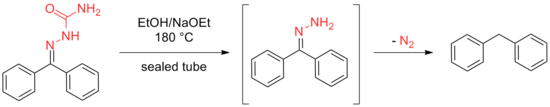
Преимущество метода, разработанного Кишнером, состоит в том, что он не требует наличия герметичной трубки, но обе методологии страдали ненадежностью при применении ко многим затрудненным субстратам. Эти недостатки способствовали развитию процедуры Вольфа, в которой использовались высококипящие растворители, такие как этиленгликоль и триэтиленгликоль, чтобы обеспечить высокие температуры, необходимые для реакции, при этом избегая необходимость герметичной трубки. За этими первоначальными модификациями последовало множество других улучшений, описанных ниже.
Механизм редукции Вольфа – Кишнера был изучен Шмантом и соавторами. Согласно исследованию Шманта, первой стадией этой реакции является образование гидразон-аниона 1 путем депротонирования концевого азота под действием МОН. Если семикарбазоны используются в качестве субстратов, за первоначальным превращением в соответствующий гидразон следует депротонирование. Ряд механистических данных предполагает, что этап , определяющий скорость, включает образование новой углерод-водородной связи на углеродном конце в делокализованном гидразоновом анионе. Этот захват протона происходит согласованным образом с отводом второго протона на азотном конце, вызванного растворителем. Открытие Шманта, что эта реакция является первым порядком как по гидроксид-иону, так и по кетон-гидразону, поддерживает это механистическое предположение. В этом процессе должны быть задействованы несколько молекул растворителя, чтобы обеспечить согласованный процесс. Подробный анализ Хаммета арилальдегидов, метиларилкетонов и диарилкетонов показал нелинейную зависимость, которую авторы связывают со сложностью этапа определения скорости. Слегка электроноакцепторные заместители способствуют образованию углерод-водородной связи, но сильно электроноакцепторные заместители уменьшают отрицательный заряд у концевого азота и, в свою очередь, способствуют более крупной и твердой сольватной оболочке, которая затрудняет разрыв связи N-H. Наблюдаемая исключительно высокая отрицательная энтропия значений активации может быть объяснена высокой степенью организации в предлагаемом переходном состоянии.
Кроме того, было обнаружено, что скорость реакции зависит от концентрации гидроксильного растворителя и от катиона в алкоксидном катализаторе. Присутствие краун-эфира в реакционной среде может повысить реакционную способность гидразонового аниона 1 за счет диссоциации ионной пары и, следовательно, повысить скорость реакции. Конечной стадией восстановления Вольфа-Кишнера является коллапс диимид-аниона 2 в присутствии источника протонов с образованием углеводорода за счет потери диазота с образованием алкиланиона 3, который претерпевает быструю и необратимую кислотно-щелочную реакцию с растворителем с образованием алкана. Доказательства этого высокоэнергетического промежуточного продукта были получены Табером с помощью внутримолекулярного захвата. Стереохимический результат этого эксперимента больше соответствовал промежуточному алкил-аниону, чем альтернативной возможности алкильного радикала. Общая движущая сила реакции - выделение газообразного азота из реакционной смеси.

Многие усилия, направленные на улучшение восстановления Вольфа-Кишнера, были сосредоточены на более эффективном образовании промежуточного гидразона за счет удаления воды и более высокой скорости разложения гидразона за счет повышения температуры реакции. Некоторые из новых модификаций обеспечивают более значительные преимущества и позволяют проводить реакции в значительно более мягких условиях. В таблице представлена сводка некоторых модификаций, которые были разработаны с момента первоначального открытия.
| Исходная процедура | Хуанг Минлон | Бартон | Крам | Хенбест | Калиоти | Майерс | |
|---|---|---|---|---|---|---|---|
| Реагенты | карбонильное соединение, 100% H 2 NNH 2, Na или NaOEt | карбонильное соединение, 85% H 2 NNH 2, KOH | карбонильное соединение, безводный H 2 NNH 2, предварительно образованный гидразон Na | , KOtBu | предварительно образованный гидразон, KOtBu | тозилгидразон, гидрид-донор | карбонильное соединение, 1,2-бис (трет-бутилдиметилсилил) гидразин, Sc (OTf) 3, KOtBu |
| Растворитель | высококипящий растворитель, например этиленгликоль | высококипящий растворитель, например этиленгликоль | высококипящий растворитель, например диэтиленгликоль | анх. ДМСО | толуол | ТГФ | ДМСО |
| Температура | 200 ° C | 180–200 ° C (после удаления вода и избыток гидразина) | 210 ° C | 25 ° C | 111 ° C | 66 ° C | 25 ° C |
| Преимущества | одностадийная процедура | сокращение времени реакции, может быть достигнута более высокая температура, нет необходимости использовать anh. гидразин | позволяет декарбонилирование стерически затрудненных субстратов | протекает при комнатной температуре | нет необходимости в медленном добавлении гидразона | мягкие условия реакции, возможно с различными восстановители | очень мягкие условия реакции |
| Недостатки | длительное время реакции (50–100 ч) | необходима дистилляция | жесткие условия реакции | необходимо выделение гидразона и медленное добавление | необходимо выделение гидразона | необходимо выделение тозилгидразона. донор гидрида может действовать как основание | синтез 1,2-бис (трет-бутилдиметилсилил) гидразин необходим |
| Толерантность функциональной группы | не переносит сложные эфиры, амиды, галогены, циано-, и нитрогруппы | , аналогичные исходной процедуре | , аналогичной исходной методике | , допускают амиды | более высокую толерантность к α-заместителям, которые будут подвергаться элиминированию и α, β-ненасыщенные еноны, которые будут подвергаться миграции в исходных условиях | , допускают сложные эфиры, амиды, циано-, нитро- и хлорзаместители с NaBH 3 CN в качестве источника гидридов, не допускают первичные бром- и йод-заместители | не сообщается |
В 1946 г. Хуанг Минлон сообщил о модифицированной методике восстановления кетонов по Вольфу – Кишнера в котором избыток гидразина и воды удаляли отгонкой после образования гидразона. Эффект понижения температуры воды, который образовывался при образовании гидразона, обычно приводил к длительному времени реакции и суровым условиям реакции, даже если при образовании гидразона использовался безводный гидразин. Модифицированная процедура состоит из кипячения карбонильного соединения в 85% гидразингидрате с тремя эквивалентами гидроксида натрия с последующей отгонкой воды и избытка гидразина и повышением температуры до 200 ° C. С помощью этой модификации можно значительно сократить время реакции и повысить выход. В первоначальном отчете Хуан Минлон описывается восстановление β- (п-феноксибензоил) пропионовой кислоты до γ- (п-феноксифенил) масляной кислоты с выходом 95% по сравнению с выходом 48%, полученным с помощью традиционной процедуры.

Через девять лет после первой модификации Хуан Минлона Бартон разработал метод восстановления стерически затрудненных карбонильных групп. Этот метод отличается строгим исключением воды, более высоких температур и более продолжительного времени реакции, а также натрия в диэтиленгликоле вместо алкоксидного основания. В этих условиях можно облегчить некоторые проблемы, которые обычно возникают с затрудненными кетонами - например, C 11 -карбонильная группа в стероидном соединении, показанном ниже, была успешно восстановлена в условиях Бартона, в то время как условия Хуанга-Минлона не удалось произвести это преобразование.

Медленное добавление предварительно образованных гидразонов к трет-бутоксиду калия в ДМСО в качестве реакционной среды вместо гликолей позволяет успешно проводить образование углеводородов при таких низких температурах, как 23 ° C. Крам объяснил более высокую реакционную способность ДМСО как растворителя более высокой щелочностью трет-бутоксида калия в этой среде.

Эта модификация не использовалась в значительной степени в органическом синтезе из-за необходимости изолировать предварительно сформированные гидразоновые субстраты и добавлять гидразон в реакционную смесь в течение нескольких часов.
Хенбест расширил методику Крама путем кипячения с обратным холодильником карбонилгидразонов и трет-бутоксида калия в сухом толуоле. Медленное добавление гидразона не является необходимым, и было обнаружено, что эта процедура лучше подходит для карбонильных соединений, склонных к побочным реакциям, вызываемым основанием, чем модификация Крама. Например, было обнаружено, что миграция двойной связи в α, β-ненасыщенных енонах и отщепление функциональных групп некоторых α-замещенных кетонов с меньшей вероятностью происходит в условиях Хенбеста.
Обработка тозилгидразонов реагентами-донорами гидрида для получения соответствующих алканов известна как реакция Калиоти. Изначально заявленные условия реакции были изменены, и доноры гидридов, такие как цианоборгидрид натрия, триацетоксиборгидрид натрия или катехолборан, могут восстанавливать тозилгидразоны до углеводородов. Реакция протекает в относительно мягких условиях и, следовательно, может допускать более широкий набор функциональных групп, чем исходная процедура. Восстановление с цианоборгидридом натрия в качестве восстановителя можно проводить в присутствии сложных эфиров, амидов, циано-, нитро- и хлорзаместителей. В этих условиях первичные бром- и йод-заместители замещаются нуклеофильным гидридом.

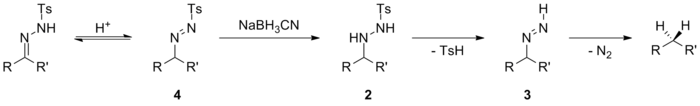
В нескольких работах был изучен механизм этого восстановления, и возможны множественные пути реакции, в зависимости от pH реакции, используемого восстанавливающего агента и электронных свойств субстрата. Одна возможность, имеющая место в кислых условиях, включает прямую гидридную атаку иона иминия 1 после предварительного протонирования тозилгидразона. Полученное производное тозилгидразина 2 впоследствии подвергается элиминированию п-толуолсульфиновой кислоты и разлагается через диимин промежуточное соединение 3 до соответствующего углеводорода.

Небольшое изменение этот механизм возникает, когда таутомеризация до азогидразона облегчается индуктивными эффектами. Переходный азогидразин 4 затем может быть восстановлен до производного тозилгидразина 2 и дать декарбонилированный продукт аналогично первой возможности. Этот механизм работает, когда используются относительно слабые доноры гидрида, такие как цианоборгидрид натрия. Известно, что этот цианоборгидрид натрия недостаточно силен для восстановления иминов, но может восстанавливать ионы иминия.
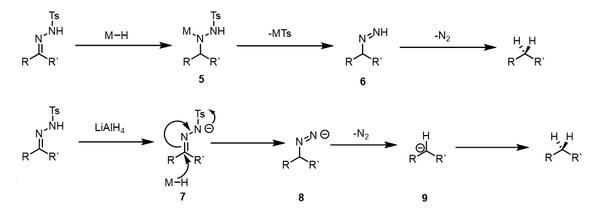
Когда используются более сильные доноры гидридов, действует другой механизм, который позволяет избежать использования кислых условий. Доставка гидрида происходит с получением промежуточного соединения 5, с последующим удалением металлического сульфината с получением промежуточного азопродукта 6 . Затем этот промежуточный продукт разлагается с потерей газообразного азота с образованием восстановленного соединения. Когда используются сильноосновные доноры гидрида, такие как алюмогидрид лития, то перед доставкой гидрида может происходить депротонирование тозилгидразона. Промежуточный анион 7 может подвергаться гидридной атаке, удаляя сульфинат металла с образованием азоаниона 8 . Он легко разлагается до карбаниона 9, который протонируется с образованием восстановленного продукта.
Как и в случае исходного восстановления Вольфа-Кишнера, реакция декарбонилирования часто может быть неудачной из-за безуспешного образования соответствующего тозилгидразона. Это типично для стерически затрудненных кетонов, как это было в случае циклического аминокетона, показанного ниже.

Если образование гидразона не удается получить, можно использовать альтернативные методы восстановления, включая восстановление тиокета с помощью Никель Ренея или реакция с триэтилборгидридом натрия.
α, β-ненасыщенных карбонилтозилгидразонов может быть преобразована в соответствующие алкены с миграцией двойного облигация. Восстановление происходит стереоселективно с получением геометрического изомера E.

Очень мягкий метод был разработан Kabalka et al. которые использовали один эквивалент катехолборана для восстановления α, β-ненасыщенных тозилгидразонов.

Djerassi et al. изучили механизм восстановления NaBH 3 CN α, β-ненасыщенных тозилгидразонов. Основываясь на экспериментах по мечению дейтерием, они пришли к выводу, что образование алкена инициируется восстановлением гидрида иона иминия с последующей миграцией двойной связи и экструзией азота, которые происходят согласованным образом. Перегруппировка аллильного диазена в качестве конечной стадии восстановительной 1,3-транспозиции α, β-ненасыщенных тозилгидразонов в восстановленные алкены также может быть использована для создания sp-стереоцентров из аллильных диазенов, содержащих прохиральные стереоцентры. Влияние алкоксистереоцентра приводит к диастереоселективному восстановлению α, β-ненасыщенного тозилгидразона. Авторы предсказали, что диастереоселективный перенос диазенового водорода на одну сторону прохирального алкена может быть усилен во время супрафациальной перегруппировки.

В 2004 году Майерс и соавторы разработали метод получения N-трет-бутилдиметилсилилгидразонов из карбонилсодержащих соединений. Эти продукты могут использоваться как превосходная альтернатива гидразонам при превращении кетонов в алканы. Преимуществами этой процедуры являются значительно более мягкие условия реакции и более высокая эффективность, а также удобство эксплуатации. Конденсация 1,2-бис (трет-бутилдиметилсилил) гидразина с альдегидами и кетонами с Sc (OTf) 3 в качестве катализатора происходит быстро и эффективно при температуре окружающей среды. Образование и восстановление N-трет-бутилдиметилсилилгидразонов можно проводить в одном реакторе с высоким выходом.

Недавно разработанный метод сравнивали непосредственно со стандартными условиями восстановления Хуанга – Минлона Вольфа – Кишнера (гидразингидрат, гидроксид калия, диэтиленгликоль, 195 ° C) для стероидного кетона, показанного выше. Продукт был получен с выходом 79% по сравнению с 91%, полученным при восстановлении через промежуточный N-трет-бутилдиметилсилилгидразон.
Восстановление Вольфа – Кишнера не подходит для оснований, чувствительных к основанию, и при определенных условиях ему может препятствовать стерическое препятствие, окружающее карбонильную группу. Некоторые из наиболее распространенных побочных реакций перечислены ниже.
Обычно встречающаяся побочная реакция при восстановлении Вольфа-Кишнера включает образование азина в результате реакции гидразона с карбонильным соединением. Образование кетона можно подавить, энергично исключив воду во время реакции. Некоторые из представленных процедур требуют выделения соединения гидразона перед восстановлением. Это может быть осложнено дальнейшим превращением гидразона продукта в соответствующий гидразин во время очистки продукта. Крам обнаружил, что образованию азина способствует быстрое добавление предварительно образованных гидразонов к трет-бутоксиду калия в безводном диметилсульфоксиде.

Вторая основная побочная реакция - восстановление кетона или альдегид к соответствующему спирту. После начального гидролиза гидразона свободное карбонильное производное восстанавливается алкоксидом до карбинола. В 1924 году Эйзенлор сообщил, что значительные количества гидроксидекалина наблюдались во время попытки восстановления транс-β-декалона по Вольфу-Кишнеру. Как правило, образование спирта можно подавить путем исключения воды или добавления избытка гидразина.
Во время своих первоначальных исследований Кишнер отметил, что в некоторых случаях α-замещение карбонильной группы может привести к элиминированию с образованием ненасыщенных углеводородов в типичных условиях реакции. Позже Леонард развил эту реакцию и исследовал влияние различных α-заместителей на результат реакции. Он обнаружил, что степень элиминации увеличивается с увеличением стерической массы уходящей группы. Кроме того, α-диалкиламино-замещенные кетоны обычно давали смесь продуктов восстановления и элиминирования, тогда как менее основные уходящие группы приводили к исключительному образованию алкенового продукта.

Фрагментация α, β-эпоксикетонов до аллильных спиртов была расширена до синтетически полезного процесса и известна как реакция Уортона.
Перегруппировка Гроба напряженных колец, смежных с карбонильной группой, наблюдалась Эрманом и соавторами. Во время попытки восстановления транс-π-бромкамфора по Вольфу-Кишнера в условиях Крама лимонен был выделен как единственный продукт.
Подобным образом может происходить расщепление напряженных колец, прилегающих к карбонильной группе. Когда 9β, 19-цикло-5α-прегнан-3,11,20-трион, 3,20-диэтиленкеталь подвергали условиям Хуанга-Минлона, вместо образования 11-дезоксосоединения наблюдалось расширение кольца.

Восстановление Вольфа – Кишнера - эффективный инструмент в органическом синтезе. Например, Ishibashi и его коллеги использовали модификацию Huang Minlon восстановления Вольфа-Кишнера в качестве одного из заключительных шагов в своем синтезе (±) -аспидоспермидина. Дистиллируемый материал удаляли после образования гидразона при 160 ° C, а затем нагревали до 210 ° C в течение ночи. Карбонильная группа, которая была восстановлена при восстановлении Вольфа-Кишнера, была важна для предыдущих стадий синтеза. Третичный амид был стабилен в условиях реакции и впоследствии был восстановлен литийалюмогидридом.
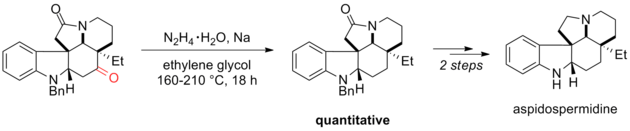
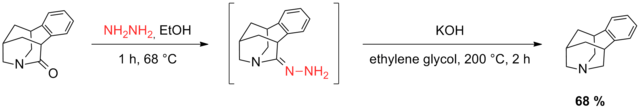
Амиды обычно не являются подходящими субстратами для восстановления Вольфа-Кишнера, как показано в приведенном выше примере. Коу с соавторами, однако, обнаружили, что скрученный амид может быть эффективно восстановлен в условиях Вольфа-Кишнера. Авторы объясняют это наблюдение стереоэлектронным смещением субстрата, которое предотвращает образование ионов «анти-Bredt » иминиевый и, следовательно, способствует выбросу спирта и образованию гидразона. Функциональность амида в этом напряженном субстрате можно рассматривать как изолированные функциональные группы амина и кетона, поскольку резонансная стабилизация предотвращается из-за торсионных ограничений. Продукт был получен с общим выходом 68% по двухстадийной методике.
В 2011 году Петтус и Грин восстановили трициклическое карбонильное соединение, используя модификацию восстановления Вольфа – Кишнера Хуанг Минлон. Несколько попыток декарбонилирования трициклического аллилового ацетата, содержащего кетон, не увенчались успехом, и пришлось удалить ацетатную функциональность, чтобы обеспечить успешное восстановление Вольфа-Кишнера. Наконец, аллиловый спирт был установлен с помощью кислородной канализации.

Восстановление Вольфа-Кишнера также использовалось в килограммах для синтеза функционализированного имидазольного субстрата. Было исследовано несколько альтернативных методов восстановления, но все испытанные условия остались безуспешными. Проблемы безопасности при крупномасштабном восстановлении по методу Вольфа – Кишнера были учтены, и высокооптимизированная процедура позволила получить продукт с хорошим выходом.

McIntosh et al. использовали перегруппировку аллильного диазена в своем синтезе С 245-фрагмента антаскомицина В. Гидразон селективно восстанавливали катехолбораном, а избыток восстанавливающего агента разлагался тиосульфатом натрия. Затем неочищенный продукт реакции обрабатывали ацетатом натрия и нагревали с обратным холодильником в хлороформе с получением 1,4-син-изомера.
