 18-crown-6 согласование Ион калия
18-crown-6 согласование Ион калия Краун-эфиры представляют собой циклические химические соединения, которые состоят из кольца, содержащего несколько эфирных групп. Наиболее распространенными краун-эфирами являются циклические олигомеры этиленоксида, повторяющееся звено - этиленокси, то есть –CH 2CH2O–. Важными членами этой серии являются тетрамер (n = 4), пентамер (n = 5) и гексамер (n = 6). Термин «корона» относится к сходству между структурой краун-эфира, связанного с катионом, и короной, сидящей на голове человека. Первое число в названии краун-эфира относится к числу атомов в цикле, а второе число относится к числу тех атомов, которые являются кислородом. Краун-эфиры намного шире, чем олигомеры этиленоксида; важная группа происходит из катехолов.
. Краун-эфиры прочно связывают определенные катионы, образуя комплексы. Атомы кислорода хорошо расположены для координации с катионом, расположенным внутри кольца, тогда как внешняя часть кольца гидрофобна. Образующиеся катионы часто образуют соли, растворимые в неполярных растворителях, и по этой причине краун-эфиры полезны в катализе фазового переноса. Дентальность полиэфира влияет на сродство краун-эфира к различным катионам. Например, 18-краун-6 имеет высокое сродство к катиону калия, 15-краун-5 - к катиону натрия и 12-краун-4 - к катиону лития. Высокое сродство 18-краун-6 к ионам калия способствует его токсичности. Самым маленьким краун-эфиром, все еще способным связывать катионы, является 8-краун-4, а самым большим, экспериментально подтвержденным краун-эфиром является 81-краун-27. Краун-эфиры - не единственные макроциклические лиганды, которые обладают сродством к катиону калия. Ионофоры, такие как валиномицин, также демонстрируют заметное предпочтение катиона калия по сравнению с другими катионами.
Краун-эфиры взаимодействуют с кислотами Льюиса посредством электростатических, σ-дырочных (см. связь галогена ) взаимодействий между основными атомами кислорода Льюиса в крауне. эфир и электрофильный кислотный центр Льюиса.
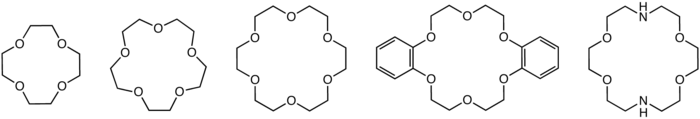 Структуры обычных краун-эфиров: 12-краун-4, 15-краун-5, 18-краун-6, дибензо-18-краун-6 и
Структуры обычных краун-эфиров: 12-краун-4, 15-краун-5, 18-краун-6, дибензо-18-краун-6 иВ 1967 году Чарльз Педерсен, который был химиком, работающим в DuPont, открыл простой метод синтеза краун-эфир, когда он пытался приготовить комплексообразователь для. Его стратегия заключалась в связывании двух катехолатных групп через один гидроксил на каждой молекуле. Это связывание определяет полидентатный лиганд, который может частично охватывать катион и путем ионизации фенольных гидроксилов нейтрализовать связанный дикатион. Он был удивлен, выделив побочный продукт, который образовывал сильно комплексные катионы калия. Ссылаясь на более раннюю работу по растворению калия в 16-краун-4, он понял, что циклические простые полиэфиры представляют новый класс комплексообразователей, способных связывать щелочной металл. катионы. Он приступил к сообщению о систематических исследованиях синтеза и связывающих свойств краун-эфиров в основополагающей серии статей. Открытие краун-эфиров принесло пользу в областях органического синтеза, катализаторов межфазного переноса и других новых дисциплин. Педерсен особенно популяризировал дибензокраунэфиры.
 Катенан, полученный из циклобис (паракват-п-фенилен) (циклофан с двумя виологенными звеньями) и циклического полиэфира (бис (пара-фенилен-34-краун-10)). Атомы углерода двух компонентов ротаксана окрашены в зеленый и фиолетовый цвета. В противном случае O = красный, N = синий. Атомы H опущены. Вторая из Нобелевских премий по химии с участием краун-эфиров была присуждена за разработку и синтез молекулярных машин. Многие из этих "машин" включают краун-эфиры в качестве основных компонентов конструкции.
Катенан, полученный из циклобис (паракват-п-фенилен) (циклофан с двумя виологенными звеньями) и циклического полиэфира (бис (пара-фенилен-34-краун-10)). Атомы углерода двух компонентов ротаксана окрашены в зеленый и фиолетовый цвета. В противном случае O = красный, N = синий. Атомы H опущены. Вторая из Нобелевских премий по химии с участием краун-эфиров была присуждена за разработку и синтез молекулярных машин. Многие из этих "машин" включают краун-эфиры в качестве основных компонентов конструкции. Педерсен получил Нобелевскую премию по химии 1987 за открытие синтетических путей и связывающих свойств краун-эфиров.
Благодаря хелатному эффекту и макроциклическому эффекту краун-эфиры проявляют более сильное сродство к различным катионам, чем их разделенные или ациклические аналоги. Таким образом, селективность катионов для ионов щелочных металлов в основном зависит от размера и плотности заряда иона, а также размера полости краун-эфира.
| Краун-эфир | Размер полости / Å | Предпочтительный ион щелочного металла | Эффективный ионный радиус / Å |
|---|---|---|---|
| 12-краун-4 | 0,6-0,75 | Li | 0,76 |
| 15-крон-5 | 0,86-0,92 | Na | 1,02 |
| 18-крон-6 | 1,34-1,55 | K | 1,38 |
| 21-крон-7 | 1,7-2,1 | Cs | 1,67 |
Сродство данного краун-эфира к катионам лития, натрия и калия может меняться на несколько величин, что объясняется большой разницей в их плотности заряда. Между катионами калия, рубидия и цезия изменения в сродстве менее заметны, поскольку их плотность заряда меняется меньше, чем у щелочных металлов в более ранние периоды.
Помимо высокого сродства к калию катионы, 18-краун-6 могут также связываться с протонированными аминами и образовывать очень стабильные комплексы как в растворе, так и в газовой фазе. Некоторые аминокислоты, такие как лизин, содержат первичный амин на своих боковых цепях. Эти протонированные аминогруппы могут связываться с полостью 18-краун-6 и образовывать стабильные комплексы в газовой фазе. Водородные связи образуются между тремя атомами водорода протонированных аминов и тремя атомами кислорода 18-краун-6. Эти водородные связи делают комплекс стабильным аддуктом. Благодаря включению люминесцентных заместителей в их основную цепь эти соединения оказались чувствительными ионными зондами, поскольку изменения в поглощении или флуоресценции фотоактивных групп могут быть измерены для очень низких концентраций присутствующего металла. Некоторые привлекательные примеры включают макроциклы, содержащие доноры кислорода и / или азота, которые присоединены к полиароматическим соединениям, таким как антрацены (через положения 9 и / или 10) или нафталины (через положения 2 и 3). Некоторые модификации ионофоров красителей краун-эфирами демонстрируют коэффициенты экстинкции, которые зависят от длины цепочки связанных катионов.
| На Викискладе есть материалы, связанные с эфирами короны. |