 | |||
| |||
| Имена | |||
|---|---|---|---|
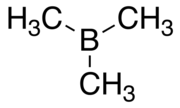
| Предпочтительное название ИЮПАК Триметилборан | |||
| Другие названия Триметилбор. Триметилбор | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.008.926 | ||
| Номер EC |
| ||
| PubChem CID | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | C3H9B | ||
| Молярная масса | 55,92 г / моль | ||
| Внешний вид | Бесцветный газ или жидкость | ||
| Плотность | 0,625 г / см при -100 ° C | ||
| Температура плавления | -161,5 ° C (-258,7 ° F; 111,6 K) | ||
| Температура кипения | -20,2 ° C (-4,4 ° F; 253,0 K) | ||
| Растворимость в воде | Небольшая, высокореакционная | ||
| Структура | |||
| Молекулярная форма | Δ | ||
| Опасности | |||
| Основные опасности | Спонтанно воспламеняется в воздухе; вызывает ожоги | ||
| пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасно | ||
| Указания на опасность GHS | H220, H250, H280, H314 | ||
| Меры предосторожности GHS | P210, P222, P260, P264, P280, P301 + 330 + 331, P302 + 334, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P321, P363, P370 + 378, P377, P381, P403, P405, P410 + 403, P422, P501 | ||
| Температура вспышки | Нет применимо, пирофорный газ | ||
| Самовоспламенение. Температура | -40 ° C (-40 ° F; 233 K) | ||
| Родственные соединения | |||
| Родственные соединения | |||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Триметилборан (TMB) - токсичный пирофорный газ с формулой B (CH 3)3(которую также можно записать как s Me 3 B, где Me представляет метил ).
Как жидкость, он бесцветен. Самая яркая линия в инфракрасном спектре находится на 1330 см, за ней следуют линии на 3010 см и 1185 см.
Его температура плавления составляет -161,5 ° C, а температура кипения составляет -20,2 ° C.
Давление пара определяется как log P = 6,1385 + 1,75 log T - 1393,3 / T - 0,007735 T, где T - температура в кельвинах. Молекулярный вес 55,914. Теплота испарения составляет 25,6 кДж / моль.
Триметилборан был впервые описан в 1862 году Эдвардом Франклендом, который также упомянул его аддукт с аммиаком. Из-за своей опасной природы соединение больше не изучалось до 1921 года, когда Альфред Сток и Фридрих Цейдлер воспользовались преимуществом реакции между газообразным трихлоридом бора и диметилцинком. Хотя вещество может быть получено с использованием реактивов Гриньяра, выход загрязнен нежелательными продуктами из растворителя. Триметилборан может быть получен в небольшом масштабе с выходом 98% путем взаимодействия триметилалюминия в гексане с трибромидом бора в дибутиловом эфире в качестве растворитель. Другие методы включают взаимодействие с хлоридом триметилалюминия или тетрафторборатом калия с триметилалюмием. Еще один метод заключается в добавлении трифторида бора в эфире к.
Триметилборан спонтанно воспламеняется на воздухе, если концентрация достаточно высока. Он горит зеленым пламенем, образуя сажу. При более медленном окислении кислородом в растворителе или в газовой фазе может образоваться диметилтриоксадиборалан, содержащий кольцо из двух атомов бора и трех атомов кислорода. Однако основным продуктом является диметилборилметилпероксид, который быстро разлагается до диметоксиметилборана.
Триметилборан представляет собой сильную кислоту Льюиса. B (CH 3)3может образовывать аддукт с аммиаком : (NH 3): B (CH 3)3., А также с другими основаниями Льюиса. Кислотные свойства Льюиса ( B (CH 3)3был проанализирован с помощью модели ECW, получив E A = 2,90 и C A = 3,60. Когда триметилборан образует аддукт с триметиламин, стерическое отталкивание между метильными группами на результатах B и N. Модель ECW может обеспечить меру этого стерического эффекта.
Триметилборан реагирует с водой и хлором при комнатной температуре. Он также реагирует со смазкой, но не с тефлоном или стеклом.
Триметилборан реагирует с дибораном с диспропорционированием с образованием монометилдиборана и диметилдиборана : (CH 3) BH 2.BH 3 и (CH 3)2BH.BH 3.
Он реагирует как газ с триметилфосфином. с образованием твердой соли Льюиса с теплотой образования -41 ккал на моль. Этот аддукт имеет теплоту сублимации -24,6 ккал / моль. Реакция не происходит с триметиларсином или триметилстибин.
Метилитий, реагируя с триметилбораном, дает тетраметилборатную соль: LiB (CH 3)4. Ион тетраметилбората имеет отрицательный заряд и является изоэлектронным с неопентаном, тетраметилсиланом и катионом тетраметиламмония.
Триметилборан использовался в качестве счетчика нейтронов. Для этого он должен быть очень чистым. Он также используется в химическом осаждении из паровой фазы, где бор и углерод необходимо наносить вместе.