 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Триметилалюминий | |
| Другие имена Триметилалюминий; триметил алюминия; триметил алюминия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.000.776 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
| SMILES | |
| Свойства | |
| Химическая формула | C6H18Al2 |
| Молярная масса | 144,17 г / моль. 72,09 г / моль (C 3H9Al) |
| Внешний вид | Бесцветная жидкость |
| Плотность | 0,752 г / см |
| Точка плавления | 15 ° C (59 ° F; 288 K) |
| Точка кипения | 125-130 ° C (257-266 ° F; 398-403 K) |
| Растворимость в воде | Реагирует |
| Давление пара |
|
| Вязкость |
|
| Термохимия | |
| Теплоемкость (C) | 155,6 Дж / моль · K |
| Стандартная молярная. энтропия (S 298) | 209,4 Дж / моль · K |
| Стандартная энтальпия образования. (ΔfH298) | −136,4 кДж / моль |
| свободная энергия Гиббса (ΔfG˚) | -9,9 кДж / моль |
| Опасности | |
| Основные опасности | Пирофорные |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасностей GHS | H250, H260, H314 |
| Меры предосторожности GHS | P222, P223, P231 + 232, P280, P370 + 378, P422 |
| NFPA 704 (огненный алмаз) |  4 3 3 4 3 3 |
| Температура вспышки | −17,0 ° C (1,4 ° F ; 256,1 K) |
| Родственные соединения | |
| Родственные соединения | Триэтилалюминий |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
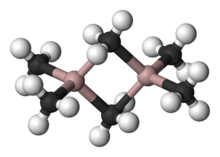
Триметилалюминий является одним из простейших примеров алюминийорганического соединения. Несмотря на свое название, он имеет формулу Al 2(CH3 )6(сокращенно Al 2Me6или TMA), так как он существует как димер. Эта бесцветная жидкость пирофорна. Это промышленно важное соединение, тесно связанное с триэтилалюминием.
Структура и связывание в Al 2R6и диборане аналогичны (R = алкил). В Al 2Me6расстояния Al-C (концевой) и Al-C (мостик) составляют 1,97 и 2,14 Å соответственно. Центр Al четырехгранный. Каждый атом углерода мостиковых этильных групп окружен пятью соседями: тремя атомами водорода и двумя атомами алюминия. Этильные группы легко меняются внутримолекулярно. При более высоких температурах димер расщепляется на мономерный AlMe 3.
ТМА получают с помощью двухэтапного процесса, который можно резюмировать следующим образом:
Начиная с изобретения Циглера-Натта при катализе, алюминийорганические соединения играют важную роль в производстве полиолефинов, таких как полиэтилен и полипропилен. Метилалюмоксан, который производится из ТМА, является активатором для многих катализаторов переходных металлов.
ТМА также используется в производстве полупроводников для нанесения тонких пленок с высоким k диэлектрики, такие как Al 2O3, посредством процессов химического осаждения из паровой фазы или осаждения атомных слоев. ТМА является предпочтительным предшественником для парофазной эпитаксии металлоорганических соединений (MOVPE ) алюминийсодержащих сложных полупроводников, например AlAs, AlN, AlP, AlSb, AlGaAs, AlGaN и т. д. Критерии качества ТМА сосредоточены на (а) элементарных примесях, (б) кислородсодержащих и органических примесях.
Триметилалюминий гидролизуется легко, даже опасно:
В контролируемых условиях реакцию можно остановить с получением метилалюмоксана:
Реакции алкоголиза и аминолиза протекают примерно одинаково. Например, диметиламин дает димер диамида диалюминия:
ТМА реагирует со многими галогенидами металлов с образованием алкильных групп. В сочетании с трихлоридом галлия дает триметилгаллий. Al 2Me6реагирует с трихлоридом алюминия с образованием (AlMe 2 Cl). 2.
Реакции ТМА / галогенида металла используются в качестве реагентов в органическом синтезе. Реагент Теббе, который используется для метиленирования сложных эфиров и кетонов, получают из ТМА и дихлорида титаноцена. В сочетании с 20-100 мол.% Cp 2 ZrCl 2(дихлорид цирконоцена ), (CH 3)2Al-CH 3 добавляет «поперек» алкинов, чтобы получить разновидности винилалюминия, которые используются в органическом синтезе в реакции, известной как карбоалюминирование.
Что касается других «электронодефицитных» соединений, триметилалюминий дает аддукты R3N.AlMe 3. Кислотные свойства Льюиса AlMe 3 были определены количественно. Данные по энтальпии показывают, что AlMe 3 является твердым кислоты и ее кислотные параметры в модели ECW равны E A = 8,66 и C A = 3,68.
Эти аддукты, например комплекс с третичным амином DABCO, более безопасен в обращении, чем сам TMA.
Миссия NASA ATREX (Аномальный перенос Ракетный эксперимент ) использовал белый дым, который ТМА образует при контакте с воздухом, для изучения высотного реактивного потока.
ТМА является источником метилнуклеофилов, сродни т. o метиллитий, но менее реакционноспособен. Он реагирует с кетонами, давая после гидролитической обработки третичные спирты.
Триметилалюминий пирофорен, бурно реагирует с воздухом и водой.
| На Викискладе есть средства массовой информации, относящиеся к триметилалюминий. |