 Схема топливного элемента PEM
Схема топливного элемента PEM Топливный элемент с протонообменной мембраной (PEMFC ), также известный как топливные элементы с мембраной с полимерным электролитом (PEM), представляют собой тип топливных элементов, разрабатываемых в основном для транспортных средств, а также для стационарных приложения для топливных элементов и приложения для переносных топливных элементов. Их отличительные особенности включают более низкие диапазоны температуры / давления (от 50 до 100 ° C) и специальную протонпроводящую полимерную электролитную мембрану. PEMFC генерируют электричество и работают по принципу, противоположному электролизу PEM, который потребляет электричество. Они являются ведущим кандидатом на замену стареющей технологии щелочных топливных элементов, которая использовалась в Space Shuttle.
PEMFC построены из мембранных электродных узлов (MEA), которые включают электроды, электролит, катализатор и газодиффузионные слои. Чернила из катализатора, углерода и электрода распыляются или окрашиваются на твердый электролит, а копировальная бумага подвергается горячему прессованию с обеих сторон, чтобы защитить внутреннюю часть ячейки, а также действовать как электроды. Центральная часть ячейки - это тройная фазовая граница (TPB), где смешиваются электролит, катализатор и реагенты и, таким образом, там, где на самом деле происходят реакции в ячейке. Важно отметить, что мембрана не должна быть электропроводной, чтобы не происходило смешение половинных реакций. Желательны рабочие температуры выше 100 ° C, чтобы побочным продуктом воды становился пар, а управление водой стало менее критичным в конструкции ячейки.
Топливный элемент с протонообменной мембраной преобразует химическую энергию, высвобождаемую во время электрохимической реакции водорода и кислорода, в электрическую энергию, в отличие от прямого сжигания газообразного водорода и кислорода для получения тепловой энергии.
Поток водорода подается на анодную сторону МЭБ. Со стороны анода он каталитически расщеплен на протоны и электроны. Эта реакция полуячейки окисления или реакция окисления водорода (HOR) представлена как:
На аноде:
 |  |  |
Вновь образованные протоны проникают через мембрану полимерного электролита на катодную сторону. Электроны перемещаются по внешней цепи нагрузки к катодной стороне MEA, создавая, таким образом, ток на выходе топливного элемента. Между тем, на катодную сторону МЭБ подается поток кислорода. На катодной стороне молекулы кислорода реагируют с протонами, проникающими через мембрану полимерного электролита, и электронами, проходящими через внешнюю цепь, с образованием молекул воды. Эта реакция восстановления полуячейки или реакция восстановления кислорода (ORR) представлена следующим образом:
На катоде:
 |  |  |
Общая реакция:
 |  |  |
Обратимая реакция выражается уравнением и показывает повторное включение водорода протоны и электроны вместе с молекулой кислорода и образование одной молекулы воды. В каждом случае потенциалы даны относительно стандартного водородного электрода.

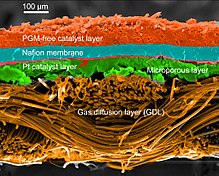 SEM-микрофотография поперечного сечения PEMFC MEA с катодом-катализатором из неблагородного металла и Pt / C-анодом. Для ясности применены ложные цвета.
SEM-микрофотография поперечного сечения PEMFC MEA с катодом-катализатором из неблагородного металла и Pt / C-анодом. Для ясности применены ложные цвета.  Методы изготовления МЭБ для PEMFC
Методы изготовления МЭБ для PEMFC Для функционирования мембрана должна проводить ионы водорода (протоны), но не электроны, так как это приведет к «короткому замыканию » топливного элемента. Мембрана также не должна позволять газу проходить на другую сторону ячейки, проблема известна как переход газа . Наконец, мембрана должна быть устойчивой к восстановительной среде на катоде, а также к жесткой окислительной среде на аноде.
Расщепление молекулы водорода относительно легко при использовании платинового катализатора. Однако, к сожалению, расщепление молекулы кислорода является более трудным, и это вызывает значительные электрические потери. Подходящий каталитический материал для этого процесса не найден, и платина - лучший вариант.
Более дешевой альтернативой платине является катализатор на основе оксида церия (IV), используемый исследовательской группой профессора Владимира Матолина при разработке PEMFC.
Благодаря своей компактности PEMFC является основным кандидатом для использования в транспортных средствах и других мобильных приложениях любого размера, вплоть до мобильных телефонов.
Топливные элементы на основе PEM по-прежнему имеют много проблем:
1. Управление водными ресурсами
Управление водными ресурсами имеет решающее значение для производительности: если вода испаряется слишком медленно, она затопит мембрану, и накопление воды внутри пластины полевого потока будет препятствовать потоку кислорода в топливный элемент, но если вода испаряется слишком быстро, мембрана высыхает и сопротивление через нее увеличивается. Оба случая приведут к нарушению стабильности и выходной мощности. Управление водой - очень сложный предмет в системах PEM, прежде всего потому, что вода в мембране притягивается к катоду ячейки через поляризацию.
Существует широкий спектр решений для управления водой, включая интеграцию электроосмотического насоса.
Еще одним инновационным методом решения проблемы рециркуляции воды является трехмерная конструкция поля потока с мелкими ячейками, используемая в Toyota Mirai., 2014. Традиционная конструкция дымовой трубы FC обеспечивает рециркуляцию воды от воздуховыпускного отверстия к воздухозаборнику через увлажнитель с прямым каналом и пористыми металлическими полями потока. Поле потока представляет собой структуру, состоящую из ребра и каналов. Однако ребро частично покрывает газодиффузионный слой (GDL), и результирующее расстояние транспортировки газа больше, чем расстояние между каналами. Кроме того, контактное давление между GDL и ребром также сжимает GDL, делая его толщину неоднородной по ребру и каналу. Большая ширина и неоднородная толщина ребра увеличивают вероятность накопления водяного пара, и кислород будет скомпрометирован. В результате кислород не сможет диффундировать в слой катализатора, что приведет к неравномерной выработке энергии в FC.
Эта новая конструкция позволила использовать первый стек FC без системы увлажнения, одновременно преодолев проблемы рециркуляции воды и достигнув высокой стабильности выходной мощности. Трехмерная микрорешетка обеспечивает больше путей для потока газа; следовательно, он способствует потоку воздуха к мембранному электроду и узлу газодиффузионного слоя (MEGA) и способствует диффузии O2 к слою катализатора. В отличие от обычных полей потока, трехмерные микрочастицы в сложном поле, которые действуют как перегородки и вызывают частые микромасштабные межфазные потоки между GDL и полями потока. Благодаря этому повторяющемуся микромасштабному конвективному потоку перенос кислорода к слою катализатора (CL) и удаление жидкой воды из GDL значительно улучшаются. Образующаяся вода быстро вытягивается через поле потока, предотвращая накопление в порах. В результате выработка энергии из этого поля потока однородна по всему поперечному сечению, и включается самовлажнение.
2. Уязвимость катализатора
Платиновый катализатор на мембране легко отравляется оксидом углерода (обычно допускается не более одной части на миллион), и мембрана чувствительна к таким вещам, как ионы металлов, которые могут быть внесены коррозия металлических биполярных пластин, металлических компонентов в системе топливных элементов или загрязняющих веществ в топливе / окислителе.
системы PEM, в которых используется реформированный метанол, были предложены, как в Daimler Chrysler Necar 5; риформинг метанола, то есть его взаимодействие с получением водорода, является, однако, очень сложным процессом, который также требует очистки от монооксида углерода, образующегося в результате реакции. Катализатор платина - рутений необходим, поскольку некоторое количество оксида углерода неизбежно достигнет мембраны. Уровень не должен превышать 10 частей на миллион. Кроме того, время запуска такого реактора риформинга составляет около получаса. В качестве альтернативы, метанол и некоторые другие биотопливо могут подаваться в топливный элемент PEM напрямую без риформинга, таким образом создавая топливный элемент с прямым метанолом (DMFC ). Эти устройства работают с ограниченным успехом.
3. Ограничение рабочей температуры
Наиболее часто используемой мембраной является Nafion от Chemours, которая основана на увлажнении мембраны жидкой водой для переноса протонов. Это означает, что невозможно использовать температуры выше 80–90 ° C, так как мембрана высохнет. Другие, более современные типы мембран, основанные на полибензимидазоле (PBI) или фосфорной кислоте, могут достигать 220 ° C без использования какого-либо управления водой: более высокая температура позволяет повысить эффективность, мощность плотность, легкость охлаждения (из-за большей допустимой разницы температур), пониженная чувствительность к отравлению угарным газом и лучшая управляемость (из-за отсутствия проблем с водоотведением в мембране); однако эти недавние типы не так распространены. PBI может быть легирован фосфорной или серной кислотой, а проводимость зависит от количества легирования и температуры. При высоких температурах трудно сохранять нафион гидратированным, но этот легированный кислотой материал не использует воду в качестве среды для протонной проводимости. Он также обладает лучшими механическими свойствами, большей прочностью, чем нафион, и дешевле. Однако кислотное выщелачивание представляет собой серьезную проблему, и обработка, смешанная с катализатором для образования чернил, оказалась сложной. Ароматические полимеры, такие как PEEK, намного дешевле тефлона (PTFE и основная цепь Nafion), и их полярный характер приводит к гидратации, которая меньше зависит от температуры, чем Nafion. Однако PEEK имеет гораздо меньшую ионную проводимость, чем Nafion, и поэтому является менее подходящим выбором электролита. Недавно протонные ионные жидкости и протонные органические ионные пластические кристаллы были показаны как многообещающие альтернативные электролитические материалы для высокотемпературных (100–200 ° C) PEMFC.
Электрод обычно состоит из углерода носитель, частицы Pt, иономер нафион и / или тефлоновое связующее. Углеродная опора действует как электрический проводник; частицы Pt являются центрами реакции; иономер обеспечивает пути для протонной проводимости, а тефлоновое связующее увеличивает гидрофобность электрода, чтобы минимизировать возможное затопление. Чтобы обеспечить электрохимические реакции на электродах, протоны, электроны и газы-реагенты (водород или кислород) должны получить доступ к поверхности катализатора в электродах, в то время как вода-продукт, которая может находиться в жидкой или газовой фазе. или обе фазы должны иметь возможность проникать от катализатора к выпускному отверстию для газа. Эти свойства обычно реализуются за счет пористых композитов связующего полимерного электролита (иономера) и наночастиц катализатора, нанесенных на углеродные частицы. Обычно платина используется в качестве катализатора электрохимических реакций на аноде и катоде, в то время как наночастицы обеспечивают высокое отношение поверхности к массе (как дополнительно описано ниже), что снижает количество дорогостоящей платины. Связующее из полимерного электролита обеспечивает ионную проводимость, в то время как углеродная подложка катализатора улучшает электрическую проводимость и обеспечивает низкое содержание металлической платины. Электропроводность композитных электродов обычно более чем в 40 раз выше, чем протонная проводимость.
GDL электрически соединяет катализатор и токоприемник. Он должен быть пористым, электропроводящим и тонким. Реагенты должны достигать катализатора, но проводимость и пористость могут действовать как противодействующие силы. Оптимально, GDL должен состоять из примерно одной трети Nafion или 15% PTFE. Частицы углерода, используемые в GDL, могут быть больше, чем частицы, используемые в катализаторе, поскольку площадь поверхности не является наиболее важной переменной в этом слое. GDL должен иметь толщину около 15–35 мкм, чтобы сбалансировать необходимую пористость с механической прочностью. Часто промежуточный пористый слой добавляется между GDL и слоем катализатора, чтобы облегчить переходы между большими порами в GDL и небольшой пористостью в слое катализатора. Поскольку основная функция GDL заключается в том, чтобы помочь удалить воду, продукт, затопление может произойти, когда вода эффективно блокирует GDL. Это ограничивает доступ реагентов к катализатору и значительно снижает производительность. На GDL можно нанести тефлоновое покрытие, чтобы ограничить возможность затопления. В GDLS анализируются несколько микроскопических переменных, таких как пористость, извилистость и проницаемость. Эти переменные влияют на поведение топливных элементов.
Максимальный теоретический КПД с применением уравнения свободной энергии Гиббса ΔG = -237,13 кДж / моль и использования теплотворная способность водорода (ΔH = -285,84 кДж / моль) составляет 83% при 298 К.

Практическая эффективность ФЭУ находится в диапазоне 50–60 %. Основные факторы, вызывающие потери:
Металлоорганические каркасы (MOF) являются относительно новый класс пористых высококристаллических материалов, которые состоят из металлических узлов, соединенных органическими линкерами. Из-за простоты манипулирования металлическими центрами и лигандами или их замены существует практически неограниченное количество возможных комбинаций, что является привлекательным с точки зрения дизайна. MOF демонстрируют множество уникальных свойств благодаря регулируемым размерам пор, термической стабильности, высокой объемной емкости, большой площади поверхности и желаемым электрохимическим характеристикам. Среди множества разнообразных применений, MOF являются многообещающими кандидатами для приложений чистой энергии, таких как хранение водорода, разделение газов, суперконденсаторы, литий-ионные батареи, солнечные элементы и топливные элементы. В области исследований топливных элементов MOF изучаются как потенциальные материалы для электролитов и электродных катализаторов, которые когда-нибудь могут заменить традиционные полимерные мембраны и Pt-катализаторы, соответственно.
В качестве материалов электролита включение MOF на первый взгляд кажется нелогичным. Мембраны топливных элементов обычно имеют низкую пористость, чтобы предотвратить переход топлива и потерю напряжения между анодом и катодом. Кроме того, мембраны имеют тенденцию к низкой кристалличности, поскольку перенос ионов более благоприятен в неупорядоченных материалах. С другой стороны, поры могут быть заполнены дополнительными ионными носителями, которые в конечном итоге увеличивают ионную проводимость системы, а высокая кристалличность делает процесс проектирования менее сложным.
Общие требования к хорошему электролиту для PEMFC: высокая протонная проводимость (>10 См / см для практических применений), обеспечивающая перенос протонов между электродами, хорошая химическая и термическая стабильность в условиях эксплуатации топливных элементов (влажность окружающей среды, переменные температуры, устойчивость к ядовитым веществам и т. д.), низкая стоимость, возможность переработки в тонкие пленки и общая совместимость с другими компонентами клеток. В то время как полимерные материалы в настоящее время являются предпочтительным выбором для протонпроводящей мембраны, они требуют увлажнения для адекватной работы и иногда могут физически разрушаться из-за эффектов гидратации, что приводит к потере эффективности. Как уже упоминалось, Nafion также ограничен температурой дегидратации < 100 °C, which can lead to slower reaction kinetics, poor cost efficiency, and CO poisoning of Pt electrode catalysts. Conversely, MOFs have shown encouraging proton conductivities in both low and high temperature regimes as well as over a wide range of humidity conditions. Below 100 °C and under hydration, the presence of hydrogen bonding and solvent water molecules aid in proton transport, whereas anhydrous conditions are suitable for temperatures above 100 °C. MOFs also have the distinct advantage of exhibiting proton conductivity by the framework itself in addition to the inclusion of charge carries (i.e., water, acids, etc.) into their pores.
. Примером низкой температуры является работа Kitagawa, et al. которые использовали двумерный каркас анионного слоя с оксалатным мостиком в качестве основы и вводили катионы аммония и молекулы адипиновой кислоты в поры для увеличения концентрации протонов. Результатом стал один из первых примеров MOF, демонстрирующего «суперпротонную» проводимость (8 × 10 См / см) при 25 ° C и 98% относительной влажности (RH). Позже они обнаружили, что увеличение гидрофильности катионов, вводимых в поры, может еще больше повысить протонную проводимость. В этом низкотемпературном режиме, который зависит от степени гидратации, также было показано, что протонная проводимость сильно зависит от уровня влажности.
Примером высокотемпературного безводного вещества является PCMOF2, который состоит из ионов натрия, координированных с трисульфированным производным бензола. Чтобы улучшить характеристики и обеспечить более высокие рабочие температуры, воду в качестве носителя протонов можно заменить менее летучими молекулами имидазола или триазола в порах. Достигнутая максимальная температура составляла 150 ° C с оптимальной проводимостью 5 × 10 См / см, что ниже, чем у других современных электролитных мембран. Однако эта модель является многообещающей благодаря ее температурному режиму, безводным условиям и способности контролировать количество молекул-гостей в порах, что позволяет настраивать протонную проводимость. Кроме того, загруженный триазолом PCMOF2 был включен в узел мембрана-электрод из H 2 / воздух и достиг напряжения холостого хода 1,18 В при 100 ° C, которое было стабильным в течение 72 часов и позволяло оставаться газонепроницаемым. на протяжении всего тестирования. Это был первый пример, который доказал, что MOF действительно могут быть внедрены в действующие топливные элементы, а умеренная разность потенциалов показала, что переход топлива из-за пористости не является проблемой.
На сегодняшний день самая высокая протонная проводимость, достигнутая для электролита MOF, составляет 4,2 × 10 См / см при 25 ° C во влажных условиях (98% относительной влажности), что является конкурентоспособным с Nafion. В некоторых недавних экспериментах даже были успешно получены тонкопленочные мембраны MOF вместо традиционных объемных образцов или монокристаллов, что имеет решающее значение для их промышленного применения. Как только MOF смогут стабильно обеспечивать достаточный уровень проводимости, механическую прочность, водостойкость и простоту обработки, они потенциально могут сыграть важную роль в PEMFC в ближайшем будущем.
MOF также были нацелены на потенциальную замену материалов металлов платиновой группы (МПГ) для электродных катализаторов, хотя эти исследования все еще находятся на ранних стадиях разработки. В PEMFC реакция восстановления кислорода (ORR) на платиновом катоде протекает значительно медленнее, чем реакция окисления топлива на аноде, поэтому в качестве альтернативы исследуются катализаторы, не содержащие МПГ и не содержащие металлов. Высокая объемная плотность, большая площадь поверхности пор и открытость центров ионов металлов в MOF делают их идеальными кандидатами в качестве предшественников катализаторов. Несмотря на многообещающие каталитические способности, долговечность этих предложенных катализаторов на основе MOF в настоящее время менее желательна, и механизм ORR в этом контексте все еще полностью не изучен.
Большая часть текущих исследований катализаторов для топливных элементов PEM может быть классифицирована как преследующая одну из следующих основных целей:
Примеры этих подходов приведены в следующих разделах.
Как упоминалось выше, платина на сегодняшний день является наиболее эффективным элементом, используемым для катализаторов топливных элементов с PEM, и почти все современные топливные элементы с PEM используют частицы платины на пористых углеродных носителях для катализирования как окисление водорода, так и восстановление кислорода. Однако из-за их высокой стоимости современные катализаторы Pt / C нецелесообразны для коммерческого использования. США По оценкам Министерства энергетики, в катализаторах на основе платины потребуется примерно в четыре раза меньше платины, чем в текущих конструкциях топливных элементов с PEM, чтобы представить реалистичную альтернативу двигателям внутреннего сгорания. Следовательно, одной из основных целей конструкции катализатора для топливных элементов с PEM является повышение каталитической активности платины в четыре раза, так что для достижения аналогичных характеристик требуется только одна четвертая часть драгоценного металла.
Одним из способов повышения эффективности платиновых катализаторов является оптимизация размера и формы частиц платины. Уменьшение размера частиц само по себе увеличивает общую площадь поверхности катализатора, доступного для участия в реакциях, в расчете на объем использованной платины, но недавние исследования продемонстрировали дополнительные способы дальнейшего улучшения каталитических характеристик. Например, в одном исследовании сообщается, что высокоиндексные грани платиновых наночастиц (то есть индексы Миллера с большими целыми числами, такими как Pt (730)) обеспечивают большую плотность реактивных сайтов для снижение содержания кислорода по сравнению с типичными наночастицами платины.
Поскольку наиболее распространенный и эффективный катализатор, платина, чрезвычайно дорог, необходима альтернативная обработка, чтобы максимизировать площадь поверхности и минимизировать нагрузку. Осаждение наноразмерных частиц Pt на углеродный порошок (Pt / C) обеспечивает большую площадь поверхности Pt, в то время как углерод обеспечивает электрическое соединение между катализатором и остальной частью ячейки. Платина настолько эффективна, потому что она обладает высокой активностью и связывается с водородом достаточно сильно, чтобы облегчить перенос электронов, но не препятствовать продолжению движения водорода по ячейке. Однако платина менее активна в реакции катодного восстановления кислорода. Это требует использования большего количества платины, что увеличивает стоимость элемента и, следовательно, его осуществимость. Многие возможные варианты катализатора исключаются из-за чрезмерной кислотности ячейки.
Наиболее эффективными способами достижения наноразмеров Pt на углеродном порошке, который в настоящее время является лучшим вариантом, являются вакуумное осаждение, распыление и электроосаждение. Частицы платины наносятся на копировальную бумагу, пропитанную ПТФЭ. Однако этот слой катализатора имеет оптимальную толщину, что ограничивает нижний предел стоимости. Ниже 4 нм Pt образует островки на бумаге, ограничивая ее активность. При толщине, превышающей эту толщину, Pt будет покрывать углерод и быть эффективным катализатором. Еще больше усложняет ситуацию то, что нафион не может проникнуть за пределы 10 мкм, поэтому использование большего количества Pt, чем это, является ненужными расходами. Таким образом, количество и форма катализатора ограничены ограничениями других материалов.
Второй способ увеличения каталитической активности платины заключается в сплаве ее с другими металлами. Например, недавно было показано, что поверхность Pt 3 Ni (111) имеет более высокую активность восстановления кислорода, чем чистая Pt (111), в десять раз. Авторы объясняют это резкое повышение производительности модификациями электронной структуры поверхности, снижая ее тенденцию связываться с кислородсодержащими ионными частицами, присутствующими в топливных элементах PEM, и, следовательно, увеличивая количество доступных участков для кислорода адсорбция и восстановление.
Дополнительная эффективность может быть реализована с использованием ультразвукового сопла для нанесения платинового катализатора на слой электролита или на копировальную бумагу в атмосферных условиях, что приводит к высокоэффективному распылению. Исследования показали, что из-за однородного размера капель, создаваемых этим типом спрея, из-за высокой эффективности переноса технологии, из-за того, что сопло не засоряется, и, наконец, из-за того, что энергия ультразвука деформируется. -агломерирует суспензию непосредственно перед распылением, топливные элементы MEA, изготовленные таким образом, имеют большую однородность в конечном MEA, а поток газа через элемент более однороден, что максимизирует эффективность платины в MEA. Недавние исследования с использованием струйной печати для нанесения катализатора на мембрану также показали высокую степень использования катализатора из-за уменьшенной толщины нанесенных слоев катализатора.
Совсем недавно появился новый класс электрокатализаторов ORR были введены в случае систем Pt-M (M-Fe и Co) с упорядоченным интерметаллическим ядром, заключенным в оболочку, богатую Pt. Было обнаружено, что эти интерметаллические нанокатализаторы ядро-оболочка (IMCS) проявляют повышенную активность и, что наиболее важно, повышенную долговечность по сравнению со многими предыдущими разработками. В то время как наблюдаемое усиление активности приписывается напряженной решетке, авторы сообщают, что их выводы о кинетике разложения устанавливают, что увеличенная каталитическая стойкость объясняется устойчивым атомным порядком.
Другим популярным подходом к улучшению характеристик катализатора является снижение его чувствительности к примесям в источнике топлива, особенно к монооксиду углерода (CO). В настоящее время чистый газообразный водород становится экономичным для массового производства посредством электролиза. Однако в настоящее время газообразный водород получают с помощью парового риформинга легких углеводородов, процесса, при котором образуется смесь газов, которая также содержит CO (1–3%), CO 2 (19–25%) и N 2 (25%). Даже десятки частей на миллион CO могут отравить чистый платиновый катализатор, поэтому повышение устойчивости платины к CO является активной областью исследований.
Например, в одном исследовании сообщается, что наночастицы платины кубической формы с (100) гранями демонстрируют четырехкратное увеличение активности восстановления кислорода по сравнению со случайно граненными наночастицами платины аналогичного размера. Авторы пришли к выводу, что грани (111) наночастиц произвольной формы сильнее связаны с сульфат-ионами, чем грани (100), уменьшая количество каталитических центров, открытых для молекул кислорода. Синтезированные ими нанокубки, напротив, имели почти исключительно (100) граней, которые, как известно, слабее взаимодействуют с сульфатом. В результате большая часть площади поверхности этих частиц была доступна для восстановления кислорода, что повысило активность катализатора по восстановлению кислорода.
Кроме того, исследователи изучали способы снижения содержания CO в водородном топливе до того, как он попадет в топливный элемент, как возможный способ избежать отравления катализаторов. Одно недавнее исследование показало, что рутениево-платиновые наночастицы ядро-оболочка особенно эффективны при окислении CO с образованием CO 2, гораздо менее вредного загрязнителя топлива. Механизм, вызывающий этот эффект, концептуально аналогичен описанному выше для Pt 3 Ni: рутениевое ядро частицы изменяет электронную структуру поверхности платины, делая ее более способной катализировать окисление CO.
Сегодня проблема жизнеспособности топливных элементов PEM по-прежнему заключается в их стоимости и стабильности. Высокая стоимость в значительной степени может быть связана с использованием драгоценного металла платины в слое катализатора ячеек PEM. Электрокатализатор в настоящее время составляет почти половину стоимости батареи топливных элементов. Хотя содержание Pt в топливных элементах с PEM было уменьшено на два порядка за последнее десятилетие, необходимо дальнейшее сокращение, чтобы сделать технологию экономически жизнеспособной для коммерциализации. В то время как некоторые исследовательские усилия направлены на решение этой проблемы путем повышения электрокаталитической активности катализаторов на основе Pt, альтернативой является полное исключение использования Pt путем разработки катодного катализатора на основе неплатиновой группы (не МПГ), чьи характеристики не уступают технология Pt. Министерство энергетики США установило вехи для разработки топливных элементов, нацеленных на срок службы 5000 часов и объемную активность ORR не-МПГ катализатора 300 А см.
Многообещающими альтернативами катализаторам на основе Pt являются Металл / азот / углерод-катализаторы (M / N / C-катализаторы). Для достижения высокой плотности мощности или выхода мощности по площади поверхности элемента необходимо обеспечить объемную активность, по меньшей мере, 1/10 от активности катализаторов на основе Pt, наряду с хорошими свойствами массопереноса. Хотя катализаторы M / N / C по-прежнему демонстрируют более низкую объемную активность, чем катализаторы на основе Pt, снижение стоимости таких катализаторов позволяет компенсировать большую нагрузку. Однако увеличение загрузки катализаторов M / N / C также делает каталитический слой более толстым, ухудшая его свойства массопереноса. Другими словами, H 2, O 2, протоны и электроны испытывают большие трудности при перемещении через каталитический слой, что снижает выходное напряжение ячейки. В то время как высокая микропористость каталитической сетки M / N / C приводит к высокой объемной активности, улучшенные свойства массопереноса вместо этого связаны с макропористостью сетки. Эти материалы M / N / C синтезируются с использованием высокотемпературного пиролиза и другой высокотемпературной обработки прекурсоров, содержащих металл, азот и углерод.
Недавно исследователи разработали катализатор Fe / N / C, полученный из железа. (II) ацетат (FeAc), фенантролин (Phen) и металлорганический каркас (MOF). MOF представляет собой каркас из цеолитного имидазолата Zn (II) (ZIF), называемый ZIF-8, который демонстрирует большую площадь микропористой поверхности и высокое содержание азота, способствующее активности ORR. Плотность мощности катализатора FeAc / Phen / ZIF-8 составила 0,75 Вт / см при 0,6 В. Это значение является значительным улучшением по сравнению с максимальной плотностью мощности 0,37 Вт / см для предыдущих катализаторов M / N / C и составляет намного ближе к соответствию типичному значению 1,0–1,2 Вт / см для катализаторов на основе Pt с содержанием Pt 0,3 мг / см3. Катализатор также продемонстрировал объемную активность 230 А · см, что является наивысшим значением для катализаторов, не содержащих МПГ, на сегодняшний день, приближаясь к рубежу Министерства энергетики США.
Хотя удельная мощность, достигаемая новым катализатором FeAc / Phen / ZIF-8, является многообещающей, его долговечность остается недостаточной для коммерческого применения. Сообщается, что лучшая долговечность, продемонстрированная этим катализатором, все же имела 15% -ное падение плотности тока за 100 часов в H 2 / воздух. Следовательно, хотя катализаторы на основе Fe, не содержащие МПГ, по своей электрокаталитической активности конкурируют с катализаторами на основе Pt, предстоит еще многое сделать для понимания механизмов их разложения и повышения их долговечности.
Основное применение топливных элементов PEM сосредоточено на транспортировке в первую очередь из-за их потенциального воздействия на окружающую среду, например контроль выбросов парниковых газов (ПГ). Другие приложения включают распределенную / стационарную и портативную генерацию электроэнергии. Большинство крупных автомобилестроительных компаний работают исключительно на топливных элементах из ПЭМ из-за их высокой удельной мощности и отличных динамических характеристик по сравнению с другими типами топливных элементов. Благодаря небольшому весу PEMFC наиболее подходят для транспортных средств. PEMFC для автобусов, в которых в качестве топлива используется сжатый водород, могут работать с КПД до 40%. Обычно PEMFC внедряются в автобусах, а не в автомобилях меньшего размера из-за доступного объема для размещения системы и хранения топлива. Технические проблемы для транспорта включают в себя включение PEM в современные автомобильные технологии и обновление энергетических систем. Транспортные средства, полностью заполненные топливными элементами, невыгодны, если водород получают из ископаемого топлива; однако они становятся полезными при использовании в виде гибридов. Есть потенциал для использования PEMFC для стационарной выработки электроэнергии, где они обеспечивают 5 кВт при 30% КПД; однако они конкурируют с другими типами топливных элементов, в основном SOFC и MCFC. В то время как для работы PEMFC обычно требуется водород высокой чистоты, другие типы топливных элементов могут работать на метане и, таким образом, являются более гибкими системами. Следовательно, PEMFC лучше всего подходят для небольших систем, пока не станет доступным экономически масштабируемый чистый водород. Кроме того, у PEMFC есть возможность заменить батареи для портативной электроники, хотя интеграция источника водорода является технической проблемой, особенно без удобного места для его хранения в устройстве.
До изобретение топливных элементов PEM, существующие типы топливных элементов, такие как твердооксидные топливные элементы, применялись только в экстремальных условиях. Такие топливные элементы также требовали очень дорогих материалов и из-за своего размера могли использоваться только для стационарных применений. Эти проблемы были решены с помощью топливного элемента PEM. Топливный элемент PEM был изобретен в начале 1960-х Уиллардом Томасом Граббом и Леонардом Нидрахом из General Electric. Первоначально мембраны из сульфированного полистирола использовались для электролитов, но в 1966 году они были заменены иономером Nafion , который оказался лучше сульфированного полистирола по характеристикам и долговечности.
Топливные элементы PEM использовались в космических аппаратах серии NASA Gemini, но они были заменены на щелочные топливные элементы в Программа Apollo и в программе Space Shuttle.
Параллельно с Pratt and Whitney Aircraft, General Electric разработала первые топливные элементы с протонообменной мембраной (PEMFC) для космических миссий Gemini в начале 1960-х. Первой миссией по использованию PEMFC была Gemini V. Однако в космических миссиях Аполлон и последующих Аполлонах-Союз, Скайлэб и космических челноках использовались топливные элементы, основанные на конструкции Бэкона, разработанной Pratt and Whitney Aircraft.
Были использованы чрезвычайно дорогие материалы, а топливные элементы требовали очень чистого водорода и кислорода. Ранние топливные элементы, как правило, требовали неудобно высоких рабочих температур, что было проблемой во многих приложениях. Тем не менее, топливные элементы были признаны желательными из-за большого количества топлива. доступны (водород и кислород).
Несмотря на успех в космических программах, системы топливных элементов были ограничены космическими полетами и другими специальными приложениями, где можно было допустить высокую стоимость. Только в конце 1980-х и начале 1990-х топливные элементы стали реальным вариантом для более широкого применения. Несколько ключевых нововведений, таких как загрузка катализатора с низким содержанием платины и тонкопленочные электроды, снизили стоимость топливных элементов, сделав разработку систем PEMFC более реалистичной. Однако ведутся серьезные споры относительно того, будут ли водородные топливные элементы реальной технологией для использования в автомобилях или других транспортных средствах. (См. водородная экономия.) Большая часть производства PEMFC предназначена для Toyota Mirai. Министерство энергетики США оценивает цену в 2016 г. в 53 доллара за кВт, если будет производиться 500 000 единиц в год.
.