 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Церий (IV) оксид | |
| Другие названия Оксид церия,. Церий,. Диоксид церия | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.013.774 |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | CeO 2 |
| Молярная масса | 172,115 г / моль |
| Внешний вид | белое или бледно-желтое твердое вещество,. слегка гигроскопично |
| Плотность | 7,215 г / см |
| Точка плавления | 2400 ° C (4350 ° F; 2670 K) |
| Точка кипения | 3500 ° C (6330 ° F; 3770 K) |
| Растворимость в воде | нерастворим |
| Магнитная восприимчивость (χ) | + 26,0 · 10 см / моль |
| Структура | |
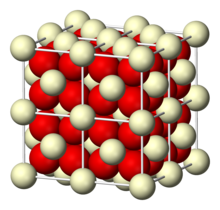
| Кристаллическая структура | кубическая (флюорит ) |
| Опасности | |
| NFPA 704 (огненный алмаз) |  0 1 0 0 1 0 |
| Родственные соединения | |
| Родственные соединения | Оксид церия (III) |
| Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Оксид церия (IV), также известный как оксид церия, диоксид церия, церий, оксид церия или диоксид церия, представляет собой оксид редкоземельного металла церий. Это бледно-желто-белый порошок с химической формулой CeO 2. Это важный коммерческий продукт и промежуточное соединение при очистке элемента от руд. Отличительным свойством этого материала является его обратимое превращение в нестехиометрический оксид.
Церий встречается в природе в виде смеси с другими редкоземельными элементами в основных рудах бастнезит и монацит. После экстракции ионов металла водным основанием Ce отделяют от этой смеси добавлением окислителя с последующим регулированием pH. На этом этапе используется низкая растворимость CeO 2 и тот факт, что другие редкоземельные элементы сопротивляются окислению.
Оксид церия (IV) образуется при прокаливании оксалат церия или гидроксид церия.
Церий также образует оксид церия (III), Ce. 2O. 3, который является нестабильным и окисляется до оксида церия (IV).
Оксид церия имеет структуру флюорита, пространственная группа Fm 3 m, # 225, содержащая 8-координатный Ce и 4 -координата O. При высоких температурах он выделяет кислород с образованием нестехиометрической, дефицитной анионами формы, которая сохраняет решетку флюорита. Этот материал имеет формулу CeO (2 − x), где 0 < x < 0.28. The value of x depends on both the temperature, surface termination and the oxygen partial pressure. The equation

предсказывает равновесную нестехиометрию x в широком диапазоне парциального давления кислорода (10–10 Па) и температуры (1000–1900 ° C).
Нестехиометрическая форма имеет цвет от синего до черного и проявляет как ионную, так и электронную проводимость, причем ионная является наиболее значимо при температурах>500 ° C.
Количество кислородных вакансий часто измеряется с помощью рентгеновской фотоэлектронной спектроскопии для сравнения отношения Ce. к Ce..
В наиболее стабильной флюоритной фазе диоксида церия обнаруживается несколько дефектов в зависимости от парциального давления кислорода или напряженного состояния материала.
Основные дефекты, вызывающие озабоченность кислородные вакансии и малые поляроны (электроны, локализованные на катионах церия). Увеличение концентрации кислородных дефектов увеличивает скорость диффузии оксидных анионов в решетке, что отражается в увеличении ионной проводимости. Эти факторы обеспечивают благоприятные рабочие характеристики оксида церия при применении в качестве твердого электролита в твердооксидных топливных элементах. Нелегированный и легированный диоксид церия также демонстрируют высокую электронную проводимость при низких парциальных давлениях кислорода из-за восстановления иона церия, приводящего к образованию небольших поляронов. Поскольку атомы кислорода в кристалле церия расположены в плоскостях, диффузия этих анионов легка. Скорость диффузии увеличивается с увеличением концентрации дефектов.
Присутствие кислородных вакансий на концевых плоскостях церия определяет энергетику взаимодействия церия с молекулами адсорбата и его смачиваемость. Контроль таких поверхностных взаимодействий является ключом к использованию оксида церия в каталитических приложениях.
Основным новым применением применяемых материалов CeO 2 является область катализа. На поверхности церия в его наиболее стабильной флюоритной фазе преобладают плоскости (111) с более низкой энергией, которые имеют тенденцию проявлять более низкую поверхностную энергию. Реакция, наиболее часто катализируемая церием (IV), представляет собой реакцию конверсии водяного газа, включающую окисление моноксида углерода. Церий был исследован для катализа различных реакций конверсии углеводородов, включая CO 2метанирование и каталитическое окисление углеводородов, таких как толуол.
Поверхностная функциональность CeO 2 в значительной степени определяется из-за его внутренней гидрофобности, признака, который является общим для оксидов редкоземельных элементов. Гидрофобность имеет тенденцию придавать устойчивость к дезактивации воды на поверхности катализаторов и, таким образом, усиливает адсорбцию органических соединений. Гидрофобность, которую, наоборот, можно рассматривать как органофильность, обычно связана с более высокими каталитическими характеристиками и желательна в приложениях, связанных с органическими соединениями и селективным синтезом.
Взаимопревращаемость материалов CeO x является основой использования оксида церия в качестве катализатора окисления. Одним из небольших, но иллюстративных вариантов использования является его использование в стенках самоочищающихся печей в качестве катализатора окисления углеводородов в процессе высокотемпературной очистки. Другой небольшой, но известный пример - его роль в окислении природного газа в газовых оболочках.
 светящихся Колеманов белых газовых мантийных фонарях. Раскаленный элемент в основном ThO 2, легированный CeO 2, нагретый в результате катализируемого церием окисления природного газа воздухом.
светящихся Колеманов белых газовых мантийных фонарях. Раскаленный элемент в основном ThO 2, легированный CeO 2, нагретый в результате катализируемого церием окисления природного газа воздухом. Основываясь на его различных взаимодействиях с поверхностью, церий находит также использовать в качестве датчика в каталитических нейтрализаторах в автомобильной промышленности, контролируя соотношение воздуха и выхлопных газов для уменьшения выбросов NOx и угарного газа.
Основным промышленным применением оксида церия является полирование, особенно химико-механическое выравнивание (CMP). Для этой цели он вытеснил многие другие оксиды, которые использовались ранее, такие как оксид железа и диоксид циркония. Для любителей это также известно как «румяна для оптиков».
CeO 2 используется для обесцвечивания стекла путем превращения зеленых примесей железа в почти бесцветные. оксиды железа.
Оксид церия нашел применение в инфракрасных фильтрах, в качестве окислителя в каталитических конвертерах и в качестве замены диоксида тория в раскаленных оболочках
Благодаря значительной ионной и электронной проводимости оксида церия, он хорошо подходит для использования в качестве смешанного проводника, имеющего важное значение в исследованиях и разработках топливных элементов.
Наночастицы оксида церия (наноцерии) были исследованы на предмет их антибактериальной и антиоксидантной активности.
Хотя он прозрачен для видимого света, он сильно поглощает ультрафиолетовое излучение, поэтому он является перспективной заменой оксида цинка и диоксида титана в солнцезащитных кремах, так как он имеет более низкую фотокаталитическую активность. Однако его термокаталитические свойства должны быть снижены путем покрытия частиц аморфным диоксидом кремния или нитридом бора.
Церий представляет интерес как материал для твердооксидные топливные элементы (ТОТЭ) из-за их относительно высокой кислородной ионной проводимости (т.е. атомы кислорода легко проходят через него) при промежуточных температурах (500–650 ° C) и более низкой энтальпии ассоциации по сравнению с Система диоксида циркония.
Цикл оксид церия (IV) – оксид церия (III) или CeO 2 / Ce 2O3цикл представляет собой двухэтапный термохимический процесс разделения воды на основе оксида церия (IV) и оксида церия (III) для производства водорода.
Nanoceria привлекла внимание как биологический антиоксидант.