аллильная перегруппировка или аллильный сдвиг - это органическая реакция, в которой двойная связь в химическом соединении аллил смещается к следующему атому углерода. Это встречается при нуклеофильном замещении.
в условиях реакции, которые благоприятствуют реакции SN1 Механизм, промежуточным звеном является карбокатион , для которого возможны несколько резонансных структур. Это объясняет p распределение продукта (или распределение продукта ) после рекомбинации с нуклеофилом Y. Этот тип процесса называется заменой SN1 '. .
В качестве альтернативы, нуклеофил может атаковать непосредственно в аллильном положении, вытесняя уходящую группу за один этап, в процессе, называемом SN2 'замена . Это вероятно в случаях, когда аллильное соединение беспрепятственно, и используется сильный нуклеофил. Продукты будут аналогичны продуктам с заменой S N 1 '. Таким образом, реакция 1-хлор-2-бутена с гидроксидом натрия дает смесь 2-бутен-1-ола и 3-бутен-2-ола:
Тем не менее, продукт, в котором OH группа находится на первичном атоме второстепенная. При замещении 1-хлор-3-метил-2-бутена вторичный 2-метил-3-бутен-2-ол получается с выходом 85%, тогда как выход первичного 3-метил-2-бутена -1-ол составляет 15%.
В одном механизме реакции нуклеофил атакует не непосредственно по электрофильному сайту, а путем присоединения конъюгата по двойной связи:
Это обычно для аллильных соединений которые имеют объемную уходящую группу в условиях S N 2 или объемный неизвлекаемый заместитель, которые вызывают значительные стерические затруднения, тем самым увеличивая замещение конъюгата. Этот тип реакции называется S N 1 'или S N 2', в зависимости от того, следует ли реакция по S N 1-подобному механизму или S <103.>N 2-подобный механизм. Подобно тому, как существуют аналоги S N 1 'и S N 2' для реакций S N 1 и S N 2 соответственно, также существует аналог для S N i, который представляет собой S N i ', применимый для реакций между аллильными соединениями и реагентами, такими как SOCl 2.
Синтетическое применение может быть расширено до замещений по бутадиену связей:

На первой стадии этой макроциклизации тиольная группа на одном конце 1,5-пентандитиола реагирует с бутадиеновым хвостом в 1 с еноном 2в аллильном сдвиге с сульфоном уходящей группой, которая далее реагирует с другим концом в реакции присоединения конъюгата .
В одном исследовании аллильный сдвиг применялся дважды в кольцевой системе:

В этой последовательности реакций a эпоксидирование Якобсена a связывает эпокси группу с диеном, который служит уходящей группой в реакции с пиразольным нуклеофилом. Второй нуклеофил - это метилмагнийбромид, изгоняющий пиразольную группу.
Реакция S N 2 'должна объяснять результат реакции азиридина, несущего метиленбромидную группу, с метиллитием :
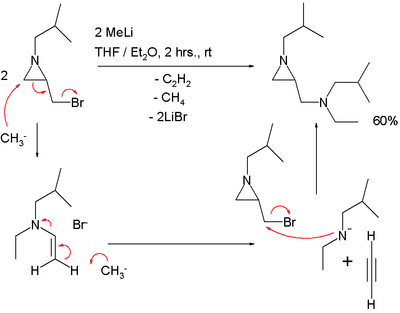
в этой реакции один эквивалент ацетилена потерян.
Примеры аллильных сдвигов:
В одной адаптации, называемой SN2' редукцией a формальное органическое восстановление аллильной группы, содержащей хорошую уходящую группу, сопровождается перегруппировкой. Один пример такой реакции обнаружен как часть полного синтеза таксола (кольцо C):

гидрид представляет собой алюмогидрид лития и уходящая группа соль фосфония. Продукт содержит новую экзоциклическую двойную связь. Только когда кольцо циклогексана правильно замещено, протон будет присоединяться в положении транс по отношению к соседней метильной группе. Концептуально связанной реакцией является реакция Уайтинга с образованием диенов.
Аллильные сдвиги также могут происходить с электрофилами. В приведенном ниже примере карбонильная группа в бензальдегиде активирована дибороновой кислотой перед реакцией с аллиловым спиртом (см.: реакция Принса ):
