 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 8-Метил-8-азабицикло [3.2.1] октан-3-он | |
| Другие названия 3-Тропинон | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.007.756 |
| PubChem CID | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C8H13NO |
| Молярная масса | 139,195 г / моль |
| Внешний вид | Коричневое твердое вещество |
| Точка плавления | 42,5 ° C (108,5 ° F; 315,6 K) |
| Точка кипения | (разлагается) |
| Опасности | |
| NFPA 704 (огненный алмаз) |  1 2 0 1 2 0 |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа | |
| Ссылки на инфобокс | |
Тропинон - это алкалоид, синтезированный в 1917 году Робертом Робинсоном в качестве синтетического предшественника атропина, дефицитного товара во время Первой мировой войны. Тропинон, алкалоиды кокаин и атропин имеют одинаковую структуру ядра тропана. Соответствующий ему конъюгат кислоты при pH 7,3, основной вид известен как тропиниумон.
Первый синтез тропинона был осуществлен Ричардом Вильштеттером в 1901 году. Он начался с, казалось бы, связанного циклогептанон, но для введения азотного мостика потребовалось много стадий; общий выход для пути синтеза составляет только 0,75%. Вильштеттер ранее синтезировал кокаин из тропинона, что было первым синтезом и выяснением структуры кокаина.
 Синтез тропинона Вильштеттером
Синтез тропинона Вильштеттером Синтез Робинсона 1917 года рассматривается классика в тотальном синтезе благодаря своей простоте и биомиметическому подходу. Тропинон представляет собой бициклическую молекулу, но реагенты, используемые при его получении, довольно просты: янтарный альдегид, метиламин и ацетонедикарбоновая кислота. (или даже ацетон ). Синтез является хорошим примером биомиметической реакции или синтеза биогенетического типа, поскольку в биосинтезе используются одни и те же строительные блоки. Он также демонстрирует тандемную реакцию в однореакторном синтезе. Кроме того, выход синтеза составил 17%, а с последующими улучшениями превысил 90%.
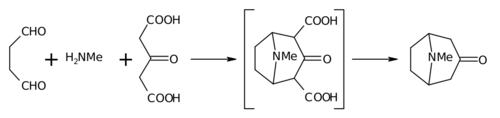
Эта реакция описана как внутримолекулярная «двойная реакция Манниха » по очевидным причинам. В этом отношении он не уникален, так как другие также пытались использовать его в синтезе пиперидина.
Вместо ацетона, ацетонедикарбоновая кислота известна как «синтетический эквивалент » 1,3- Группы дикарбоновой кислоты представляют собой так называемые «активирующие группы » для облегчения реакций образования кольца. Соль кальция присутствует в виде «буфера », поскольку утверждается, что более высокие выходы возможны, если реакция проводится при «физиологическом pH ».
Основными особенностями, очевидными из приведенной ниже последовательности реакций, являются:
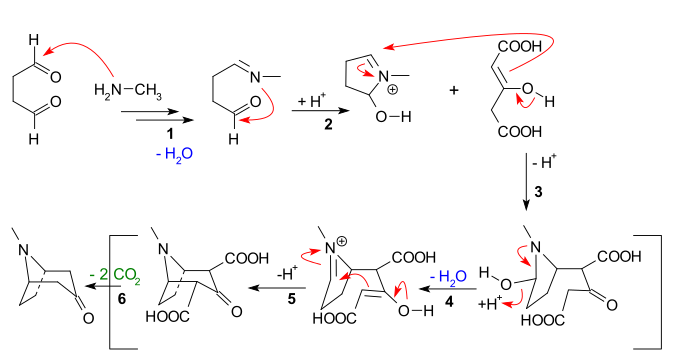
Некоторые авторы фактически пытались сохранить одну из групп CO 2 H.
CO2R-тропинон имеет 4 стереоизомера, хотя соответствующий экгонидин алкиловый эфир имеет только пару энантиомеров.
Снижение уровня тропинона опосредуется НАДФН -зависимыми ферментами редуктазы, которые были охарактеризованы у многих видов растений. Все эти виды растений содержат два типа ферментов редуктазы, тропинонредуктазу I и тропинонредуктазу II. TRI производит тропин, а TRII производит псевдотропин. Из-за различных кинетических характеристик и характеристик pH / активности ферментов, а также из-за более высокой активности TRI в 25 раз по сравнению с TRII, большая часть снижения тропинона происходит за счет TRI с образованием тропина.
 Восстановление тропинона
Восстановление тропинона