 Гексагидропорфин, ядро порфириногенов.
Гексагидропорфин, ядро порфириногенов. В биохимии a порфириноген является членом класса встречающихся в природе соединений с ядром тетрапиррола, макроциклом четырех пиррольных колец, соединенных четырьмя метиленовые мостики. Их можно рассматривать как производные от исходного соединения гексагидропорфина путем замещения различных функциональных групп на атомы водорода во внешнем (20-углеродном) кольце.
Порфириногены представляют собой промежуточные соединения в биосинтезе порфиринов, кофакторов с ядром порфина, которые присутствуют во многих ферментах. и белки, включая миоглобин, гемоглобин, цитохромы и хлорофиллы.
Порфирины отличаются от порфириногенов наличием четырех пиррольных колец, связанных метиновые мостики = CH- вместо метиленовых мостиков -CH. 2-, и из-за отсутствия атома водорода в двух из четырех аминных -NH- групп, превращая их в имины = N−. При биосинтезе порфиринов исходный порфириноген дегидрируется протопорфириногеноксидазой.
Из-за их ограниченной делокализации порфириногены бесцветны. Потеря всех четырех центральных атомов водорода в ядре дает четырехвалентный анион, который может действовать как лиганд для катионов металлов, создавая координационное соединение. Последующие промежуточные продукты биосинтеза на пути к порфиринам сильно окрашены и часто фитотоксичны.
Порфирогены, которые встречаются в живых организмах, обычно имеют боковые цепи, заменяющие некоторые или все атомы водорода в двух крайних углеродных атомах каждого пиррольного кольца (в отличие от атомов водорода в метиленовых мостиках).

Уропорфириноген III, предшественник копропорфириногена III.

копропорфириноген III, предшественник протопорфириногена IX.
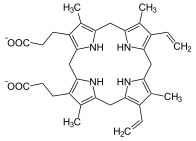
Протопорфириноген IX, предшественник протопорфирина IX.
Были произведены и исследованы в лабораториях различные синтетические порфириногены. Они часто имеют боковые группы, которые не встречаются в природе, и, возможно, у атомов углерода в метиленовых мостиках (мезоположениях) вместо пиррольных колец. Мезозамещенные порфириногены являются промежуточными продуктами так называемых мезозамещенных порфиринов. Окисление превращает центральное гексагидропорфиновое ядро в порфиновое ядро, давая желаемый порфирин.
При кислотном катализе, пиррол и кетоны R- ( C = O) -R 'или альдегиды R- (C = O) -H конденсируются с образованием многих олигомеров, включая циклические [- (CRR') - (C. 4H. 2NH) -]. п \. Затем можно разделить желаемые порфириногены (n = 4). Мезозамещенные порфириногены с восемью неводородными боковыми цепями также называют каликс [4] пирролами. Эти продукты сопротивляются дегидрированию внешнего кольца лучше, чем природные порфириногены.
Например, конденсация с бензальдегидом C. 6H. 5- (C = O) -H дает может быть окислен до мезо-тетрафенилпорфирина. Конденсация с ацетоном H. 3C- (C = O) -CH. 3 дает родительский элемент.
Альтернативно, пиррол с боковыми цепями, замещенными у атомов углерода 3 и 4 (те не примыкающий к азоту) может быть конденсирован с формальдегидом H- (C = O) -H с получением порфириногенов, более близких к природным. Например, получают исходное соединение октаэтилпорфирина.

мезооктаметилпорфириноген (CAS 4475-42-7).