 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Первоначально Алдара. Доступно множество торговых марок. |
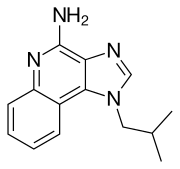
| Другие названия | 1-изобутил-1H-имидазо [4,5-c] хинолин-4-амин |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a698010 |
| Данные лицензии | |
| Беременность. категория |
|
| Способы применения. | Местное |
| Код АТС | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные данные | |
| Период полувыведения | 30 часов (местная доза), 2 часа (подкожная доза) |
| Идентификаторы | |
Название ИЮПАК
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| CompTox Dashboard (EPA ) | |
| ECHA InfoCard | 100.131.047 |
| Химические и физические данные | |
| Формула | C14H16N4 |
| Молярная масса | 240,310 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Имиквимод (INN ) - это рецептурный препарат, который действует как модификатор иммунного ответа, который используется для лечения остроконечных кондилом, поверхностная базальноклеточная карцинома и актинический кератоз. Ученые фармацевтического подразделения 3M обнаружили это лекарство, и в 1997 году компания 3M получила первое одобрение FDA под брендом Aldara . По состоянию на 2015 год имиквимод является универсальным и доступен во всем мире под разными брендами.
Имиквимод представляет собой крем, который назначают пациенту для лечения остроконечных кондилом, болезни Боуэнса (плоскоклеточный рак in situ) и вторичного по отношению к хирургическое лечение базальноклеточного рака, а также актинического кератоза.
Крем Имиквимод 5% показан для местного лечения:
Крем Имиквимод 3,75% показан для местного лечения клинически типичный негиперкератотический, негипертрофический, видимый или пальпируемый актинический кератоз всего лица или облысения кожи головы у иммунокомпетентных взрослых, когда другие варианты местного лечения противопоказаны или менее подходят.
Побочные эффекты включают местные воспалительные реакции, такие как волдыри, ощущение жжения, покраснение кожи, сухость кожи, зуд, разрушение кожи, образование корок или струпьев на коже, дренаж кожи, шелушение или шелушение кожи, изъязвление кожи, язвы, отек, а также системные реакции, такие как лихорадка, симптомы гриппа, головная боль и усталость.
Людям, перенесшим трансплантацию органов и принимающим иммунодепрессанты, не следует использовать имиквимод.
Имиквимод проявляет выраженную противоопухолевую активность за счет синергетического воздействия на несколько иммунологических уровней. Имиквимод стимулирует врожденную иммунную систему, активируя толл-подобный рецептор 7 (TLR7), обычно участвующий в распознавании патогенов. Клетки, активированные имиквимодом через TLR-7, секретируют цитокины (в первую очередь интерферон-α (IFN-α), интерлейкин-6 (IL-6) и фактор некроза опухоли-α (TNF-α)). Имеются данные о том, что имиквимод при нанесении на кожу может приводить к активации клеток Лангерганса, которые впоследствии мигрируют в местные лимфатические узлы, чтобы активировать адаптивную иммунную систему. Другие типы клеток, активируемые имиквимодом, включают естественные клетки-киллеры, макрофаги и B-лимфоциты.
. Имиквимод проявляет свое действие за счет увеличения уровней рецептора опиоидного фактора роста. (OGFr). В экспериментах блокирование функции OGFr с помощью технологии siRNA привело к потере любого антипролиферативного эффекта имиквимода.
 Спектр ЯМР Имиквимода
Спектр ЯМР Имиквимода Ученые фармацевтического подразделения 3M обнаружили имиквимод как часть программы по обнаружению ингибиторов репликации вируса простого герпеса на основе известного производного аденина. Компания 3M получила первое одобрение FDA в 1997 году как средство для лечения наружных генитальных и перианальных бородавок под торговой маркой «Aldara». В 2004 году 3M получила одобрение FDA на продажу имиквимода для лечения поверхностной базально-клеточной карциномы.
. В 2006 году 3M продала свой фармацевтический бизнес в Северной и Южной Америке компании Graceway Pharmaceuticals, своему европейскому фармацевтическому бизнесу. Meda AB и ее фармацевтический бизнес на других территориях двум частным акционерным компаниям.
Graceway объявила о банкротстве в 2011 году после истечения срока действия патентов на имиквимод, и его активы, включая права на брендинг имиквимода и разрешения на него в Северной и Южной Америке, были приобретены Medicis Pharmaceutical.
Имиквимод 5% был одобрен для медицинского использования в Европейском Союзе в сентябре 1998 года. Имиквимод 3,75% был одобрен для медицинского использования в Европейском Союзе в августе 2012 года.
По состоянию на 2015 год имиквимод является дженериком и доступен во всем мире под многими торговыми марками.
Одно рандомизированное двойное слепое клиническое исследование фазы III исследование показало, что устранение остроконечных кондилом (показание, одобренное FDA) улучшилось уменьшилось с 9% при применении плацебо до 24,9% при применении крема с 3,75% имиквимодом на срок до восьми недель.
Имиквимод был протестирован для лечения контагиозного моллюска. Однако в двух крупных рандомизированных контролируемых испытаниях не было обнаружено доказательств эффективности имиквимода при лечении детей с контагиозным моллюском, а также отмечены побочные эффекты. Это опровергает более ранние анекдотические утверждения и меньшие, менее надежные исследования.
Имиквимод также был протестирован для лечения внутриэпителиальной неоплазии вульвы, вагинальной интраэпителиальной неоплазии, часто бородавки (Кокрановский обзор 2012 г. не выявил рандомизированных контролируемых испытаний), подошвенные бородавки, бородавки у людей с подавленной иммунной системой, плоские бородавки на лице и шее, а также бородавки под ногтями и ногтями на руках и ногах и вокруг них. По состоянию на 2014 г. недостаточно данных, чтобы рекомендовать лечение бородавок (кроме остроконечных кондилом) имиквимодом из-за небольшого размера и отсутствия средств контроля в существующих исследованиях.
.