A дегидрогеназа (также называется DH или DHase в литературе) представляет собой фермент, принадлежащий к группе оксидоредуктаз, который окисляет субстрат за счет восстановления акцептора электронов, обычно NAD / NADP или флавин кофермент, такой как FAD или FMN. Они также катализируют обратную реакцию, например, алкогольдегидрогеназа не только окисляет этанол до ацетальдегид у животных, но также производит этанол из ацетальдегида в дрожжах.
Дегидрогеназы являются подклассом из класса ферментов, называемых «оксидоредуктазами». Оксидоредуктазы, как правило, катализируют реакции окисления и восстановления. Эти ферменты делятся на шесть категорий: оксигеназы, редуктазы, пероксидазы, оксидазы, гидроксилазы и дегидрогеназы. Большинство ферментов оксидоредуктазы являются дегидрогеназами, хотя редуктазы также встречаются часто. Принятая номенклатура дегидрогеназ - «донорная дегидрогеназа», где донором является субстрат, который может окисляться.
Реакции окисления-восстановления необходимы для роста и выживания организмов, поскольку окисление органических молекул производит энергию. Энергетические реакции могут стимулировать синтез важных энергетических молекул, таких как АТФ, в гликолизе. По этой причине дегидрогеназы играют ключевую роль в метаболизме.
Дегидрогеназы окисляют субстрат путем переноса водорода на акцептор электронов, при этом общие акцепторы электронов NAD или FAD. Это можно рассматривать как окисление субстрата, при котором субстрат либо теряет атомы водорода, либо получает атом кислорода (из воды). Название «дегидрогеназа» основано на идее, что она способствует удалению (де-) водорода (-водород-) и является ферментом (-аза). Реакции дегидрогеназы обычно протекают в двух формах: перенос гидрида и высвобождение протона (часто с водой в качестве второго реагента) и перенос двух атомов водорода.
Иногда реакция, катализируемая дегидрогеназой, будет выглядеть так: AH + B ↔ A + BH, когда переносится гидрид.
 Алкогольдегидрогеназа окисляет этанол с помощью электронного носителя НАД, образуя ацетальдегид.
Алкогольдегидрогеназа окисляет этанол с помощью электронного носителя НАД, образуя ацетальдегид. А представляет собой субстрат, который будет окисляться, а В является акцептором гидрида. Обратите внимание, как когда гидрид переносится от A к B, A принимает положительный заряд; это потому, что фермент взял два электрона от субстрата, чтобы восстановить акцептор до BH.
Результатом реакции, катализируемой дегидрогеназой, не всегда является получение положительного заряда. Иногда субстрат теряет протон. Это может оставить свободные электроны на подложке, которые переходят в двойную связь. Это часто случается, когда субстратом является спирт; когда протон на кислороде уходит, свободные электроны на кислороде будут использоваться для создания двойной связи, как видно из окисления этанола до ацетальдегида, осуществляемого алкогольдегидрогеназой на изображении справа.
Другая возможность заключается в том, что молекула воды вступит в реакцию, внося вклад гидроксид-ион в субстрат и протон в окружающую среду. Конечный результат на подложке - добавление одного атома кислорода. Это видно, например, в окислении ацетальдегида до уксусной кислоты с помощью ацетальдегиддегидрогеназы, стадии метаболизма этанола и производства уксуса.
 Реакция, катализируемая сукцинатдегидрогеназой, обратите внимание на двойную связь, образованную между двумя центральными атомами углерода при удалении двух атомов водорода.
Реакция, катализируемая сукцинатдегидрогеназой, обратите внимание на двойную связь, образованную между двумя центральными атомами углерода при удалении двух атомов водорода. В приведенном выше случае дегидрогеназа перенесла гидрид, высвобождая протон, H, но дегидрогеназы могут также переносить два атома водорода, используя FAD в качестве акцептора электронов. Это было бы обозначено как AH 2 + B ↔ A + BH 2. Двойная связь обычно образуется между двумя атомами, из которых взяты атомы водорода, как в случае сукцинатдегидрогеназы. Два атома водорода были перенесены на носитель или другой продукт вместе со своими электронами.
Различие между подклассами оксидоредуктаз, катализирующих реакции окисления, заключается в их акцепторах электронов.
 Реакция, катализируемая оксидазой, обратите внимание на восстановление кислорода как электрона акцептор
Реакция, катализируемая оксидазой, обратите внимание на восстановление кислорода как электрона акцептор дегидрогеназа и оксидаза легко различимы, если рассматривать акцептор электронов. Оксидаза также удаляет электроны с подложки, но использует только кислород в качестве акцептора электронов. Одна из таких реакций: AH 2 + O 2 ↔ A + H 2O2.
Иногда оксидазная реакция будет выглядеть так: 4A + 4H + O 2 ↔ 4A + 2H 2 O. В этом случае фермент забирает электроны у субстрата и использует свободные протоны для восстановления кислорода, оставляя субстрат с положительным зарядом. Продукт представляет собой воду, а не перекись водорода, как показано выше. Примером оксидазы, которая функционирует подобным образом, является комплекс IV в цепи переноса электронов (ETC ).
Обратите внимание, что оксидазы обычно переносят эквивалент дигидрогена (H 2), а акцептором является Аналогично, пероксидаза (другой подкласс оксидоредуктаз) будет использовать пероксид (H 2O2) в качестве акцептора электронов, а не кислород.
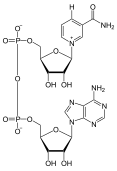 Никотинамид Адениндинуклеотид
Никотинамид Адениндинуклеотид Ферменты дегидрогеназы переносят электроны от субстрата к носителю электронов; какой носитель используется, зависит от протекающей реакции. Обычными акцепторами электронов, используемыми в этом подклассе, являются НАД, ФАД и НАДФ. В этом процессе переносчики электронов восстанавливаются и считаются окислителями субстрата. Носителями электронов являются коферменты, которые часто называют «окислительно-восстановительными кофакторами».
НАД или никотинамидадениндинуклеотид, представляет собой динуклеотид, содержащий два нуклеотида. Один из нуклеотидов, который он содержит, является аденином группа, а другая - никотинамид. Чтобы восстановить эту молекулу, к 6-углеродному кольцу никотинамида необходимо добавить водород и два электрона; один электрон добавляется к углероду напротив положительно заряженного азота, вызывая перегруппировку связей внутри кольца, чтобы дать азоту больше электронов; в результате он потеряет свой положительный заряд. Другой электрон «украден» у дополнительного водорода, оставляя ион водорода в растворе.
Восстановление НАД: НАД + 2H + 2e ↔ НАДН + H
НАД в основном используется в катаболических путях, например гликолиз, который разрушает энергетические молекулы с образованием АТФ. Отношение НАД к НАДН в клетке поддерживается на очень высоком уровне, что делает его доступным для использования в качестве окислителя.
 Никотинамид-аденозиндинуклеотидфосфат
Никотинамид-аденозиндинуклеотидфосфат НАДФ отличается от НАД только добавлением фосфатной группы к 5-членному углеродному кольцу аденозина. Добавление фосфата не изменяет способность переносчика электронов к переносу. Фосфатная группа создает достаточный контраст между двумя группами, которые они связывают с активным центром разных ферментов, обычно катализируя различные типы реакций.
Эти два переносчика электронов легко различимы ферментами и участвуют в очень разных реакциях. НАДФ в основном функционирует с ферментами, которые катализируют анаболические или биосинтетические пути. В частности, НАДФН будет действовать как восстанавливающий агент в этих реакциях, приводя к НАДФ. Это пути преобразования субстратов в более сложные продукты с использованием АТФ. Причина наличия двух отдельных переносчиков электронов для анаболических и катаболических путей связана с регуляцией метаболизма. Отношение НАДФ к НАДФН в клетке поддерживается на довольно низком уровне, так что НАДФН легко доступен в качестве восстановителя; он чаще используется в качестве восстанавливающего агента, чем НАДФ в качестве окислителя.
 Флавин-адениндинуклеотид
Флавин-адениндинуклеотид FAD, или флавинадениндинуклеотид, представляет собой простетическую группу (a (неполипептидная единица, связанная с белком, который необходим для функционирования), который состоит из аденинового нуклеотида и флавинмононуклеотида. ФАД - уникальный акцептор электронов. Его полностью восстановленная форма - это FADH 2 (известная как форма гидрохинона), но FAD также может быть частично окислен как FADH либо путем восстановления FAD, либо путем окисления FADH 2. Дегидрогеназы обычно полностью восстанавливают FAD до FADH 2. Производство FADH редко.
Атомы азота с двойной связью в FAD делают его хорошим акцептором при отборе двух атомов водорода от подложки. Поскольку для этого требуется два атома, а не один, FAD часто участвует в образовании двойной связи во вновь окисленном субстрате. FAD уникален, потому что он восстанавливается двумя электронами и двумя протонами, в отличие от NAD и NADP, которые принимают только один протон.
 Механизм альдегиддегидрогеназы, обратите внимание на использование НАД в качестве акцептора электронов.
Механизм альдегиддегидрогеназы, обратите внимание на использование НАД в качестве акцептора электронов. Альдегиды являются естественным побочным продуктом многих физиологических процессов, а также являясь следствием многих промышленных процессов, выбрасывается в окружающую среду в виде смога и выхлопных газов автомобилей. Накопление альдегидов в головном мозге и перикарде может быть вредным для здоровья человека, поскольку они могут образовывать аддукты с важными молекулами и вызывать их инактивацию.
Учитывая, насколько распространены альдегиды, необходим фермент, способствующий развитию их окисление до менее летучих соединений. Альдегиддегидрогеназы (ALDH) - это НАД-зависимые ферменты, которые действуют для удаления токсичных альдегидов из организма и действуют в основном в митохондриях клеток. Эти ферменты в значительной степени ответственны за детоксикацию ацетилальдегида, который является промежуточным звеном в метаболизме этанола. Было показано, что мутация в гене ALDH2 (один из 19 генов альдегиддегидрогеназы) является причиной частого появления у населения Восточной Азии покраснения лица после употребления алкоголя из-за накопления ацетальдегида. Это накопление ацетальдегида также вызывает головные боли и рвоту (симптомы похмелья ), если оно не распадается достаточно быстро, что является еще одной причиной плохой реакции на алкоголь у людей с дефицитом ацетальдегида DH. Важно отметить, что недостаток этого фермента был связан с увеличением риска инфаркта миокарда, в то время как активация показала способность фермента уменьшать повреждения, вызванные ишемией.
. Деактивация альдегиддегидрогеназ имеет было показано, что он играет важную роль в механизмах многих видов рака. ALDH участвуют в дифференцировке, пролиферации, окислении клеток и устойчивости к лекарствам. Эти ферменты являются лишь одним из множества различных типов дегидрогеназ в организме человека; их широкий спектр функций и влияние, которое их деактивация или мутации оказывают на важнейшие клеточные процессы, подчеркивают важность всех дегидрогеназ в поддержании гомеостаза организма.
цикл TCA примеры: