| Алкогольдегидрогеназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
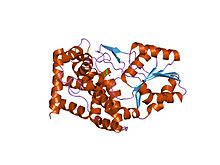
 Кристаллографическая структура гомодимера ADH5 человека. Кристаллографическая структура гомодимера ADH5 человека. | |||||||||
| Идентификаторы | |||||||||
| ЕС нет. | 1.1.1.1 | ||||||||
| № CAS | 9031-72-5 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
Алкогольдегидрогеназы ( ADH) ( EC 1.1.1.1 ) представляют собой группу ферментов дегидрогеназ, которые встречаются во многих организмах и способствуют взаимному превращению спиртов и альдегидов или кетонов с восстановлением никотинамидадениндинуклеотида (NAD +) до NADH. У людей и многих других животных они служат для расщепления токсичных спиртов, а также участвуют в образовании полезных альдегидных, кетоновых или спиртовых групп во время биосинтеза различных метаболитов. В дрожжах, растениях и многих бактериях некоторые алкогольдегидрогеназы катализируют противоположную реакцию как часть ферментации, чтобы обеспечить постоянное поступление НАД +.
Генетические данные, полученные при сравнении нескольких организмов, показали, что глутатион- зависимая формальдегиддегидрогеназа, идентичная алкогольдегидрогеназе класса III (ADH-3 / ADH5), предположительно является предковым ферментом для всего семейства ADH. На раннем этапе эволюции важен был эффективный метод устранения как эндогенного, так и экзогенного формальдегида, и эта способность сохраняла предковый ADH-3 с течением времени. Дупликация гена ADH-3, за которой последовала серия мутаций, привела к развитию других ADH.
Считается, что способность производить этанол из сахара (который лежит в основе производства алкогольных напитков) изначально возникла у дрожжей. Хотя эта функция не является адаптивной с энергетической точки зрения, производя алкоголь в таких высоких концентрациях, чтобы они были токсичными для других организмов, дрожжевые клетки могли бы эффективно устранить их конкуренцию. Поскольку гниющие плоды могут содержать более 4% этанола, животным, поедающим эти плоды, необходима система для метаболизма экзогенного этанола. Считалось, что это объясняет сохранение активного в этаноле ADH у видов, отличных от дрожжей, хотя в настоящее время известно, что ADH-3 также играет важную роль в передаче сигналов оксида азота.
У людей секвенирование гена ADH1B (ответственного за продукцию полипептида алкогольдегидрогеназы) показывает несколько функциональных вариантов. В одном есть SNP (однонуклеотидный полиморфизм), который приводит к остатку гистидина или аргинина в положении 47 зрелого полипептида. В варианте гистидина фермент гораздо более эффективен при вышеупомянутом превращении. Однако фермент, ответственный за превращение ацетальдегида в ацетат, остается неизменным, что приводит к разным скоростям катализа субстрата и вызывает накопление токсичного ацетальдегида, вызывая повреждение клеток. Это обеспечивает некоторую защиту от чрезмерного употребления алкоголя и алкогольной зависимости (алкоголизма). Различные гаплотипы, возникающие в результате этой мутации, более сконцентрированы в регионах недалеко от Восточного Китая, регионе, также известном своей низкой толерантностью к алкоголю и зависимостью.
Было проведено исследование, чтобы найти корреляцию между распределением аллелей и алкоголизмом, и результаты показывают, что распределение аллелей возникло вместе с выращиванием риса в регионе между 12000 и 6000 лет назад. В регионах, где выращивался рис, его также ферментировали до этанола. Это привело к предположению, что увеличение доступности алкоголя привело к алкоголизму и злоупотреблению, что привело к снижению репродуктивной способности. Люди с вариантным аллелем плохо переносят алкоголь, что снижает вероятность зависимости и злоупотребления. Гипотеза утверждает, что люди с ферментом гистидинового варианта были достаточно чувствительны к воздействию алкоголя, что привело к дифференцированному репродуктивному успеху и соответствующие аллели передавались из поколения в поколение. Классическая дарвиновская эволюция будет действовать для отбора против вредной формы фермента (вариант Arg) из-за снижения репродуктивного успеха индивидуумов, несущих аллель. Результатом будет более высокая частота аллеля, ответственного за His-вариант фермента в областях, которые дольше всего находились под давлением отбора. Распространение и частота His-варианта следует за распространением выращивания риса во внутренних регионах Азии, с более высокими частотами His-варианта в регионах, где рис возделывается дольше всех. Таким образом, географическое распределение аллелей, по-видимому, является результатом естественного отбора против индивидуумов с более низким репродуктивным успехом, а именно тех, которые несли аллель варианта Arg и были более восприимчивы к алкоголизму. Однако сохранение варианта Arg в других популяциях свидетельствует о том, что эффект не может быть сильным.
 Лошадь LADH (алкогольдегидрогеназа печени)
Лошадь LADH (алкогольдегидрогеназа печени) Первая в истории выделенная алкогольдегидрогеназа (АДГ) была выделена в 1937 году из Saccharomyces cerevisiae (пивных дрожжей). Многие аспекты каталитического механизма фермента АДГ в печени лошади были исследованы Хьюго Теореллом и соавторами. АДГ был также одним из первых олигомерных ферментов, у которых была определена его аминокислотная последовательность и трехмерная структура.
В начале 1960 года он был обнаружен у плодовых мух рода Drosophila.
Алкогольдегидрогеназы включают группу из нескольких изоферментов, которые катализируют окисление первичных и вторичных спиртов до альдегидов и кетонов соответственно, а также могут катализировать обратную реакцию. У млекопитающих это окислительно- восстановительная реакция ( окислительно- восстановительная) с участием кофермента никотинамида адениндинуклеотида (НАД +).
Механизм у дрожжей и бактерий противоположен этой реакции. Эти шаги поддерживаются кинетическими исследованиями.
Субстрат координирован с цинком, и этот фермент имеет два атома цинка на субъединицу. Один из них - это активный центр, который участвует в катализе. В активном центре лиганды представляют собой Cys-46, Cys-174, His-67 и одну молекулу воды. Другая субъединица связана со структурой. По этому механизму гидрид спирта переходит в НАД +. Кристаллические структуры показывают, что His-51 депротонирует никотинамид рибозу, которая депротонирует Ser-48. Наконец, Ser-48 депротонирует спирт, превращая его в альдегид. С механистической точки зрения, если фермент добавляет гидрид к поверхности NAD +, образующийся водород включается в положение pro-R. Ферменты, которые добавляют гидрид к поверхности, считаются дегидрогеназами класса А.
 Активный центр алкогольдегидрогеназы
Активный центр алкогольдегидрогеназы Активный сайт человеческого ADH1 (PDB: 1HSO) состоит из атома цинка, His-67, Cys-174, Cys-46, Thr-48, His-51, Ile-269, Val-292, Ala-317 и Phe-319. В обычно исследуемой изоформе печени лошади Thr-48 представляет собой Ser, а Leu-319 представляет собой Phe. Цинк координирует субстрат (спирт). Цинк координируется Cys-46, Cys-174 и His-67. Leu-319, Ala-317, His-51, Ile-269 и Val-292 стабилизируют НАД +, образуя водородные связи. His-51 и Ile-269 образуют водородные связи со спиртами на никотинамид-рибозе. Phe-319, Ala-317 и Val-292 образуют водородные связи с амидом на NAD +.
 Структурный цинк-связывающий мотив в алкогольдегидрогеназе из МД-моделирования
Структурный цинк-связывающий мотив в алкогольдегидрогеназе из МД-моделирования Алкогольдегидрогеназы млекопитающих также имеют структурный участок цинка. Этот ион Zn играет структурную роль и имеет решающее значение для стабильности белка. Структуры каталитических и структурных центров цинка в алкогольдегидрогеназе печени лошади (HLADH), выявленные в кристаллографических структурах, были изучены вычислительными методами квантовой химии, а также методами классической молекулярной динамики. Структурный сайт цинка состоит из четырех близко расположенных цистеиновых лигандов (Cys97, Cys100, Cys103 и Cys111 в аминокислотной последовательности), расположенных в почти симметричном тетраэдре вокруг иона Zn. Недавнее исследование показало, что взаимодействие между цинком и цистеином регулируется в первую очередь электростатическим вкладом с дополнительным ковалентным вкладом в связывание.
У человека ADH существует во многих формах в виде димера и кодируется по крайней мере семью различными генами. Существует пять классов (IV) алкогольдегидрогеназы, но печеночные формы, которые используются в основном у людей, относятся к классу 1. Класс 1 состоит из субъединиц α, β и γ, которые кодируются генами ADH1A, ADH1B и ADH1C. Фермент присутствует в больших количествах в печени и слизистой оболочке желудка. Это катализирует окисление из этанола до ацетальдегида (этаналя):
Это позволяет употреблять алкогольные напитки, но его эволюционная цель, вероятно, заключается в расщеплении спиртов, естественным образом содержащихся в пищевых продуктах или производимых бактериями в пищеварительном тракте.
Другой эволюционной целью может быть метаболизм эндогенного алкогольного витамина А ( ретинола ), который генерирует гормон ретиноевую кислоту, хотя его функция может заключаться в первую очередь в устранении токсичных уровней ретинола.
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Алкогольдегидрогеназа также участвует в токсичности других типов алкоголя: например, она окисляет метанол с образованием формальдегида и, в конечном итоге, муравьиной кислоты. У людей по крайней мере шесть слегка различающихся алкогольдегидрогеназ. Каждый из них является димером (т.е. состоит из двух полипептидов ), причем каждый димер содержит два иона цинка Zn 2+. Один из этих ионов имеет решающее значение для работы фермента: он расположен в каталитическом центре и удерживает гидроксильную группу спирта на месте.
Активность алкогольдегидрогеназы варьируется между мужчинами и женщинами, между молодыми и старыми, а также среди населения из разных регионов мира. Например, молодые женщины не могут перерабатывать алкоголь с той же скоростью, что и молодые мужчины, потому что они не имеют такой высокой экспрессии алкогольдегидрогеназы, хотя обратное верно для людей среднего возраста. Уровень активности может зависеть не только от уровня экспрессии, но и от аллельного разнообразия в популяции.
Гены человека, кодирующие алкогольдегидрогеназы класса II, III, IV и V, - это ADH4, ADH5, ADH7 и ADH6 соответственно.
В отличие от людей дрожжи и бактерии (за исключением молочнокислых бактерий и кишечной палочки в определенных условиях) не ферментируют глюкозу до лактата. Вместо этого они сбраживают его до этанола и CO. 2. Общую реакцию можно увидеть ниже:
 Алкогольдегидрогеназа
Алкогольдегидрогеназа У дрожжей и многих бактерий алкогольдегидрогеназа играет важную роль в ферментации: пируват, образующийся в результате гликолиза, превращается в ацетальдегид и диоксид углерода, а ацетальдегид затем восстанавливается до этанола алкогольдегидрогеназой, называемой ADH1. Целью этой последней стадии является регенерация NAD +, чтобы мог продолжаться генерирующий энергию гликолиз. Люди используют этот процесс для производства алкогольных напитков, позволяя дрожжам сбраживать различные фрукты или зерна. Дрожжи могут производить и потреблять собственный алкоголь.
Основная алкогольдегидрогеназа у дрожжей больше, чем у человека, и состоит из четырех, а не двух субъединиц. Он также содержит цинк на его каталитическом сайте. Вместе с цинксодержащими алкогольдегидрогеназами животных и человека эти ферменты дрожжей и многих бактерий образуют семейство «длинноцепочечных» алкогольдегидрогеназ.
У пивных дрожжей также есть другая алкогольдегидрогеназа, ADH2, которая произошла из дублированной версии хромосомы, содержащей ген ADH1. ADH2 используется дрожжами для обратного превращения этанола в ацетальдегид, и он выражается только при низкой концентрации сахара. Наличие этих двух ферментов позволяет дрожжам производить алкоголь, когда сахара в изобилии (и этот спирт затем убивает конкурирующие микробы), а затем продолжать окисление спирта, когда сахар и конкуренция исчезают.
У растений АДГ катализирует ту же реакцию, что и у дрожжей и бактерий, обеспечивая постоянное поступление НАД +. Кукуруза имеет две версии ADH - ADH1 и ADH2, Arabidopsis thaliana содержит только один ген ADH. Структура ADH арабидопсиса консервативна на 47% по сравнению с ADH из печени лошади. Однако структурно и функционально важные остатки, такие как семь остатков, которые обеспечивают лиганды для каталитических и некаталитических атомов цинка, являются консервативными, что позволяет предположить, что ферменты имеют аналогичную структуру. АДГ конститутивно экспрессируется на низких уровнях в корнях молодых растений, выращенных на агаре. Если корням не хватает кислорода, экспрессия АДГ значительно увеличивается. Его экспрессия также увеличивается в ответ на обезвоживание, низкие температуры и абсцизовую кислоту, и он играет важную роль в созревании плодов, развитии проростков и пыльцы. Различия в последовательностях АДГ у разных видов были использованы для создания филогении, показывающей, насколько тесно связаны разные виды растений. Это идеальный ген для использования благодаря его удобному размеру (длина 2–3 т.п.н. с последовательностью, кодирующей ≈1000 нуклеотидов) и низкому количеству копий.
| Железосодержащая алкогольдегидрогеназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 комплекс глицериндегидрогеназы bacillus stearothermophilus с глицерином комплекс глицериндегидрогеназы bacillus stearothermophilus с глицерином | |||||||||
| Идентификаторы | |||||||||
| Условное обозначение | Fe-ADH | ||||||||
| Pfam | PF00465 | ||||||||
| Клан пфам | CL0224 | ||||||||
| ИнтерПро | IPR001670 | ||||||||
| ПРОФИЛЬ | PDOC00059 | ||||||||
| SCOP2 | 1jqa / SCOPe / SUPFAM | ||||||||
| |||||||||
Третье семейство алкогольдегидрогеназ, не связанное с двумя вышеупомянутыми, представляет собой железосодержащие. Они встречаются у бактерий и грибов. По сравнению с ферментами вышеуказанных семейств, эти ферменты чувствительны к кислороду. Члены семейства железосодержащих алкогольдегидрогеназ включают:
Другой класс алкогольдегидрогеназ относится к хиноферментам и требует хиноидных кофакторов (например, пирролохинолинхинона, PQQ) в качестве связанных с ферментом акцепторов электронов. Типичным примером этого типа ферментов является метанолдегидрогеназа метилотрофных бактерий.
При биотрансформации алкогольдегидрогеназы часто используют для синтеза энантиомерно чистых стереоизомеров хиральных спиртов. Часто может быть достигнута высокая химио- и энантиоселективность. Одним из примеров является алкогольдегидрогеназа из Lactobacillus brevis ( Lb ADH), которая описывается как универсальный биокатализатор. Высокая хемоспецифичность была подтверждена также в случае субстратов, представляющих два потенциальных окислительно-восстановительных центра. Например, коричный альдегид представляет собой как алифатическую двойную связь, так и альдегидную функцию. В отличие от обычных катализаторов алкогольдегидрогеназы способны избирательно воздействовать только на последние, давая исключительно коричный спирт.
В топливных элементах алкогольдегидрогеназы могут использоваться для катализа разложения топлива для топливного элемента на основе этанола. Ученые в Университете Сент - Луиса использовали углерода при поддержке дегидрогеназы спирта с поли ( метиленового зеленого цвета ) в качестве анода, с нафионовую мембраны, чтобы достигнуть приблизительно 50 μ / см 2.
В 1949 г. Э. Ракер определил одну единицу активности алкогольдегидрогеназы как количество, которое вызывает изменение оптической плотности на 0,001 в минуту при стандартных условиях анализа. В последнее время международное определение ферментативной единицы (ЕС) стало более распространенным: одна единица алкогольдегидрогеназы преобразует 1,0 мкмоль этанола в ацетальдегид в минуту при pH 8,8 при 25 ° C.
Были исследования, показывающие, что вариации АДГ, влияющие на метаболизм этанола, влияют на риск алкогольной зависимости. Самый сильный эффект обусловлен вариациями ADH1B, которые увеличивают скорость превращения спирта в ацетальдегид. Один такой вариант чаще всего встречается у людей из Восточной Азии и Ближнего Востока, другой - у выходцев из Африки. Оба варианта снижают риск алкоголизма, но, несмотря на это, люди могут стать алкоголиками. Исследователи предварительно обнаружили несколько других генов, связанных с алкоголизмом, и знают, что их еще предстоит найти. Исследования продолжаются с целью выявления генов и их влияния на алкоголизм.
Наркозависимость - еще одна проблема, связанная с ADH, которая, по мнению исследователей, может быть связана с алкоголизмом. Одно конкретное исследование предполагает, что с лекарственной зависимостью связаны семь генов АДГ, однако необходимы дополнительные исследования. Алкогольная и другая наркотическая зависимость могут иметь общие факторы риска, но поскольку алкогольная зависимость часто сопровождается другими наркотическими зависимостями, связь АДГ с другими наркотическими зависимостями не может быть причинной.
Фомепизол, препарат, который конкурентно ингибирует алкогольдегидрогеназу, может использоваться при острой токсичности метанола или этиленгликоля. Это предотвращает превращение метанола или этиленгликоля в его токсичные метаболиты (например, муравьиную кислоту, формальдегид или гликолят ). Такой же эффект иногда достигается и с этанолом, опять же путем конкурентного ингибирования АДГ.
Препарат гидроксизин расщепляется на его активный метаболит цетиризин алкогольдегидрогеназой. Другие препараты с алкогольными группами могут метаболизироваться аналогичным образом, если стерические препятствия не препятствуют проникновению алкоголя в активный центр.