Кумоловый процесс (кумено-фенольный процесс, Хокковый процесс ) представляет собой промышленный процесс синтеза фенола и ацетона из бензола и пропилена. Термин происходит от кумола (изопропилбензол), промежуточного материала в процессе. Он был изобретен Р. Эдрисом и П. Сергеевым в 1942 г. (СССР) и независимо Генрихом Хоком в 1944 г.
В этом процессе преобразуются два относительно дешевых исходных материала, бензол и пропилен, на два более ценных: фенол и ацетон. Другими необходимыми реагентами являются кислород из воздуха и небольшие количества радикального инициатора. Большая часть мирового производства фенола и ацетона в настоящее время основана на этом методе. В 2003 году с помощью кумольного процесса было произведено около 7 миллионов тонн фенола. Для того, чтобы этот процесс был экономичным, также должен существовать спрос на побочный продукт ацетон, а также на фенол.

Кумол образуется в газовой фазе алкилирования Фриделя – Крафтса бензола пропиленом. Бензол и пропилен сжимают вместе до давления 30 стандартных атмосфер при 250 ° C в присутствии каталитической кислоты Льюиса. Фосфорная кислота часто предпочтительнее галогенидов алюминия . Кумол окисляется на воздухе, который удаляет третичный бензильный водород из кумола и, следовательно, образует кумольный радикал :
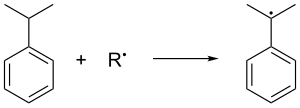
Затем кумольный радикал связывается с молекулой кислорода с образованием кумола. пероксидный радикал, который, в свою очередь, образует гидропероксид кумола (C6H5C (CH 3)2O2H), отщепляя бензиловый водород от другой молекулы кумола. Этот последний кумол превращается в кумольный радикал и возвращается в последующие цепные образования гидропероксидов кумола. Давление 5 атм используется для обеспечения того, чтобы нестабильный пероксид оставался в жидком состоянии.
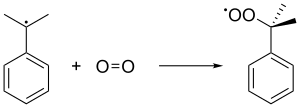

Гидропероксид кумола затем гидролизуют в кислой среде (перегруппировка Хока ) с получением фенола и ацетона. На первом этапе протонируется концевой гидроперокси-атом кислорода. За этим следует стадия, на которой фенильная группа мигрирует от бензильного углерода к соседнему кислороду, и молекула воды теряется, образуя резонансный стабилизированный третичный карбокатион. Согласованный механизм этой стадии аналогичен механизмам окисления Байера-Виллигера, а также стадии окисления гидроборирования-окисления. В 2009 году подкисленная бентонитовая глина оказалась более экономичным катализатором, чем серная кислота в качестве кислой среды.

Как показано ниже, образующийся карбокатион затем подвергается атаке воды, затем протон переносится от гидрокси-кислорода к эфирному кислороду, и, наконец, ион распадается на фенол и ацетон.
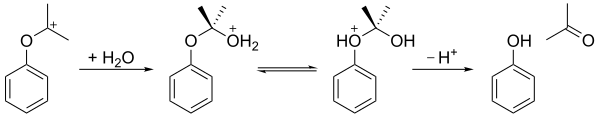
Циклогексилбензол может заменить изопропилбензол. Посредством перегруппировки Хока гидропероксид циклогексилбензола расщепляется с образованием фенола и циклогексанона. Циклогексанон является важным предшественником некоторых нейлонов.
. Начиная с алкилирования бензола смесью 1 и 2-бутенов, в процессе кумола получают фенол и бутаноны.
| На Викискладе есть средства массовой информации, связанные с процессом Кумола. |