 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Tracleer, Stayveer |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a605001 |
| Данные лицензии | |
| Беременность. категория |
|
| Способы введения. | перорально |
| ATC код | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | 50% |
| Связывание с белками | >98% |
| Метаболизм | Печень |
| Выведение период полураспада | 5 часов |
| Идентификаторы | |
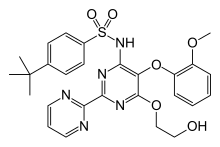
Название ИЮПАК
| |
| CA Номер S | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| Панель управления CompTox (EPA ) | |
| ECHA InfoCard | 100.171.206 |
| Химические и физические данные | |
| Формула | C27H29N5O6S |
| Молярная масса | 551,62 г · моль |
| 3D модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
| (что это?) | |
Бозентан, продается под торговой маркой Tracleer, среди прочего, представляет собой двойной антагонист рецепторов эндотелина препарат, используемый для лечения гипертензии легочной артерии (ПАУ).
Бозентан выпускается в виде таблеток с пленочным покрытием (62,5 или 125 мг) или диспергируемых таблеток для пероральной суспензии (32 мг).
Бозентан используется для лечения людей с умеренной легочной артериальной гипертензией и для уменьшения количества пальцевых язв - открытых ран, особенно на кончиках пальцев, и реже на суставах пальцев - у людей. с системной склеродермией.
Бозентан причиняет вред плоду, и беременным женщинам запрещается его принимать, а женщинам нельзя беременеть во время его приема (Категория беременности X). Это может сделать гормональные контрацептивы неэффективными, поэтому необходимо использовать другие формы контроля над рождаемостью.
В США они доступны только у врачей, которые следуют утвержденным FDA оценке риска и снижению риска. стратегия (REMS) в отношении рисков для плода и рисков повреждения печени. Врач должен задокументировать отрицательный результат теста на беременность для женщины перед назначением препарата, проконсультироваться по поводу контрацепции и регулярно проводить тесты на беременность. Поскольку существует высокий риск того, что бозентан вызывает повреждение печени, план REMS также требует предварительного тестирования на повышение уровня трансаминаз и регулярных тестов во время приема препарата. Бозентан также противопоказан пациентам, принимающим глибурид из-за повышенного риска увеличения печеночных ферментов и повреждения печени при совместном приеме этих двух агентов.
Кроме того, к риску возникновения врожденных дефектов и повреждения печени, бозентан имеет высокий риск возникновения отека, легочной веноокклюзионной болезни, уменьшения количества сперматозоидов и гемоглобина и гематокрит.
К очень частым побочным эффектам (встречающимся у более чем 10% людей) относятся головная боль, повышение уровня трансаминаз и отек. Общие побочные эффекты (от 1% до 10% людей) включают анемию, снижение гемоглобина, реакции гиперчувствительности, воспаление кожи, зуд, сыпь, покраснение кожи, покраснение, обмороки, учащенное сердцебиение, низкое кровяное давление, заложенность носа, гастро -эзофагеальная рефлюксная болезнь и диарея.
Бозентан является конкурентным антагонистом эндотелина -1 в отношении эндотелина-A (ET-A) и рецепторы эндотелина-B (ET-B). В нормальных условиях связывание эндотелином-1 рецепторов ЕТ-A вызывает сужение легочных кровеносных сосудов. Напротив, связывание эндотелина-1 с рецепторами ЕТ-В было связано как с расширением сосудов, так и с сужением сосудов гладкой мускулатуры сосудов, в зависимости от подтипа ЕТ-В (ЕТ-В1 или ЕТ-B2) и ткани. Бозентан блокирует рецепторы ЕТ-А и ЕТ-В, но считается, что он оказывает большее влияние на рецепторы ЕТ-А, вызывая общее снижение легочного сосудистого сопротивления.
Абсолютная биодоступность бозентана составляет около 50% у здоровых людей. Пиковая концентрация бозентана в плазме диспергируемых таблеток для пероральной суспензии в среднем на 14% меньше, чем пиковая концентрация пероральных таблеток.
Бозентан является субстратом CYP3A4 и CYP2C9. CYP2C19 также может играть роль в его метаболизме. Он также является субстратом печеночных транспортеров органических анион-транспортирующих полипептидов (OATP ) OATP1B1, OATP1B3 и OATP2B1.
Выведение бозентана происходит в основном через печень с минимальным вкладом почек и фекальная экскреция.
Использование бозентана с циклоспорином противопоказано, поскольку циклоспорин А заметно увеличивает концентрацию бозентана в сыворотке крови.
Бозентан изучался в сердечная недостаточность в исследовании REACH-1, которое было прекращено в начале 1997 года из-за токсичности изучаемой дозы; по состоянию на 2001 г. результаты этого испытания не публиковались.
Оно было одобрено для лечения гипертонии легочной артерии в США в ноябре 2001 г. и в Европейском Союзе в мае 2002 г.
К 2013 году мировые продажи бозентана составили 1,57 миллиарда долларов. Срок действия патентов на бозентан истек в 2015 году.