| Borrelia burgdorferi | |
|---|---|
 | |
| Borrelia burgdorferi | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Spirochates |
| Отряд: | Spirochaetales |
| Семейство: | Spirochaetaceae |
| Род: | Borrelia |
| Вид: | B. burgdorferi |
| Биномиальное имя | |
| Borrelia burgdorferi . Johnson et al. 1984 исправление. Барантон и др. 1992 | |
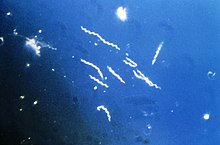
Borrelia burgdorferi - бактериальный вид класса спирохет класса рода Borrelia. B. burgdorferi существует в Северной Америке и Европе и до 2016 года была единственной известной причиной болезни Лайма в Северной Америке (Borrelia mayonii, обнаруженная на Среднем Западе США, также, как известно, вызывает болезнь). Виды Borrelia считаются грамотрицательными.
Borrelia burgdorferi названа в честь исследователя Вилли Бургдорфера, который первым выделил бактерия в 1982 году. Borrelia виды - это комплекс видов, которые, как известно, вызывают болезнь Лайма, все вместе называемые Borrelia burgdorferi.
B. burgdorferi напоминает другие спирохеты тем, что имеет внешнюю и внутреннюю мембраны с тонким слоем пептидогликана между ними. Однако во внешней мембране отсутствует липополисахарид. Его форма - плоская волна. Он имеет ширину около 0,3 мкм и длину от 5 до 20 мкм.
B. burgdorferi - это микроаэробная, подвижная спирохета с 7-11 связанными перисплазматическими жгутиками на каждом конце, которые позволяют бактериям перемещаться в средах с низкой и высокой вязкостью, что связано с его высокий фактор вирулентности.
B. burgdorferi - это медленнорастущая микроаэрофильная спирохета с временем удвоения от 24 до 48 часов.
B. burgdorferi циркулирует между клещами Ixodes и позвоночным хозяином в энзоотическом цикле. B. burgdorferi, живущий в клещах, может передаваться его потомству (Buhner, 2015). Спирохеты выживают, когда личинки линяют в нимфу, и сохраняются в бедной питательными веществами средней кишке, когда нимфа зимует. Затем инфицированные нимфы передают B. burgdorferi, питаясь другим позвоночным, чтобы завершить цикл. Клещи могут передавать B. burgdorferi человеку, но люди - тупиковые хозяева, которые вряд ли продолжат жизненный цикл спирохет. Нимфы превращаются в взрослых клещей, которые обычно питаются более крупными млекопитающими, не способными поддерживать выживание B. burgdorferi.
Болезнь Лайма является зоонозом, трансмиссивное заболевание, передающееся Ixodes клещом (также переносчиком Babesia и Anaplasma ). Зараженный нимфальный клещ передает B. burgdorferi через слюну человеку во время приема пищи с кровью.
Клинические проявления болезни Лайма наиболее известны по характерной сыпи типа «яблочко» (также известной как erythema chronicum migrans ), но также могут включать миокардит, кардиомиопатию, аритмию, артрит, артралгию, менингит, невропатия и паралич лицевого нерва в зависимости от стадии инфекции.
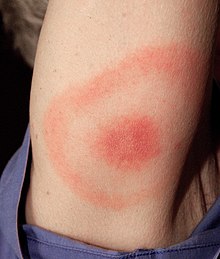 Характерная сыпь типа "яблочко" (хроническая мигрирующая эритема) болезни Лайма 1 стадии
Характерная сыпь типа "яблочко" (хроническая мигрирующая эритема) болезни Лайма 1 стадии B. burgdorferi были обнаружены в связи с возможной ассоциацией с первичными кожными B-клеточными лимфомами (PCBCL), где в обзоре первичной литературы по состоянию на 2010 год было отмечено, что большинство исследованных PCBLC «не реагировали» на антибиотики; следовательно, как и в случае ассоциации Chlamydophila psittaci с лимфомой лимфоидной ткани, связанной со слизистой оболочкой глаза (MALT), рабочий вывод заключался в том, что «если B. burgdorferi действительно ассоциируется с PCBCL, то существует широкий географический охват. вариабельность и другие факторы, вероятно, вовлечены ".
Развитие болезни проходит в 3 стадии.
Стадия 1 известна как ранняя локализованная стадия и происходит примерно через 3 дня - 1 месяц после инокуляции. Он поражает локальную область вокруг укуса и характеризуется локальным отеком и / или красной сыпью типа «яблочко» (также известной как хроническая мигрирующая эритема ), проявляющейся в виде эритематозного круга, окружающего определенный центр, который расширяется. наружу. Он может достигать 15 см в диаметре. Когда сыпь начинает исчезать, первые симптомы могут проявляться как симптомы гриппа. На этой стадии антибиотики наиболее эффективны для предотвращения дальнейшего роста и появления симптомов заболевания до того, как проявятся основные симптомы.
Стадия 2 известна как стадия раннего распространения и наступает через несколько недель - через несколько месяцев после заражения, если не лечить. Бактерии распространяются через кровь по телу и поражают органы. Он часто проявляется общими симптомами, такими как лихорадка, озноб, утомляемость и лимфаденопатия, а также специфическими для органа симптомами. Это может повлиять на сердце, вызывая миокардит и аритмию, например, атриовентрикулярную блокаду (которая, если достаточно сильная, может потребовать установки кардиостимулятора). Это может повлиять на опорно-двигательный аппарат вызывая невоспалительной переходная артрит и / или артралгия. Это может повлиять на нервную систему, проявляясь в виде паралича лицевого нерва (паралич Белла, обычно двусторонний), утомляемости и потери памяти.
Стадия 3 известна как стадия позднего распространения и наступает через месяцы - годы после первоначального заражения. Последствия 3 стадии включают энцефалит или менингит. а также мигрирующие артропатии (чаще всего коленного сустава).
. Анаплазмоз и бабезиоз также являются распространенными клещевыми патогенами, переносимыми клещами Ixodes, которые заражают людей так же, как Borrelia burgdorferi. Следовательно, клещ Ixodes может одновременно инфицировать хозяина двумя или всеми другими заболеваниями. Когда хозяин коинфицирован, комбинированные эффекты заболеваний действуют синергетически, часто оказываясь более серьезными симптомами, чем отдельная инфекция. Коинфицированные люди имеют тенденцию проявлять более тяжелые проявления болезни Лайма. Кроме того, они имеют тенденцию приобретать более широкий спектр вторичных симптомов, таких как симптомы гриппа. Необходимо провести дополнительные исследования и исследования, чтобы определить синергетический эффект коинфекции и ее влияние на организм человека.
На данный момент существует три фактора, которые могут влиять на тяжесть клинических проявлений болезни Лайма. Присутствие рибосомных спейсеров, плазмид и протеина С внешней поверхности (OspC) являются индикаторами серьезности инфекции. Кроме того, люди сами по себе различаются по своей реакции на инфекцию. Различная реакция приводит к различным клиническим проявлениям и различным инфекциям различных органов.
После передачи возбудителя он акклиматизируется к условиям млекопитающих. Borrelia burgdorferi изменяет свои гликопротеины и протеазы на своей плазматической мембране, чтобы облегчить его распространение по крови. При инфицировании B. burgdorferi будет экспрессировать белки, которые будут взаимодействовать с эндотелиальными клетками, тромбоцитами, хондроцитами и внеклеточным матриксом. Это взаимодействие препятствует правильному функционированию инфицированных участков, что приводит к патологическим проявлениям болезни Лайма. В ответ хозяин инициирует воспалительную реакцию, чтобы попытаться устранить инфекцию.
Borrelia burgdorferi также экспрессирует по меньшей мере семь связывающих плазминоген белков для вмешательства фактора H на уровне активации. Это часть стратегии уклонения системы комплемента, которая ведет к блокированию иммунного ответа ниже по течению.
Кроме того, Borrelia burgdorferi имеет стратегию прямого ингибирования классического пути системы комплемента. Боррелиальный липопротеин BBK32, экспрессируемый на поверхности Borrelia burgdorferi, связывает инициирующий протеазный комплекс C1 классического пути. Более конкретно, BBK32 взаимодействует с субъединицей C1r C1. С-концевой домен белка BBK32 опосредует связывание. В результате C1 оказывается в неактивной форме.
Б. burgdorferi (штамм B31) был третьим микробным геномом, когда-либо секвенированным после секвенирования как Haemophilus influenzae, так и Mycoplasma genitalium в 1995 году. Его линейная хромосома содержит 910,725 пар оснований и 853 гена. Используемый метод секвенирования: дробовик для полного генома. Проект секвенирования, опубликованный в журналах «Nature» в 1997 г. и «Молекулярная микробиология» в 2000 г., проводился в Институте геномных исследований. В целом, геном B. burgdorferi, как ни странно, состоит из одной мегабазной хромосомы и множества кольцевых и линейных плазмид размером от 9 до 62 килобаз. Мегабазная хромосома, в отличие от многих других эубактерий, не имеет отношения ни к вирулентности бактерий, ни к взаимодействию паразита и хозяина. Некоторые плазмиды необходимы для жизненного цикла B. burgdorferi, но не для размножения бактерий в культуре.
Геномные вариации B. burgdorferi способствуют различной степени инфицирования и распространения. Каждая геномная группа имеет различные антигены на своем мембранном рецепторе, специфичные для инфекции хозяина. Одним из таких мембранных рецепторов является поверхностный белок OspC. Показано, что поверхностный белок OspC является надежным индикатором определения геномной классификации и степени распространения. Различное количество локусов OspC является показателем и детерминантами вариаций B. burgdorferi. Поверхностный белок также находится в авангарде текущих исследований вакцин против болезни Лайма через Borrelia.
Генетически разнообразные штаммы B. burgdorferi, определяемые последовательностью ospC, поддерживаются в пределах Северо-восток США. Балансирующий отбор может воздействовать на ospC или соседнюю последовательность для поддержания генетического разнообразия B. burgdorferi. Балансирующий отбор - это процесс, с помощью которого несколько версий гена удерживаются в генофонде с неожиданно высокой частотой. Две основные модели, которые контролируют баланс отбора B.burgdorferi, - это отрицательный частотно-зависимый отбор и полиморфизм нескольких ниш . Эти модели могут объяснить, как B. burgdorferi диверсифицировалась и как отбор может повлияли на распространение вариантов B. burgdorferi или на изменение конкретных признаков вида в определенных средах.
При отрицательном частотно-зависимом отборе редкие и необычные варианты будут иметь избирательное преимущество над вариантами, которые очень распространены в окружающей среде. Для B. burgdorferi низкочастотные варианты будут предпочтительны, потому что у потенциальных хозяев будет меньше шансов вызвать иммунологический ответ на вариант-специфичный внешний белок OspC.
Экологический ниши - это все переменные в окружающей среде, такие как ресурсы, конкуренты и реакции, которые способствуют приспособленности организма. Полиморфизм множественных ниш утверждает, что разнообразие внутри популяции поддерживается за счет различного количества возможных ниш и сред. Следовательно, чем больше разнообразия ниш, тем больше вероятность полимофризма и разнообразия. Для B. burgdorferi различные ниши позвонков, такие как олени и мыши, могут влиять на выбор общего баланса для вариантов.
| Wikispecies содержит информацию, относящуюся к Borrelia burgdorferi |