Пептидогликан или муреин представляет собой полимер состоящий из сахаров и аминокислот, который образует сетчатый слой за пределами плазматической мембраны большинства бактерий, образуя клеточная стенка. Сахарный компонент состоит из чередующихся остатков β- (1,4) связанного N-ацетилглюкозамина (NAG) и N-ацетилмурамовой кислоты (NAM). К N-ацетилмурамовой кислоте присоединена пептидная цепь из трех-пяти аминокислот. Пептидная цепь может быть поперечно связана с пептидной цепью другой цепи, образующей трехмерный сетчатый слой. Пептидогликан выполняет структурную роль в стенке бактериальной клетки, придавая структурную прочность, а также противодействуя осмотическому давлению цитоплазмы. Пептидогликан также участвует в бинарном делении во время размножения бактериальных клеток.
Слой пептидогликана значительно толще у грамотрицательных бактерий (от 20 до 80 нанометров), чем у грамотрицательных бактерий (от 7 до 8 нанометров). В зависимости от условий роста pH пептидогликан образует от 40 до 90% от клеточной стенки сухой массы грамположительных бактерий, но только около 10% грамотрицательных штаммов. Таким образом, наличие высоких уровней пептидогликана является основным фактором, определяющим характеристику бактерий как грамположительных. У грамположительных штаммов он важен для роли прикрепления и серотипирования. Как для грамположительных, так и для грамотрицательных бактерий через пептидогликан могут проходить частицы размером примерно 2 нм.
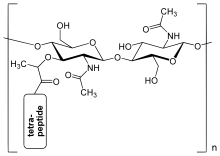 Пептидогликан.
Пептидогликан. Слой пептидогликана в стенке бактериальной клетки представляет собой структуру кристаллической решетки, образованную линейными цепями двух чередующихся амино сахара, а именно N-ацетилглюкозамин (GlcNAc или NAGA) и N-ацетилмурамовая кислота (MurNAc или NAMA). Чередующиеся сахара связаны β- (1,4) - гликозидной связью. Каждый MurNAc присоединен к короткой (4-5 остатков) аминокислотной цепи, содержащей L-аланин, D-глутаминовую кислоту, мезо-диаминопимелиновую кислоту и D-аланин в случае Escherichia coli (грамотрицательная бактерия) или L-аланин, D-глютамин, L-лизин, и D-аланин с промежуточным мостиком 5- глицин между тетрапептидами в случае Staphylococcus aureus (грамположительная бактерия). Пептидогликан - один из важнейших источников D-аминокислот в природе.
Сшивание между аминокислотами в различных линейных аминосахарных цепях происходит с помощью фермента DD-транспептидаза и приводит к образованию трехмерной структуры, которая является прочный и жесткий. Конкретная аминокислотная последовательность и молекулярная структура меняются в зависимости от бактерий видов.

Структура пептидогликана. NAG = N-ацетилглюкозамин (также называемый GlcNAc или NAGA), NAM = N-ацетилмурамовая кислота (также называемая MurNAc или NAMA).

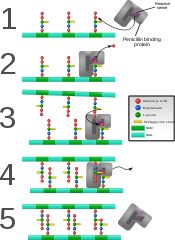
Пенициллин-связывающий белок, образующий поперечные связи во вновь образованной бактериальной клеточной стенке.
Мономеры пептидогликана синтезируются в цитозоле, а затем присоединяются к мембранному носителю бактопренолу. Бактопренол переносит мономеры пептидогликана через клеточную мембрану, где они встраиваются в существующий пептидогликан.
На первом этапе синтеза пептидогликана глутамин, который является аминокислотой, отдает аминогруппу для сахар, фруктозо-6-фосфат. Это превращает фруктозо-6-фосфат в. На втором этапе ацетильная группа переносится с ацетил-СоА на аминогруппу при образовании глюкозамин-6-фосфата. На третьей стадии процесса синтеза N-ацетилглюкозамин-6-фосфат изомеризуется, в результате чего N-ацетилглюкозамин-6-фосфат превращается в.
На стадии 4 N-ацетил- глюкозамин-1-фосфат, который теперь является монофосфатом, атакует UTP. Уридинтрифосфат, который представляет собой пиримидин нуклеотид, обладает способностью действовать как источник энергии. В этой конкретной реакции после того, как монофосфат атакует UTP, выделяется неорганический пирофосфат и заменяется монофосфатом, образуя UDP-N-ацетилглюкозамин (2,4). (Когда UDP используется в качестве источника энергии, он выделяет неорганический фосфат.) Эта начальная стадия используется для создания предшественника NAG в пептидогликане.
На этапе 5 часть UDP-N-ацетилглюкозамина (UDP-GlcNAc) превращается в UDP-MurNAc (UDP-N-ацетилмурамовая кислота) путем добавления лактильной группы к глюкозамину. Также в этой реакции гидроксильная группа C3 удаляет фосфат из альфа-углерода фосфоенолпирувата. Это создает так называемое производное енола, которое будет восстановлено до «лактильной части» под действием НАДФН на шестом этапе.
На этапе 7 UDP-MurNAc превращается в пентапептид UDP-MurNAc путем добавления пяти аминокислоты, обычно включая дипептид D -аланил- D -аланин. Каждая из этих реакций требует источника энергии АТФ. Все это называется этапом один.
Вторая стадия происходит в цитоплазматической мембране. Именно в мембране липидный носитель, называемый бактопренолом, переносит предшественники пептидогликана через клеточную мембрану. Бактопренол будет атаковать UDP-MurNAc penta, создавая PP-MurNac penta, который теперь является липидом. Затем UDP-GlcNAc транспортируется в MurNAc, создавая Lipid-PP-MurNAc пента-GlcNAc, дисахарид, также являющийся предшественником пептидогликана. Как эта молекула транспортируется через мембрану, до сих пор не понятно. Однако, как только он там оказывается, он добавляется к растущей цепи гликана. Следующая реакция известна как трангликозилирование. В этой реакции гидроксильная группа GlcNAc будет присоединяться к MurNAc в гликане, что вытесняет липид-PP из гликановой цепи. Фермент, ответственный за это, - трансгликозилаза.
Некоторые антибактериальные препараты, такие как пенициллин, препятствуют производству пептидогликана за счет связывания с бактериальными ферментами, известными как пенициллин-связывающие белки или DD-транспептидазы. Пенициллин-связывающие белки образуют связи между поперечными связями олигопептидов в пептидогликане. Чтобы бактериальная клетка могла воспроизводиться посредством бинарного деления, более миллиона субъединиц пептидогликана (NAM-NAG + олигопептид) должны быть присоединены к существующим субъединицам. Мутации в генах, кодирующих транспептидазы, которые приводят к уменьшению взаимодействий с антибиотиком, являются важным источником возникающей устойчивости к антибиотикам. Мураймицины представляют собой подкласс нуклеозидных антибиотиков, которые действуют как конкурентные ингибиторы природного субстрата UDP-MurNAc-пентапептида (UM5A) фосфо-N-ацетилмурамоил-пентапептид транслоказы (MraY).
Лизоцим, который содержится в слезах и составляет часть врожденной иммунной системы организма, проявляет свой антибактериальный эффект, разрывая β- (1,4) -гликозидные связи в пептидогликане (см. выше).
Некоторые археи имеют аналогичный слой псевдопептидогликана (также известного как псевдомуреин), в котором остатки сахара представляют собой β- (1,3) связанный N-ацетилглюкозамин и N-ацетилталозаминуроновая кислота. Это делает клеточные стенки таких архей нечувствительными к лизоциму.