| |||
| Идентификаторы | |||
|---|---|---|---|
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.013.697 | ||
| PubChem CID | |||
| UNII | |||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | C10H10Cl2Zr | ||
| Молярная масса | 292,31 г · моль | ||
| Внешний вид | белое твердое вещество | ||
| Растворимость i n вода | Растворим (гидролиз) | ||
| Опасности | |||
| Паспорт безопасности | CAMEO Chemicals MSDS | ||
| Родственные соединения | |||
| Родственные соединения | Дихлорид титаноцена.. Дихлорид ванадоцена. Дихлорид ниобоцена.. | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Дихлорид цирконоцена представляет собой цирконийорганическое соединение, состоящее из центрального атома циркония, с двумя циклопентадиенилами и двумя хлор лиганды. Это бесцветное диамагнитное твердое вещество, устойчивое на воздухе.
Дихлорид цирконоцена может быть получен из комплекса хлорида циркония (IV) - ТГФ и циклопентадиенида натрия :
Тесно родственное соединение Cp 2 ZrBr 2 был впервые описан Birmingham and Wilkinson.
Соединение представляет собой изогнутый металлоцен : кольца Cp не параллельны, среднее значение Cp (центроид) -M -Cp угол 128 °. Угол Cl-Zr-Cl 97,1 ° больше, чем в дихлориде ниобоцена (85,6 °) и дихлориде молибдоцена (82 °). Эта тенденция помогла установить ориентацию ВЗМО в этом классе комплексов.
Дихлорид цирконоцена реагирует с алюмогидридом лития чтобы получить Cp 2 ZrHCl реактив Шварца :
Поскольку алюмогидрид лития является сильным восстановителем, происходит некоторое избыточное восстановление с образованием дигидридокомплекса Cp 2 ZrH 2 ; обработка смесь продукта с метиленхлоридом превращает его в реактив Шварца.
Цирконоцендихлорид также может быть использован для приготовления реагента Негиши, Cp 2 Zr (η -бутен ), который можно использовать в качестве источника Cp 2 Zr в реакциях окислительной циклизации. Реагент Негиши получают путем обработки дихлорида цирконоцена с n-BuLi, что приводит к замене двух хлоридных лигандов бутильными группами. Дибутиловое соединение d впоследствии подвергается элиминированию бета-гидрида с образованием одного η-бутенового лиганда, при этом другой бутиловый лиганд быстро теряется в виде бутана в результате восстановительного элиминирования.

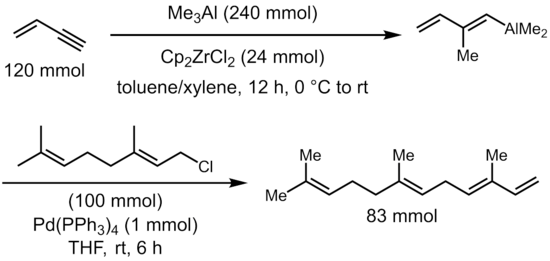
Дихлорид цирконоцена катализирует карбоалюминирование алкинов с помощью триметилалюминия с образованием (алкенил) диметилалана, универсального промежуточного соединения для дальнейших реакций кросс-сочетания для синтеза стереоданных тризамещенных олефинов.
.