 | |
 | |
| Имена | |
|---|---|
| Другие названия Карбид циркония (I) | |
| Идентификаторы | |
| Номер CAS | |
| ECHA InfoCard | 100.031.920 |
| Номер EC |
|
| PubChem CID | |
| номер RTECS |
|
| номер ООН | 3178 |
| CompTox Dashboard (EPA ) | |
| Свойства | |
| Химическая формула | ZrC |
| Молярная масса | 103,235 г · моль |
| Внешний вид | Серое тугоплавкое твердое вещество |
| Запах | Без запаха |
| Плотность | 6,73 г / см (24 ° C) |
| Температура плавления | 3,532–3,540 ° C (6,390–6,404 ° F; 3,805–3,813 K) |
| Температура кипения | 5,100 ° C (9210 ° F; 5370 K) |
| Растворимость в воде | Нерастворимый |
| Растворимость | Растворимый в концентрированной H2SO4, HF,HNO 3 |
| Структура | |
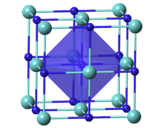
| Кристаллическая структура | Кубическая, cF8 |
| Пространственная группа | Fm3m, No. 225 |
| Постоянная решетки | a = 4,6976 (4) Å α = 90 °, β = 90 °, γ = 90 ° |
| Координационная геометрия | Октаэдрическая |
| Термохимия | |
| Теплоемкость (C) | 37,442 Дж / моль · K |
| Стандартная молярная. энтропия (S 298) | 33,14 Дж / моль · K |
| Стандартная энтальпия образования. (ΔfH298) | -207 кДж / моль (экстраполирована на стехиометрическую состав). −196,65 кДж / моль |
| Опасности | |
| Основные опасности | Пирофорные |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H228, H302, H312, H332 |
| Меры предосторожности GHS | P210, P280 |
| NFPA 704 (огненный алмаз) |  0 0 0 0 0 0 |
| Родственные соединения | |
| Прочие анионы | Нитрид циркония. Оксид циркония |
| Прочие катионы | Титаниу m карбид. карбид гафния. карбид ванадия. карбид ниобия. карбид тантала. карбид хрома. карбид молибдена. карбид вольфрама |
| Если не указано иное, данные приводятся для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Карбид циркония (Zr C ) представляет собой чрезвычайно твердый огнеупорный керамический материал, коммерчески используемый в наконечниках для режущих инструментов. Обычно его обрабатывают методом спекания.
| Тепловое расширение. Коэффициенты ZrC | |
|---|---|
| T | αV |
| 100 ° C | 0,141 |
| 200 ° C | 0,326 |
| 400 ° C | 0,711 |
| 800 ° C | 1,509 |
| 1200 ° C | 2,344 |
Он имеет вид серого металлического порошка с кубической кристаллической структурой. Он очень коррозионно-стойкий. Этот карбид переходного металла внедрения группы IV также входит в состав сверхвысокотемпературной керамики или (UHTC). Благодаря наличию металлической связи ZrC имеет теплопроводность 20,5 Вт / м · К и электрическую проводимость (удельное сопротивление ~ 43 мкОм · см), которые аналогичны таковым для металлического циркония. Прочная ковалентная связь Zr-C придает этому материалу очень высокую температуру плавления (~ 3530 ° C), высокий модуль (~ 440 ГПа) и твердость (25 ГПа). ZrC имеет более низкую плотность (6,73 г / см) по сравнению с другими карбидами, такими как WC (15,8 г / см), TaC (14,5 г / см) или HfC (12,67 г / см). ZrC кажется подходящим для использования в транспортных средствах для перезагрузки, ракетных /scramjet двигателях или сверхзвуковых транспортных средствах, в которых низкая плотность и высокие температуры несущие способности являются важнейшими требованиями.
Как и большинство карбидов тугоплавких металлов, карбид циркония субстехиометрический, то есть он содержит углерод вакансии. При содержании углерода выше, чем приблизительно ZrC 0,98, материал содержит свободный углерод. ZrC стабилен при соотношении углерода к металлу от 0,65 до 0,98.
Карбиды металлов группы IVA, TiC, ZrC и SiC практически инертны по отношению к воздействию сильных водных кислот (HCl) и сильных водные основания (NaOH) даже при 100 'C, однако ZrC реагирует с HF.
Смесь карбида циркония и карбида тантала является важным керметом материалом.
карбид циркония без гафния и карбид ниобия может использоваться в качестве тугоплавких покрытий в ядерных реакторах. Из-за низкого поперечного сечения поглощения нейтронов и слабой чувствительности к повреждению при облучении он находит применение в качестве покрытия из диоксида урана и частиц диоксида тория ядерного топлива. Покрытие обычно наносят термическим химическим осаждением из паровой фазы в реакторе с псевдоожиженным слоем. Он также обладает высоким коэффициентом излучения и высокой токовой нагрузкой при повышенных температурах, что делает его перспективным материалом для использования в термофотовольтаических радиаторах, наконечниках и массивах полевых эмиттеров.
Он также используется в качестве абразива , в плакировке, в керметах, накаливаниях нитях и режущих инструментах.
Карбид циркония может быть изготовлен несколькими способами. Один из методов - карботермическая реакция диоксида циркония графитом. В результате получается порошок. Затем можно получить уплотненный ZrC путем спекания порошка ZrC при температуре выше 2000 ° C. Горячее прессование ZrC может снизить температуру спекания и, следовательно, способствует получению полностью уплотненного мелкозернистого ZrC. Искровое плазменное спекание также использовалось для получения полностью уплотненного ZrC.
Карбид циркония также может быть получен путем обработки на основе раствора. Это достигается кипячением оксида металла с ацетилацетоном.
Другой способ изготовления - химическое осаждение из паровой фазы. Это достигается нагреванием циркониевой губки и пропусканием через нее галогенидного газа.
Плохая стойкость к окислению при температуре выше 800 ° C ограничивает области применения ZrC. Один из способов повысить стойкость ZrC к окислению - это создание композитов. Предлагаемые важные композиты - это композит ZrC-ZrB 2 и ZrC-ZrB 2 -SiC. Эти композиты могут работать при температуре до 1800 ° C. Другой способ улучшить это - использовать другой материал в качестве барьерного слоя, например, в топливных частицах TRISO.