Тетрадентатные лиганды - это лиганды, которые связываются с четырьмя донорными атомами с центральным атомом с образованием координационного комплекса. Это количество донорных атомов, которые связываются, называется дентатностью и является способом классификации лигандов. Тетрадентатные лиганды широко распространены в природе в форме хлорофилла, который имеет сердцевинный лиганд, называемый хлорин, и гема с сердцевинным лигандом, называемым порфирин. Они добавляют большую часть цвета, наблюдаемого у растений и людей. Фталоцианин представляет собой искусственный макроциклический тетрадентатный лиганд, который используется для получения синих и зеленых пигментов.
Тетрадентатные лиганды можно классифицировать по топологии связей между донорными атомами. Обычными формами являются линейные (также называемые последовательными), кольцевые или триподные. Тетраподальный лиганд, который также является тетрадентатным, имеет четыре ветви с донорными атомами и мостик, который не является донором. При связывании с центральным атомом возможно несколько расположений, называемых геометрическими изомерами.
Линейный тетрадентатный лиганд имеет четыре донорных атома в линию, каждый последующий донор соединен одним из трех мостиков.
Линейный тетрадетатный лиганд, связанный с металлом в тетраэдрической координации, может соединяться только одним способом. Если лиганд несимметричный, то есть два хиральных расположения.
Линейный тетрадетатный лиганд, связанный с металлом в плоско-квадратной координации одним способом. Расположение против часовой стрелки или по часовой стрелке эквивалентно.
 линейный тетрадентатный лиганд в трех изомерах в правом столбце. Сверху вниз α, β, транс
линейный тетрадентатный лиганд в трех изомерах в правом столбце. Сверху вниз α, β, транс Линейный тетрадентатный лиганд имеет донорные атомы, расположенные вдоль или в цепочку, так что каждый соседний донорный атом должен примыкать к центральному атому. Такое расположение приводит к трем стереохимическим результатам. Четыре донорные группы могут быть коэкваториальными. Эта геометрия называется транс, потому что оставшиеся незанятые позиции на октаэдре взаимно транс (противоположны). Когда два внутренних донорных атома, например вторичные амины в триене или EDDA являются пирамидными, два диастереомера для транс-расположения определяются относительной стереохимией этих центров. Обычно эти доноры являются взаимно транс, что приводит к образованию хирального комплекса C2-симметричных комплексов. Такое расположение иллюстрируется комплексами лиганда Троста.
. Лиганд может иметь один изгиб, так что один находится на полюсе, а три - на экваторе центрального атома. Это называется бета-цис-β (бета). Остальные октаэдрические позиции являются цис (смежными) друг с другом. Треугольники координирующих атомов и центрального атома имеют две компланарные и один перпендикулярный друг другу. Это хиральное расположение, поэтому есть два возможных зеркальных отображения. Расположение, в котором цепь идет вниз и по часовой стрелке, называется лямбда Λ, а где цепь идет вниз и против часовой стрелки, называется дельта Δ. Если цепь не симметрична, то могут быть получены разные изомеры, в зависимости от того, какой конец лиганда имеет изгиб. Если три донорных атома одинаковы на одном конце цепи, префиксы mer- и fac-, используемые для тридентатных лигандов, могут быть использованы, давая β-mer-, если три расположены на меридиане, или β-fac, если три расположены на грани октаэдра.
Цепь может иметь два изгиба, так что один на полюсе, два на экваторе и один на противоположном полюсе. Ни один из треугольников координирующих атомов и центрального атома не компланарен. Это называется цис-α (альфа). Это хиральное расположение, поэтому существует два возможных зеркальных отображения. Расположение, где цепь идет вниз по часовой стрелке и вниз, называется лямбда Λ, а где она идет вниз и против часовой стрелки и вниз, называется дельта Δ.
Триподентные тетрадентатные лиганды имеют донора. атом связан тремя цепочками с другими донорными атомами. Верхняя часть штатива называется вершиной, а донорный атом в этой позиции является апикальным или также известен как мостиковый атом. Остальные три атома-донора находятся на «ножках» штатива. Примеры могут иметь три идентичные цепи, присоединенные к атому в третичном порядке. Этот атом может быть азотом, фосфором или мышьяком. Молекулы, содержащие фосфор или донорные атомы мышьяка, остаются жесткими на P или As и могут сохранять свою форму, в отличие от соединений азота, которые быстро рацемизируются. Если все ножки штатива симметричны и идентичны друг другу, будет только один способ крепления в восьмигранной координации. Однако на центральном атоме остаются два неэквивалентных положения, поэтому, если присоединяются два разных монодентатных или несимметричный бидентатный лиганд, будут два возможных изомера. Если ступни различаются, значит, изомеров больше. Когда две ножки одинаковы, а одна отличается, существует три расположения, две из которых являются энантиомерами друг друга. При наличии трех разных ветвей возможны шесть изомеров, но два являются энантиомерами другой пары, а два - симметричными.
Атомы с пятью координатными положениями обычно тригонально-бипирамидальные или квадратная пирамида по форме. Симметричный триподный тетрадентатный лиганд может образовывать два изомера на квадратной пирамиде, в зависимости от того, находится ли мостиковый донор на вершине или в основании пирамиды. Дополнительное свободное место в квадратной пирамиде находится на основании. Квадратная пирамидальная координация имеет тенденцию происходить там, где образуется шестичленное кольцо с мостиком, мостиком, донорным атомом основания и центральным атомом. Более длинная ветвь (с тремя мостиковыми атомами) соединяется с вершиной пирамиды, и симметрия теряется.
Для тригональной бипирамиды лиганд в форме треножника занимает наиболее симметричное положение с мостиковым донором на одном из вершины и ножки штатива расположены вокруг основания, оставляя свободное место на противоположной вершине. Он имеет симметрию C 3v. Тригональная бипирамидная координация имеет тенденцию происходить, когда пятичленные кольца образуются с мостом, мостом, донорными атомами основания и центральным атомом.
В четырех координатах триподальный лиганд заполняет все доступные позиции, геометрия тригональная пирамида. Форма искажена от тетраэдра из-за несимметричности штатива.
Помимо формы, тетрадентатные лиганды можно классифицировать по лигирующим атомам на лиганде. Для линейных лигандов можно указать порядок. Лиганд может иметь отрицательный заряд, когда он находится в комплексе с центральным атомом. Это может развиться из-за потери ионов водорода при растворении вещества.
Другими характеристиками являются размер колец, образованных центральным металлом с двумя донорными атомами и промежуточной цепью лиганда. Обычно эти кольца имеют пять или шесть членов, но иногда и семь атомов. Для лигандов кольцевой формы важно общее количество атомов в кольце, поскольку оно определяет размер дырки для центрального атома. Каждый дополнительный атом в кольце увеличивает радиус дырки с 0,1 до 0,15 Å.
Лиганды также характеризуются зарядом. Тетрадентатные лиганды могут быть нейтральными, так что заряд всего комплекса такой же, как у центрального атома. Тетрадентатный моноанионный (TMDA) лиганд имеет один донорный атом с отрицательным зарядом. Тетрадентатный дианионный лиганд имеет двойной отрицательный заряд, а тетрадентатный трианионный лиганд имеет тройной отрицательный заряд. Максимальный заряд приходится на тетрадентатные тетраанионные лиганды, которые могут стабилизировать металлы в высоких степенях окисления, однако такие лиганды также должны противостоять окислению, чтобы выжить в сильно окисляющем атоме.
| name | аббревиатура | формула | форма | тип | заряд | MW | центральные атомы | pic |
|---|---|---|---|---|---|---|---|---|
| Хлорин | кольцо | NNNN | –2 | 312.3678 | Mg | 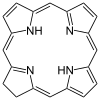 | ||
| Corrin | кольцо | NNNN | –1 | 306,40 | Co | 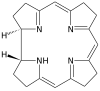 | ||
| 1,4,7,10-тетраоксациклододекан | 12-краун-4 | (C2H4O)4 | кольцо | OOOO | 0 | 176.21 | Li | 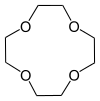 |
| 1,4,8,11-тетраазациклотетрадекан | циклам | (NHCH 2CH2NHCH 2CH2CH2)2 | кольцо | NNNN | 200,33 | переходные металлы | 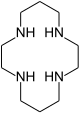 | |
| 1,4,7,10-тетраазациклододекан | циклен | кольцо | N4 | 172,271 | Zn |  | ||
| Дибензотетраметилтетрааза [14] аннулен | tmtaa | кольцо | NNNN | 2- | UO2 | |||
| N, N-этилендиаминдиуксусная кислота | NH2C2H4N (CH 2 COOH) 2 | штатив | НЕТ 2 | 2– | ||||
| N, N'-этилендиаминдиуксусная кислота | (-CH 2 NHCH 2 COOH) 2 | линейная | ONNO | 2– | ||||
| N-гидроксиимино-2,2'-дипропионовая кислота | H3HIDPA | HON (CH (CH 3) CO 2H)2 | линейная | ONOO | 3– | V |  | |
| диэтилентриаминуксусная кислота | DTMA | NH2C2H4NHC 2H4NHCH 2 COOH | линейная | NNNO | 1– | Co | ||
| изо-диэтилентриаминуксусная кислота | i-DTMA | (NH 2C2H4)2NCH 2 COOH | триподальный | NN2NO | 1– | Co | ||
| лиганд Jäger's N2O2 | линейный акацен | ONNO N 2O2 | Ni | |||||
| Нафталоцианин | C48H26N8 | кольцо | NNNN | 714,79 |  | |||
| Нитрилотриуксусная кислота | NTA | N (CH 2CO2H)3 | тройной | NO3 | 3– | 191.14 | Ca, Cr, Cu и Fe, Ni | 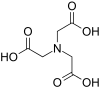 |
| Фталоцианин | H2Pc | C32H18N8 | кольцо | NNNN | 2– | Cu, Co | 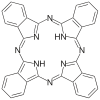 | |
| Порфирин | кольцо | NNNN | Mg, V, Fe, Ni | 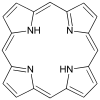 | ||||
| Родоторуловая кислота | C14H24N4O6 | Форма I | ОООО | 344,36 | Fe |  | ||
| Саленовый лиганд | линейный | ONNO N 2O2 | 268,31 | |||||
| лиганд salpn | salpn | linear | ONNO | 2- | 282,34 | Тетары Cr, Cu, Fe, Ni |  | |
| (мезо- и рацемические изомеры) | [(CH 3)2As (CH2) 3 As (C 6H5) CH 2]2 | линейный | AsAsAsAs | 0 | Co | |||
| 1,1,4,7,10,10-гексафенил-1,4,7,10-тетрафосфадекан. | тет-1 | линейный | PPPP | 0 | 670,68 | Fe Ru Os Re Pd Pt | ||
| 1,4,7,10-тетратиадодекан | [12] -ан-S 4 | кольцо | SSSS | 0 | Cu | |||
| 1,4,7,10-тетратиатридекан | [13] -ан-S 4 | кольцо | SSSS | 0 | Cu | |||
| 1,4, 8,11-тетратиатетрадекан | [14] -ан-S 4 | кольцо | SSSS | 0 | Cu | |||
| 1,4,8,12-тетратиапентадекан | [15 ] -ан-S 4 | кольцо | SSSS | 0 | Cu | |||
| 1,5,9,13-тетратиагексадекан | [14] -ан-S 4 | кольцо | SSSS | 0 | Cu | |||
| 2,5,8-тритиа [9] (2,5) тиофенофан | кольцо | SSSS | 0 | Cu | ||||
| Диметиловый эфир триэтиленгликоля | TG3 | CH3(OCH 2CH2)3OCH 3 | линейный | OOOO | 0 | 178,23 | нейтральный Na, K | |
| Триэтилентетрамин | ТЭТА. триен | [CH 2 NHCH 2CH2NH2]2 | линейный | NNNN | 146,24 | Cu | ||
| трис- (диметиларсинопропил) -арсин | As [CH 2CH2CH2As (CH 3)2]3 | штатив | AsAs 3 | 0 | Fe Ni Co oct. Ni tbp | |||
| трис- (о-диметиларсинофенил) -арсин | As [oC 6H4As (CH 3)2]3 | штатив | AsAs 3 | 0 | Pt Pd Ni tbp. Ru oct | |||
| трис- (о-дифениларсинофенил) -арсин | As [oC 6H4As (C 6H5)2]3 | штатив | AsAs 3 | 0 | Pt Pd Ru Rh Ni tbp. Re Ru Os Rh Pd Pt oct | |||
| CH3[As (CH 3) oC 6H4]3AsCH (3)2 | линейный | As4 | 0 | Pd квадратный пирамидальный | ||||
| [As (C 6H5)2oC 6H4As (C 6H5) CH 2]2 | линейный | As4 | 0 | Ni 4 координата. Ni Co пятикооринат | ||||
| трис - (о-дифенилфосфинофенил) -фосфин | штатив тетрафосфин Венанци | P [oC 6H4P (C 6H5)2]3 | штатив | PP3 | 0 | Pd Pt Ru Ru Os Cr Cr Cr Mn Co oct. Ni Fe Co Co tbp | ||
| Трис (2-пиридилметил) амин | TPA | триподаль | N3N | 290,37 | Cu |  | ||
| 2, 2'-би-1,10-фенантролин | БИФЕН | линейный | N4 | 0 | Cd Sm Am |
Гем представляет собой гетероциклический макросия cle тетрадентатный лиганд кольцевой формы. Это важная молекула красных кровяных телец.
. Хлорофилл имеет несколько форм и играет важную роль в фотосинтезе растений. Бактерии могут использовать варианты, называемые бактериохлорофиллами.