 | |
| Имена | |
|---|---|
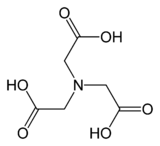
| Предпочтительное название ИЮПАК 2,2 ', 2' '- Нитрилотриуксусная кислота | |
| Другие названия N, N-Бис (карбоксиметил) глицин. 2- [Бис (карбоксиметил) амино] уксусная кислота. Триглицин | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| Ссылка Beilstein | 1710776 |
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.004.869 |
| Номер EC |
|
| Ссылка Гмелина | 3726 |
| KEGG | |
| MeSH | Нитрилотриуксусная + кислота |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| Номер ООН | 2811 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
| Химическая формула | C6H9NO6 |
| Молярная масса | 191,14 |
| Внешний вид | Белые кристаллы |
| Температура плавления | 246 ° C (475 ° F; 519 K) |
| Растворимость в воде | Нерастворим. <0.01 g/100 mL at 23℃ |
| Термохимия | |
| Стандартная энтальпия образования. (ΔfH298) | -1,3130–-1,3108 МДж моль |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Предупреждение |
| Краткая характеристика опасности GHS | H302, H319, H351 |
| Меры предосторожности GHS | P281, P305 + 351 + 338 |
| Температура вспышки | 100 ° C (212 ° F; 373 K) |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 1,1 г кг (перорально, крыса) |
| Связанные соединения | |
| Родственные алкановые кислоты | |
| Родственные соединения | |
| Если не указано иное, данные представлены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на информационный блок | |
Нитрилотриуксусная кислота (NTA) представляет собой аминополикарбоновую кислоту с формулой N (CH 2CO2H)3. Это бесцветное твердое вещество, которое используется в качестве хелатирующего агента, который образует координационные соединения с ионами металлов (хелаты), такие как Ca, Co, Cu и Fe.
Нитрилотриуксусная кислота коммерчески доступна в виде свободной кислоты и в виде натриевой соли. Его получают из аммиака, формальдегида и цианида натрия или цианида водорода. Мировая мощность оценивается в 100 тысяч тонн в год. NTA также образуется в качестве примеси при синтезе EDTA, возникающей в результате реакций побочного продукта аммиака.
NTA - это трипод. тетрадентат трианионный лиганд.
Использование NTA аналогично использованию EDTA, оба являются хелатирующими агентами. Он используется для смягчения воды и вместо трифосфата натрия и калия в моющих и очищающих средствах.
В одном применении NTA в качестве хелатирующего агента удаляет Cr, Cu и As из древесины, обработанной хромированным арсенатом меди.
В лаборатории, это соединение используется при комплексометрическом титровании. Вариант NTA используется для выделения и очистки белка в методе His-tag. Модифицированный NTA используется для иммобилизации никеля на твердой подложке. Это позволяет очищать белки, содержащие метку, состоящую из шести остатков гистидина на каждом конце.
Гистидин связывает металл хелаторных комплексов металлов. Ранее для этой цели использовалась иминодиуксусная кислота. Сейчас чаще используется нитрилотриуксусная кислота.
Для лабораторных применений Ernst Hochuli et al. 1987 г. связывает лиганд NTA и ионы никеля с шариками агарозы. Эта Ni-NTA агароза является наиболее часто используемым инструментом для очистки меченных им белков с помощью аффинной хроматографии.

Три вида структуры [Ni (NTA) (H 2O)2].
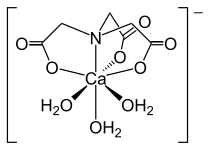
Структура нитрилотриацетат-аниона [Ca (NTA) (H 2O)3].
Нитрилоуксусная кислота может вызывать раздражение глаз, кожи и дыхательных путей, а также может вызывать повреждение почек и мочевого пузыря. Предполагается, что это соединение потенциально может вызывать рак у человека.
Напротив. до EDTA, NTA легко поддается биологическому разложению и почти полностью удаляется при очистке сточных вод. Воздействие NTA на окружающую среду минимально. Несмотря на широкое использование в чистящих средствах, концентрация в воде слишком мала, чтобы оказывать заметное воздействие на здоровье человека или окружающую среду. качество.