| H-белок расщепления глицином | |||||||||
|---|---|---|---|---|---|---|---|---|---|
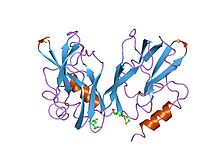 уточненные структуры при 2 ангстрем и 2,2 ангстрем двух форм h-белка, липоамидсодержащий белок глициндекарбоксилазы уточненные структуры при 2 ангстрем и 2,2 ангстрем двух форм h-белка, липоамидсодержащий белок глициндекарбоксилазы | |||||||||
| Идентификаторы | |||||||||
| Символ | GCV_H | ||||||||
| Pfam | PF01597 | ||||||||
| Pfam clan | CL0105 | ||||||||
| InterPro | IPR002930 | ||||||||
| SCOPe | 1htp / SUPFAM | ||||||||
| |||||||||
| Т-белок расщепления глицином, фолатсвязывающий домен аминометилтрансферазы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 кристаллическая структура компонента системы расщепления глицина: t-белок из pyrococcus horikoshii ot3 при 1,5 a разрешение кристаллическая структура компонента системы расщепления глицина: t-белок из pyrococcus horikoshii ot3 при 1,5 a разрешение | |||||||||
| Идентификаторы | |||||||||
| Символ | GCV_T | ||||||||
| Pfam | PF01571 | ||||||||
| Pfam clan | CL0289 | ||||||||
| InterPro | IPR006222 | ||||||||
| SCOPe | 1pj5 / SUPFAM | ||||||||
| |||||||||
| C-концевой бочкообразный домен Т-белка, расщепляемого глицином | |||||||||
|---|---|---|---|---|---|---|---|---|---|
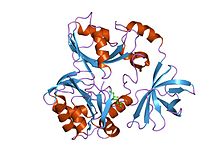 Кристаллическая структура t-белка системы расщепления глицином Кристаллическая структура t-белка системы расщепления глицином | |||||||||
| Идентификаторы | |||||||||
| Символ | GCV_T_C | ||||||||
| Pfam | PF08669 | ||||||||
| InterPro | IPR013977 | ||||||||
| SCOPe | 1pj5 / SUPFAM | ||||||||
| |||||||||
система расщепления глицином (GCS ) также известна как комплекс глициндекарбоксилазы или GDC . Система представляет собой серию ферментов, которые запускаются в ответ на высокие концентрации аминокислоты глицина. Тот же набор ферментов иногда называют глицинсинтазой, когда он работает в обратном направлении с образованием глицина. Система расщепления глицина состоит из четырех белков: Т-белка, Р-белка, L-белка и Н-белка. Они не образуют стабильного комплекса, поэтому правильнее называть его «системой», а не «комплексом». H-белок отвечает за взаимодействие с тремя другими белками и действует как челнок для некоторых промежуточных продуктов декарбоксилирования глицина. И у животных, и у растений система расщепления глицина неплотно прикреплена к внутренней мембране митохондрий. Мутации в этой ферментной системе связаны с глициновой энцефалопатией.
| Название | Номер ЕС | Функция |
|---|---|---|
| Т-белок (GCST или AMT ) | EC 2.1.2.10 | аминометилтрансфераза |
| Р-белок (GLDC ) | EC 1.4.4.2 | глициндегидрогеназа (декарбоксилирование) или просто глициндегидрогеназа. |
| L-белок (GCSL или DLD ) | EC 1.8.1.4 | известен под многими названиями, но чаще всего дигидролипоилдегидрогеназа |
| H-белок (GCSH ) | модифицирован липоевой кислотой и взаимодействует со всеми другими компонентами в цикле восстановительного метилирования (катализируемого P-белком), переноса метиламина (катализируемого T-белком) и переноса электрона (катализируемого L-белком). |
 Расщепление глицина
Расщепление глицина В у растений, животных и бактерий система расщепления глицина катализирует следующую обратимую реакцию:
В ферментативной реакции H-белок активирует P-белок, который катализирует декарбоксилирование глицина и присоединяет промежуточную молекулу к H-белку, которая перемещается к T-белку. H-белок образует комплекс с T-белком, который использует тетрагидрофолат и дает аммиак и 5,10-метилентетрагидрофолат. После взаимодействия с Т-белком в Н-белке остаются две полностью восстановленные тиоловые группы в липоатной группе. Система белков глицина регенерируется, когда H-белок окисляется с целью регенерации дисульфидной связи в активном центре за счет взаимодействия с L-белком, который восстанавливает NAD до NADH и H.
При соединении с серингидроксиметилтрансфераза, общая реакция системы расщепления глицина принимает следующий вид:
У людей и большинства позвоночных система расщепления глицина является частью наиболее заметного пути катаболизма глицина и серина. Это в значительной степени связано с образованием 5,10-метилентетрагидрофолата, который является одним из немногих доноров C 1 в биосинтезе. В этом случае метильная группа, полученная в результате катаболизма глицина, может быть передана другим ключевым молекулам, таким как пурины и метионин.
 Глицин и катаболизм серина в митохондриях и из них. Внутри митохондрий системы расщепления глицина связываются с серингидроксиметилтрансферазой в обратимом процессе, позволяющем контролировать поток в клетке.
Глицин и катаболизм серина в митохондриях и из них. Внутри митохондрий системы расщепления глицина связываются с серингидроксиметилтрансферазой в обратимом процессе, позволяющем контролировать поток в клетке. Эта реакция и, как следствие, система расщепления глицина необходимы для фотодыхания в клетке. C 3 растений. Система расщепления глицина принимает глицин, который образуется из нежелательного побочного продукта цикла Кальвина, и преобразует его в серин, который может повторно войти в цикл. Аммиак, вырабатываемый системой расщепления глицина, ассимилируется циклом глутаминсинтетазы - глутаминоксоглутарат аминотрансферазы, но стоит клетке один АТФ и один НАДФН. Положительным моментом является то, что один CO 2 вырабатывается на каждые два O 2, которые по ошибке принимаются ячейкой, генерируя некоторое значение в цикле истощения энергии в противном случае. Вместе белки, участвующие в этих реакциях, составляют примерно половину белков в митохондриях из шпината и гороха листьев. Система расщепления глицина постоянно присутствует в листьях растений, но в небольших количествах, пока они не подвергаются воздействию света. Во время пикового фотосинтеза концентрация системы расщепления глицина увеличивается в десять раз.
В анаэробных бактериях Clostridium acidiurici система расщепления глицина в основном работает в направлении синтеза глицина. Хотя синтез глицина через систему расщепления возможен из-за обратимости общей реакции, он не всегда наблюдается у животных.
Глициновая энцефалопатия, также известная как некетотическая гиперглицинемия (NKH), является первичным нарушением системы расщепления глицина, возникающим в результате снижения функции системы расщепления глицина, вызывающей повышение уровня глицина в жидкостях организма. Заболевание было впервые клинически связано с системой расщепления глицина в 1969 году. Ранние исследования показали высокий уровень глицина в крови, моче и спинномозговой жидкости. Первоначальные исследования с использованием углеродного мечения показали снижение уровней CO 2 и продукции серина в печени, что прямо указывает на недостаточность реакции расщепления глицина. Дальнейшие исследования показали, что делеции и мутации в 5'-области Р-белка являются основными генетическими причинами некетотической гиперглицинемии.. В более редких случаях было обнаружено, что миссенс-мутация в генетическом коде Т-белка, вызывающая мутацию гистидина в положении 42 в аргинин, также приводит к некетотической гипергицинемии.. Эта специфическая мутация напрямую повлияла на активный сайт Т-белка, что привело к снижению эффективности системы расщепления глицина.