| Саркомерные мышечные связки | |
|---|---|
 Изображение саркомера Изображение саркомера | |
| Подробнее | |
| Часть | поперечно-полосатой мышцы |
| Идентификаторы | |
| Латинский | саркомерум |
| MeSH | D012518 |
| TH | H2.00.05.0.00008 |
| Анатомические термины микроанатомии. [редактировать в Викиданных ] | |
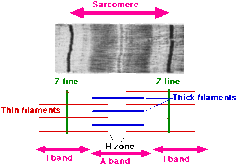
A саркомер (греч. Σάρξ sarx «плоть», μέρος meros «часть») - сложная единица поперечно-полосатой мышечной ткани. Это повторяющаяся единица между двумя линиями Z. Скелетные мышцы состоят из тубулярных мышечных клеток (миоцитов, называемых мышечных волокон или миофибр ), которые образуются в процессе, известном как миогенез. Мышечные волокна содержат многочисленные трубчатые миофибриллы. Миофибриллы состоят из повторяющихся участков саркомеров, которые под микроскопом выглядят как чередующиеся темные и светлые полосы. Саркомеры состоят из длинных волокнистых белков в виде нитей, которые скользят мимо друг друга при сокращении или расслаблении мышцы. костамер - это другой компонент, который соединяет саркомер с сарколеммой.
Двумя важными белками являются миозин, который образует толстую нить, и актин., образующий тонкую нить. Миозин имеет длинный волокнистый хвост и шаровидную головку, которая связывается с актином. Головка миозина также связывается с АТФ, который является источником энергии для движения мышц. Миозин может связываться с актином только тогда, когда сайты связывания на актине подвергаются воздействию ионов кальция.
Молекулы актина связаны с линией Z, которая образует границы саркомера. Другие полосы появляются, когда саркомер расслаблен.
Миофибриллы гладкомышечных клеток не расположены в саркомеры.
 Сокращение мышц основано на теории скользящих волокон
Сокращение мышц основано на теории скользящих волокон Именно саркомеры придают скелетным и сердечным мышцам их полосатый вид, который впервые был описан Ван Левенгук.
Взаимосвязь между белками и областями саркомера следующая:
Белок тропомиозин покрывает миозин-связывающие участки молекул актина в мышечной клетке. Чтобы мышечная клетка сократилась, тропомиозин должен быть перемещен, чтобы раскрыть участки связывания на актине. Ионы кальция связываются с молекулами тропонина C (которые рассредоточены по всему белку тропомиозина) и изменяют структуру тропомиозина, заставляя его открывать сайт связывания поперечного мостика на актине.
Концентрация кальция в мышечных клетках контролируется саркоплазматическим ретикулумом, уникальной формой эндоплазматического ретикулума в саркоплазме.
Мышечные клетки стимулируется, когда двигательный нейрон высвобождает нейромедиатор ацетилхолин, который перемещается через нервно-мышечное соединение (синапс между конечным бутоном нейрона и мышечной клеткой). Ацетилхолин связывается с постсинаптическим никотиновым рецептором ацетилхолина. Изменение конформации рецептора обеспечивает приток ионов натрия и инициирование постсинаптического потенциала действия. Потенциал действия затем проходит по Т-канальцам (поперечным канальцам), пока не достигнет саркоплазматического ретикулума. Здесь деполяризованная мембрана активирует управляемые по напряжению кальциевые каналы L-типа, присутствующие в плазматической мембране. Кальциевые каналы L-типа находятся в тесной связи с рианодиновыми рецепторами, присутствующими в саркоплазматическом ретикулуме. Входящий поток кальция из кальциевых каналов L-типа активирует рианодиновые рецепторы для высвобождения ионов кальция из саркоплазматического ретикулума. Этот механизм называется кальций-индуцированным высвобождением кальция (CICR). Неизвестно, вызывает ли открытие рианодиновых рецепторов физическое открытие кальциевых каналов L-типа или присутствие кальция. Отток кальция позволяет головкам миозина получить доступ к участкам связывания поперечного мостика с актином, что позволяет сокращать мышцы.
Сокращение мышц заканчивается, когда ионы кальция закачиваются обратно в саркоплазматический ретикулум, обеспечивая работу сократительного аппарата и, таким образом, мышечная клетка, чтобы расслабиться.
При сокращении мышцы А-полосы не изменяют своей длины (1,85 мкм в скелетных мышцах млекопитающих), тогда как I-полосы и Н-зона укорачиваются. Это приводит к сближению линий Z.
В состоянии покоя головка миозина связана с молекулой АТФ в низкоэнергетической конфигурации и не может получить доступ к сайтам связывания поперечного мостика на актин. Однако миозиновая головка может гидролизовать АТФ в аденозиндифосфат (АДФ и неорганический фосфат-ион. Часть энергии, высвобождаемой в этой реакции, изменяет форму миозиновой головки и переводит ее в высокоэнергетическую конфигурацию.. В процессе связывания с актином головка миозина высвобождает АДФ и неорганический фосфат-ион, изменяя свою конфигурацию обратно на низкоэнергетическую. Миозин остается прикрепленным к актину в состоянии, известном как окоченение, пока новый АТФ не свяжет Головка миозина. Это связывание АТФ с миозином высвобождает актин путем диссоциации поперечного мостика. Связанный с АТФ миозин готов к другому циклу, начиная с гидролиза АТФ.
Полоса А видна как темная поперечные линии через миофибриллы; I-полоса видна как слегка окрашивающиеся поперечные линии, а Z-линия видна как темные линии, разделяющие саркомеры на уровне светового микроскопа.
Большинство мышечные клетки хранят достаточно АТФ только для небольшого количества мышц. схватки. Хотя мышечные клетки также хранят гликоген, большая часть энергии, необходимой для сокращения, происходит от фосфагенов. Один такой фосфаген, креатинфосфат, используется для обеспечения АДФ с фосфатной группой для синтеза АТФ у позвоночных.
Структура саркомер влияет на его функцию несколькими способами. Перекрытие актина и миозина приводит к появлению кривой длина-напряжение, которая показывает, как уменьшается выходная мощность саркомера силы, если мышца растягивается так, что меньше поперечных мостиков может образовываться или сжиматься до тех пор, пока актиновые нити мешают друг другу. Длина актиновых и миозиновых нитей (взятая вместе как длина саркомера) влияет на силу и скорость - более длинные саркомеры имеют больше поперечных мостиков и, следовательно, большую силу, но имеют меньший диапазон укорочения. Позвоночные животные демонстрируют очень ограниченный диапазон длин саркомеров с примерно одинаковой оптимальной длиной (длина при пиковом напряжении длины) во всех мышцах человека, а также между видами. Членистоногие, однако, демонстрируют огромные различия (более семи раз) в длине саркомера как между видами, так и между мышцами у одного человека. Причины отсутствия существенной изменчивости саркомеров у позвоночных до конца не известны.
| Викискладе есть медиафайлы, связанные с Sarcomeres. |