| NOG | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||
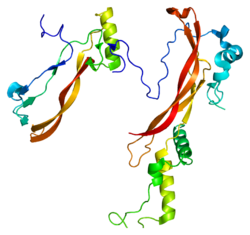
| Псевдонимы | NOG, Nog, SYM1, SYNS1, SYNS1A, noggin | ||||||||||||||||||||||||
| Внешние идентификаторы | OMIM: 602991 MGI: 104327 HomoloGene: 3979 GeneCards: NOG | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Orthologs | |||||||||||||||||||||||||
| Виды | Человек | Mouse | |||||||||||||||||||||||
| Entrez | |||||||||||||||||||||||||
| Ensembl | |||||||||||||||||||||||||
| UniProt | |||||||||||||||||||||||||
| RefSeq (мРНК) | |||||||||||||||||||||||||
| RefSeq (белок) |
Noggin, также известный как NOG, представляет собой белок, который участвует в развитии многих тканей организма, включая нервную ткань, мышцы и кости. У человека ноггин кодируется геном NOG . Аминокислотная последовательность человеческого ноггина очень гомологична таковой крысы, мыши и Xenopus (род водных лягушек). Noggin является ингибитором нескольких костных морфогенетических белков (BMP) : он ингибирует как минимум BMP2, BMP4, BMP5, BMP6, BMP7, BMP13 и BMP14. Имя белка, которое на англоязычном сленге означает «голова». ", был придуман в связи с его способностью производить эмбрионы с большими головками при воздействии высоких концентраций. Содержание
Функция Noggin - это сигнальная молекула, которая играет важную роль в продвижении сомита формирование паттерна в развивающемся эмбрионе. Он высвобождается из хорды и регулирует морфогенный белок кости (BMP4) во время развития. Отсутствие BMP4 будет вызывать формирование паттерна нервной трубки и сомитов из нервной пластинки у развивающегося эмбриона. Это также вызывает образование головы и других спинных структур. Функция ножки необходима для правильного развития нервной системы, сомитов и скелета. Эксперименты на мышах показали, что ноггин также играет роль в обучении, познании, развитии костей и сращении нервной трубки. Гетерозиготные миссенс-мутации в гене noggin могут вызывать такие деформации, как слияние суставов, и такие синдромы, как синдром множественного синостоза (SYNS1) и проксимальный симпалангизм (SIM1). SYNS1 отличается от SYM1 тем, что вызывает сращения бедра и позвоночника. У эмбриона также могут развиться более короткие кости, отсутствовать какие-либо элементы скелета или несколько суставов. Повышенные уровни Noggin в плазме наблюдались у мышей с ожирением и у пациентов с индексом массы тела более 27. Кроме того, он Было показано, что истощение Noggin в жировой ткани приводит к ожирению. Механизм действия Секретируемый полипептид noggin, кодируемый геном NOG, связывает и инактивирует членов трансформирующего фактора роста-бета. (TGF-beta ) сигнальные белки суперсемейства, такие как костный морфогенетический белок-4 (BMP4 ). Распространяясь через внеклеточные матрицы более эффективно, чем члены суперсемейства TGF-бета, ноггин может играть главную роль в создании морфогенных градиентов. Ноггин, по-видимому, обладает плейотропным эффектом как на ранней стадии развития, так и на более поздних стадиях. Модель нокаутаИсследование модели нокаута мышей отслеживало степень, в которой отсутствие мозоли влияло на эмбриологическое развитие. В центре внимания исследования было формирование уха и его роль в кондуктивной тугоухости. Внутреннее ухо подверглось множественной деформации, затронувшей улитковый канал, полукружный канал и части слуховой капсулы. Было также показано, что участие Ноггина в пороках является косвенным, через его взаимодействие с хордой и нервной осью. Перегиб хорды и дезориентация оси тела приводит к каудальному смещению плана тела эмбриона заднего мозга. Основные сигнальные молекулы из структур ромбомеров в заднем мозге не могли должным образом индуцировать образование внутреннего уха. Это отражает регуляцию BMP ноггином как основного источника деформации, а не ноггин, непосредственно влияющий на развитие внутреннего уха. Конкретные модели нокаута были созданы с использованием системы Cre-lox. Модель, выделяющая Noggin именно в адипоцитах, позволила выяснить, что Noggin также играет роль в жировой ткани: его истощение в адипоцитах вызывает изменения в структуре как коричневой, так и белой жировой ткани, наряду с дисфункцией коричневого жира (нарушение термогенеза и β-окисление ), что приводит к резкому увеличению массы тела и процентного содержания жира в организме, что вызывает изменения липидного профиля и печени; эффекты варьируются в зависимости от пола. Клиническая значимость Белки Noggin играют роль в специфическом для зародышевого листка происхождении специализированных клеток. Формирование нервных тканей, хорды, волосяных фолликулов и глазных структур происходит из зародышевого листка эктодермы. Активность ноггина в мезодерме уступает место образованию хрящей, костей и мышц, а в энтодерме ноггин участвует в развитии легких. Раннее черепно-лицевое развитие в значительной степени зависит от присутствия ноггина в соответствии с его многочисленными тканеспецифическими требованиями. Ноггин влияет на формирование и рост неба, нижней челюсти и черепа посредством взаимодействия с клетками нервного гребня. Показано, что у мышей с отсутствием гена NOG наблюдается отросток нижней челюсти и волчья пасть. Еще одна черепно-лицевая деформация, связанная с отсутствием ноггина, - это кондуктивная потеря слуха, вызванная неконтролируемым разрастанием канала улитки и его скручиванием. Недавно несколько гетерозиготных миссенс-мутаций человеческого NOG в неродственных семьях с ( SYM1) и (SYNS1) были идентифицированы; как SYM1, так и SYNS1 имеют множественное совместное слияние в качестве своей основной особенности и отображаются в той же области на хромосоме 17 (17q22), что и NOG. Эти мутации указывают на функциональную гаплонедостаточность, при которой гомозиготные формы эмбрионально летальны. Все эти мутации NOG изменили эволюционно консервативную аминокислоту остатки. Мутации в этом гене были связаны с аномалиями среднего уха. Discovery Noggin был первоначально выделен из рода водных лягушек Xenopus. Открытие было основано на способности организма восстанавливать нормальную дорсально-вентральную ось тела у эмбрионов, которые были искусственно вентрализованы обработкой УФ. Ноггин был обнаружен в лаборатории Ричарда М. Харланда и Уильяма С. Смита в Калифорнийском университете, Беркли из-за его способности вызывать образование вторичных осей у эмбрионов лягушки. Ссылки Дополнительная литература Внешние ссылки
Последняя правка сделана 2021-05-31 11:43:34
Содержание доступно по лицензии CC BY-SA 3.0 (если не указано иное). | ||||||||||||||||||||||||