 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Джевтана |
| Другие наименования | XRP-6258 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a611009 |
| Данные лицензии |
|
| Беременность. категория |
|
| Способы. введения | Внутривенное |
| Код АТС | |
| Правовой статус | |
| Правовой статус | |
| Идентификаторы | |
Имя IUPAC
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| CompTox Dashboard (EPA ) | |
| ECHA InfoCard | 100.205.741 |
| Химические и физические данные | |
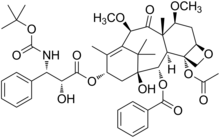
| Формула | C45H57NO14 |
| Молярная масса | 835,944 г · моль |
| 3D-модель (JSmol ) | |
SMILES
| |
InChI
| |
| (что это?) | |
Кабазитаксел, продается под торговой маркой Jevtana, является полуфабрикатом -синтетический производная от природного таксоида . Он был разработан Санофи-Авентис и был одобрен FDA США для лечения гормонорезистентного рака простаты 17 июня 2010 года. ингибитор микротрубочек и четвертый таксан, который будет одобрен в качестве противоопухолевой терапии.
Кабазитаксел в комбинации с преднизоном является вариантом лечения гормонорезистентный рак простаты после лечения доцетакселом.
Таксаны усиливают стабилизацию микротрубочек и подавляют митоз и деление клеток. Кроме того, таксаны предотвращают передачу сигналов рецептора андрогенов (AR), связывая клеточные микротрубочки и связанный с микротрубочками моторный белок динеин, тем самым предотвращая ядерную транслокацию AR.
У пациентов с метастатической резистентностью к кастрации При раке простаты (mCRPC) общая выживаемость (OS) заметно повышается при применении кабазитаксела по сравнению с митоксантроном после предшествующего лечения доцетакселом. FIRSTANA (идентификатор ClinicalTrials.gov: NCT01308567) оценила, превосходит ли кабазитаксел 20 мг / м2 (C20) или 25 мг / м2 (C25) доцетаксел 75 мг / м2 (D75) с точки зрения общей выживаемости у пациентов с мКРРПЖ, ранее не получавшими химиотерапию. Однако C20 и C25 не продемонстрировали превосходства в отношении OS по сравнению с D75 у пациентов с мКРРПЖ, не получавшими химиотерапию. Кабазитаксел и доцетаксел продемонстрировали разные профили токсичности, а C20 показал самую низкую в целом токсичность. В исследовании фазы III с участием 755 мужчин для лечения устойчивого к кастрации рака простаты средняя выживаемость составила 15,1 месяца для пациентов, получавших кабазитаксел, по сравнению с 12,7 месяцами для пациентов, получавших митоксантрон. Кабазитаксел был связан с большей частотой нейтропении 3–4 степени (81,7%), чем митоксантрон (58%). Общие побочные эффекты кабазитаксела включают нейтропению (включая фебрильную нейтропению) и побочные эффекты со стороны ЖКТ, проявляющиеся в основном при диарее, тогда как невропатия выявлялась редко.
Прием кабазитаксела вызывает снижение концентраций в плазме, что показывает трехфазная кинетика: средний период полураспада (t1 / 2) 2,6 мин в первой фазе, средний t1 / 2 1,3 часа во второй фазе и средний t1 / 2 77,3 часа в третьей фазе.
Кабазитаксел в основном метаболизируется в печени [цитохромом P450 (CYP) 3A4 / 5>CYP2C8], в результате чего образуется семь метаболитов в плазме и 20 метаболитов выводятся из организма. В течение 14 дней после приема 80% кабазитаксела выводится: 76% с калом и 3,7% через почки.
Есть много вопросов относительно оптимального использования Кабазитаксел после одобрения его использования для лечения мКРРПЖ, резистентного к доцетакселу. Один вопрос - об оптимальном использовании. Что касается значительной миелосупрессии при введении кабазитаксела в дозе 25 мг / м 2, рандомизированное исследование III фазы оценит безопасность и эффективность кабазитаксела в дозе 20 мг / м 2. Еще один вопрос касается эффективности и переносимости кабазитаксела при его применении с другими препаратами. Испытания фазы I / II проверяют совместное применение кабазитаксела с другими препаратами (например, абиратероном) и исследуемыми агентами (например, кустирсен)