 | |
 | |
| Имена | |
|---|---|
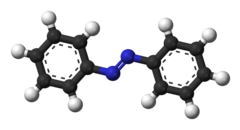
| Название ИЮПАК ( E ) -дифенилдиазен | |
| Другие названия Азобензол | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| Ссылка на Beilstein | 742610 |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100,002,820 |
| Номер ЕС | |
| Ссылка на Гмелин | 83610 |
| КЕГГ | |
| PubChem CID | |
| Номер RTECS | |
| UNII | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | C 12 H 10 N 2 |
| Молярная масса | 182,226 г моль -1 |
| Появление | оранжево-красные кристаллы |
| Плотность | 1,203 г / см 3 |
| Температура плавления | 67,88 ° C (транс), 71,6 ° C (цис) |
| Точка кипения | 300 ° С (572 ° F, 573 К) |
| Растворимость в воде | 6,4 мг / л (25 ° С) |
| Кислотность (p K a ) | -2,95 |
| Магнитная восприимчивость (χ) | -106,8 10 −6 см 3 / моль |
| Показатель преломления ( n D ) | 1,6266 (589 нм, 78 ° С) |
| Состав | |
| Молекулярная форма | sp 2 at N |
| Дипольный момент | 0 D (транс-изомер) |
| Опасности | |
| Основные опасности | ядовитый |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| Положения об опасности GHS | H302, H332, H341, H350, H373, H400, H410 |
| Меры предосторожности GHS | Р201, Р202, Р260, Р261, Р264, Р270, Р271, Р273, Р281, Р301 + 312, Р304 + 312, Р304 + 340, P308 + 313, P312, P314, P330, P391, P405, P501 |
| точка возгорания | 476 ° С (889 ° F, 749 К) |
| Родственные соединения | |
| Родственные соединения | Нитрозобензол анилин |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Азобензол является фотопереключаемым химическим соединением, состоящим из двух фенильных колец, соединенных с помощью N = N двойной связи. Это простейший пример арилазосоединения. Термин «азобензол» или просто «азо» часто используется для обозначения широкого класса подобных соединений. Эти азосоединения считаются производными диазена (диимида) и иногда называются «диазенами». Диазены сильно поглощают свет и являются обычными красителями.
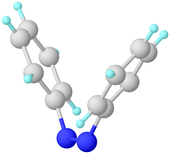 Рентгеновская кристаллография выявляет весьма неплоскую закрученную структуру цис- азобензола.
Рентгеновская кристаллография выявляет весьма неплоскую закрученную структуру цис- азобензола. транс- азобензол плоский. Расстояние NN составляет 1,189 Å. цис- азобензол неплоский с двугранным углом CN = NC, равным 173,5 °. Расстояние NN составляет 1,251 Å. Азобензол был впервые описан Эйльхардом Митчерлихом в 1834 году. Желтовато-красные кристаллические чешуйки азобензола были получены в 1856 году. Его первоначальный препарат аналогичен современному. По методу 1856 года нитробензол восстанавливают железными опилками в присутствии уксусной кислоты. В современном синтезе цинк является восстановителем в присутствии основания. Также применяется промышленный электросинтез с использованием нитробензола.
Транс-изомер более стабилен примерно на 50 кДж / моль, а барьер для изомеризации в основном состоянии составляет примерно 100 кДж / моль.
 Азобензол Фотоизомеризация. Транс - форма (слева) могут быть превращены в цис - форме (справа) с использованием УФ длиной волны 300-400 нм. Видимое освещение на длине волныgt; 400 нм переводит молекулу обратно в транс- форму. С другой стороны, молекула термически релаксирует до стабильной транс- формы.
Азобензол Фотоизомеризация. Транс - форма (слева) могут быть превращены в цис - форме (справа) с использованием УФ длиной волны 300-400 нм. Видимое освещение на длине волныgt; 400 нм переводит молекулу обратно в транс- форму. С другой стороны, молекула термически релаксирует до стабильной транс- формы.  Фотоизомеризация метоксиазобензола приводит к обратимому изменению цвета
Фотоизомеризация метоксиазобензола приводит к обратимому изменению цвета Азобензол является слабым основанием, но подвергается протонированию по одному азоту с pK a = -2,95. Он действует как основание Льюиса, например, по отношению к тригалогенидам бора. Он связывается с низковалентными металлическими центрами, например Ni (Ph 2 N 2 ) (PPh 3 ) 2 хорошо охарактеризован.
Он окисляется с образованием азоксибензола. Гидрирование дает дифенилгидразин.
Азобензол (и его производные) подвергаются фотоизомеризации в транс и цис - изомеров. цис-азобензол расслабляется обратно в темноте к транс-изомеру. Такая тепловая релаксация происходит медленно при комнатной температуре. Два изомера можно переключать с помощью определенных длин волн света: ультрафиолетового света, который соответствует запрещенной зоне перехода π-π * (состояние S 2 ), для преобразования транс-в-цис, и синего света, который эквивалентен переход n-π * (состояние S 1 ) для изомеризации из цис-в-транс. По ряду причин цис- изомер менее стабилен, чем транс (например, он имеет искаженную конфигурацию и менее делокализован, чем транс-конфигурация). Фотоизомеризация позволяет осуществлять обратимое хранение энергии (в виде фотопереключателей ).
Длины волн, при которых происходит изомеризация азобензола, зависят от конкретной структуры каждой азомолекулы, но они обычно группируются в три класса: молекулы азобензольного типа, аминоазобензолы и псевдостильбены. Эти азо желтые, оранжевые и красные, соответственно, из-за тонких различий в их электронных спектрах поглощения. Соединения, подобные незамещенному азобензолу, демонстрируют низкоинтенсивное n-π * -поглощение в видимой области и гораздо более высокую интенсивность π-π * -поглощения в ультрафиолете. Azos, которые являются орто- или пара-замещенные с донорных групп (например, аминокислот ), классифицируются как aminoazobenzenes, и, как правило, близко друг от друга п-п * и п-п * полосы в видимой области спектра. Класс псевдо-стильбенов характеризуется заменой положений 4 и 4 'двух азоколец электронодонорными и электроноакцепторными группами (то есть функционализированы два противоположных конца ароматической системы). Добавление этой двухтактной конфигурации приводит к сильно асимметричному распределению электронов, которое изменяет множество оптических свойств. В частности, он смещает спектры поглощения в транс и цис - изомеров, так что они эффективно перекрываются. Таким образом, для этих соединений одна длина волны света в видимой области будет вызывать как прямую, так и обратную изомеризацию. Под освещением эти молекулы циклически переходят между двумя изомерными состояниями.
Фотоизомеризация азобензола происходит очень быстро и в пикосекундных временных масштабах. Скорость тепловой обратной релаксации сильно варьируется в зависимости от соединения: обычно часы для молекул азобензольного типа, минуты для аминоазобензолов и секунды для псевдо-стильбенов.
Механизм изомеризации был предметом некоторых дискуссий с двумя путями, идентифицированными как жизнеспособные: вращение вокруг связи NN, с разрывом двойной связи, или через инверсию, с полулинейным и гибридным переходным состоянием. Было высказано предположение, что транс -До- цис преобразование происходит за счет вращения в S 2 состояния, в то время как инверсия приводит к цис -До- транс преобразования. Все еще обсуждается, какое возбужденное состояние играет прямую роль в ряде поведения фотоизомеризации. Однако последние исследования по фемтосекундной переходной спектроскопии предположили, что S - состояние претерпевает внутреннее преобразование в S 1 состояние, а затем транс -До- цис - изомеризация продолжается. Недавно Диау предложил другой путь изомеризации, путь «согласованной инверсии», в котором оба угла связи CNN изгибаются одновременно.
Фотоизомеризация азобензола - это форма движения молекул под действием света. Эта изомеризация также может привести к движению в больших масштабах. Например, поляризованный свет заставит молекулы изомеризоваться и релаксировать в случайных положениях. Однако те расслабленные ( транс ) молекулы, которые падают перпендикулярно поляризации входящего света, больше не смогут поглощать и останутся фиксированными. Таким образом, происходит статистическое обогащение хромофоров перпендикулярно поляризованному свету (ориентационное горение дырок). Поляризованное излучение сделает азоматериал анизотропным и, следовательно, оптически двулучепреломляющим и дихроичным. Эту фотоориентацию можно также использовать для ориентирования других материалов (особенно в жидкокристаллических системах).