 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Трисульфид мышьяка | |
| Другие имена Мышьяк ( III) сульфид. Orpiment. Сера мышьяка | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.013.744 |
| Номер EC |
|
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | As2S3 |
| Молярная масса | 246,02 г · моль |
| Внешний вид | Оранжевые кристаллы |
| Плотность | 3,43 г · см |
| Точка плавления | 310 ° C (590 ° F; 583 K) |
| Точка кипения | 707 ° C (1305 ° F; 980 K) |
| Магнитная восприимчивость (χ) | -70,0 · 10 см / моль |
| Структура | |
| Пространственная группа | P21/ n (№ 11) |
| Постоянная решетки | a = 1147,5 (5) пм, b = 957,7 (4) пм, c = 425,6 (2) пм α = 90 °, β = 90,68 (8) °, γ = 90 ° |
| Координационная геометрия | пирамидальная (As) |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H300, H331, H400, H411 |
| NFPA 704 (огненный алмаз) |  0 3 0 0 3 0 |
| NIOSH (пределы воздействия на здоровье США): | |
| PEL (Допустимо) | [1910.1018] TWA 0,010 мг / м |
| REL (рекомендуется) | Ca C 0,002 мг / м [15 минут] |
| IDLH (непосредственная опасность) | Ca [5 мг / м (в виде As)] |
| Родственные соединения | |
| Другие анионы | Триоксид мышьяка. Триселенид мышьяка |
| Другие катионы | Трисульфид фосфора. Трисульфид сурьмы. Сульфид висмута |
| Родственные соединения | Тетрасульфид тетраарьяка |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Трисульфид мышьяка является неорганическим соединение формулы As2 S3. Это темно-желтое твердое вещество, не растворимое в воде. Он также встречается в виде минерала orpiment (лат. Auripigment), который использовался в качестве пигмента, называемого королевским желтым. Производится при анализе соединений мышьяка. Это собственный полупроводник p-типа группы V / VI, который проявляет свойства фотоиндуцированного фазового перехода. Другой основной сульфид мышьяка - As 4S4, красно-оранжевое твердое вещество, известное как минерал реальгар.
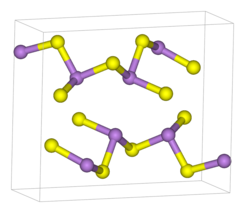
As2S3встречается как в кристаллической, так и в аморфной формах. Обе формы имеют полимерные структуры, состоящие из тригонально-пирамидальных центров As (III), связанных сульфидными центрами. Сульфидные центры двукратно координированы по двум атомам мышьяка. В кристаллической форме соединение принимает структуру взъерошенного листа. Связь между листами создается силами Ван-дер-Ваальса. Кристаллическая форма обычно встречается в геологических образцах. Аморфный As 2S3не имеет слоистой структуры, но более сшитый. Как и в других очках, здесь нет среднего или дальнего порядка, но первая координационная сфера четко определена. As 2S3является хорошим стеклообразователем и демонстрирует на его фазовой диаграмме широкую область стеклообразования.
Это полупроводник с прямой запрещенной зоной 2,7 эВ. Широкая запрещенная зона делает его прозрачным для инфракрасного между 620 нм и 11 мкм.
Аморфный As 2S3получают путем сплавления элементов при 390 ° C. При быстром охлаждении реакционного расплава получается стекло. Реакция может быть представлена химическим уравнением:
As2S3образуется, когда водные растворы, содержащие As (III), обрабатывают H 2 S. Раньше мышьяк анализировали и анализировали с помощью этой реакции, в результате чего выпадал в осадок As 2S3, который затем взвешивали. As 2S3можно даже осаждать в 6М HCl. Поскольку 2S3настолько нерастворим, что не токсичен.
При нагревании в вакууме полимерный As 2S3«трескается» с образованием смеси молекулярных частиц, включая молекулярный As 4S6. As 4S6принимает геометрию адамантана, подобную той, что наблюдается для P 4O6и As 4O6. Когда пленка из этого материала подвергается воздействию внешнего источника энергии, такого как тепловая энергия (посредством термического отжига), электромагнитное излучение (например, УФ-лампы, лазеры, электронные лучи)), As 4S6полимеризуется:
As2S3обычно растворяется при обработке водными растворами, содержащими сульфид-ионы. Растворенные частицы мышьяка представляют собой пирамидный трианион AsS. 3:
As2S3представляет собой ангидрид гипотетической тиомышьяновой кислоты, As (SH) 3. При обработке полисульфидными ионами As 2S3растворяется с образованием различных разновидностей, содержащих оба SS и связи As-S. Одно производное представляет собой S 7 As-S, кольцо, которое содержит экзоциклический сульфидоцентр, присоединенный к атому As. As 2S3также растворяется в сильнощелочных растворах с образованием смеси AsS. 3и AsO. 3.
«Обжиг» As 2S3на воздухе дает летучие токсичные производные, и это преобразование является одной из опасностей, связанных с переработкой тяжелых металлов руд :
Из-за его высокого содержания показатель преломления 2,45 и его большая твердость по Кнупу по сравнению с органическими фоторезистами. Поскольку 2S3был исследован для изготовления фотонных кристаллов с полная фотонная запрещенная зона. Достижения в технологиях лазерного формирования рисунка, таких как трехмерная прямая лазерная запись (3-D DLW) и химическое влажное травление, позволили использовать этот материал в качестве фоторезиста для изготовления трехмерных наноструктур.
As2S3исследуется на предмет использования в качестве материала фоторезиста с высоким разрешением с начала 1970-х годов с использованием водных травителей. Хотя эти водные травители позволяли изготавливать двухмерные структуры с низким аспектным соотношением, они не допускают травления структур с высоким аспектным отношением с трехмерной периодичностью. Некоторые органические реагенты, используемые в органических растворителях, обеспечивают высокую селективность травления, необходимую для создания структур с высоким аспектным отношением и трехмерной периодичностью.
As2S3и As 4S4были исследованы в качестве лечения острого промиелоцитарного лейкоза (APL).
трисульфид мышьяка, произведенный в аморфной форме, используется в качестве халькогенидного стекла для инфракрасного оптика. Он прозрачен между 620 нм и 11 мкм. Стекло с трисульфидом мышьяка более устойчиво к окислению, чем кристаллический трисульфид мышьяка, что сводит к минимуму проблемы токсичности. Его также можно использовать в качестве акустооптического материала.
Трисульфид мышьяка использовался для характерной восьмиугольной конической носовой части над инфракрасным искателем ракеты de Havilland Firestreak.
Сообщается, что древние египтяне использовали натуральный или синтетический орпимент в качестве пигмента в художественном творчестве и косметике.
Трисульфид мышьяка также используется в качестве дубильного агента. Ранее он использовался с красителем индиго для производства синего карандаша, что позволяло добавлять темно-синие оттенки к ткани с помощью карандаша или кисти.
Осаждение трисульфида мышьяка используется в качестве аналитического теста на присутствие диссимиляционных сокращающих мышьяк бактерий (DARB).
As2S3настолько нерастворим, что его токсичность невысока. Старые образцы могут содержать значительные количества оксидов мышьяка, которые растворимы и поэтому очень токсичны.
Орпимент встречается в вулканической среде, часто вместе с другими сульфидами мышьяка, в основном реалгаром. Иногда встречается в низкотемпературных гидротермальных жилах вместе с некоторыми другими сульфидными и сульфосолевыми минералами.