Серотонин 5-HT 2 рецепторы стимулируются моноаминовыми нейротрансмиттерами, включая серотонин, дофамин и норэпинефрин. Стимуляция 5-HT 2 рецептора вызывает накопление внутриклеточного инозитолтрифосфата и, таким образом, увеличение цитозольного Ca. 5-HT 2C рецептор агонисты являются привлекательными мишенями для лекарств, которые могут быть использованы при лечении ряда состояний, включая ожирение, психические расстройства, сексуальная дисфункция и недержание мочи.
5-HT 2C рецепторы являются одним из трех подтипов, которые относятся к к подсемейству рецепторов серотонина 5-HT 2 вместе с рецепторами 5-HT 2A и 5-HT 2B. Разработка агонистов 5-HT 2C была серьезным препятствием из-за серьезных побочных эффектов из-за отсутствия селективности в отношении 5-HT 2A и 5-HT 2B рецепторы. Активация рецепторов 5-HT 2A может вызывать галлюцинации, а активация рецепторов 5-HT 2B связана с клапанной недостаточностью сердца и, возможно, с легочной гипертензией.
В конце 1960-х гг. неселективные антагонисты рецепторов серотонина продемонстрировали взаимосвязь между рецепторами серотонина и потреблением пищи. Позже исследования на животных показали, что агонисты серотониновых рецепторов могут действовать как медиатор насыщения. Серотонин был задействован в качестве критического фактора в краткосрочной регуляции приема пищи и в способствовании потере веса, связанной с гиперфагией. Исследования с использованием фармакологических и генетических инструментов продемонстрировали, что подтип рецептора 5-HT 2C был одним из основных медиаторов, через которые серотонин оказывает свое аноректическое действие у грызунов. Впоследствии эти рецепторы стали многообещающей фармакотерапевтической мишенью для дальнейших исследований по лечению ожирения. Разработка мышей с нокаутом по 5-HT 2C рецепторам в середине 1990-х годов была выдающимся достижением в идентификации и разработке серотонинергических препаратов для похудания. Эти нокаутные мыши были гиперфагическими, что приводило к ожирению, частичной устойчивости лептину, увеличению отложения жира, инсулинорезистентности и нарушению толерантности к глюкозе. В результате этих симптомов исследователи определили функциональную роль рецепторов в серотонинергической регуляции приема пищи и веса тела. Позже рецепторы 5-HT 2C были предложены в качестве терапевтической мишени для лечения множественных расстройств центральной нервной системы (ЦНС), включая психические расстройства, ожирение, сексуальную дисфункцию и недержание мочи.
Агонист рецептора 5-HT2c фенфлурамин (торговые названия Pondimin, Ponderax и Adifax) был открыт в 1972 году в результате исследования, проведенного с целью выявления аноректических соединений, не обладающих действием психостимуляторов. и симпатомиметические агенты (такие как амфетамины). До открытия фенфлурамина амфетамины были основной формой доступных аноректических препаратов, однако из-за побочных эффектов их было трудно использовать. Аноректический эффект фенфлурамина достигается за счет повышения уровня серотонина, вызывающего ощущение сытости, что приводит к снижению потребления пищи. Фенфлурамин продавался в виде рацемической смеси двух энантиомеров, дексфенфлурамина и левофенфлурамина.
. В 1994 году продажи комбинированного препарата Fen -фен (фенфлурамин и фентермин ) резко увеличивалось, поскольку эта комбинация давала существенный и очевидный синергетический эффект, способствующий снижению веса. Впоследствии сообщения о серьезных побочных эффектах, связанных с аномалиями сердечного клапана и повышенным риском легочной гипертензии, привели к решению удалить продукты, содержащие фенфлурамин, с рынка США, а затем с других рынков по всему миру.
Дексфенфлурамин ингибирует. серотонин обратный захват, стимулирующий высвобождение серотонина. В 1996 году дексфенфлурамин стал первым препаратом для долгосрочного лечения от ожирения, одобренным в США; побочные эффекты, наблюдаемые во время клинических испытаний, включали сухость во рту, диарею и сонливость. В середине 1990-х годов FDA США одобрило дексфенфлурамин в качестве препарата для похудания. После нескольких сообщений о неблагоприятных сердечно-сосудистых эффектах FDA запретило дексфенфлурамин в 1997 году.
Похоже, что рецепторы 5-HT 2B, экспрессируемые в сердечных клапанах, ответственны за вальвулопатии. сообщается об использовании фенфлурамина и дексфенфлурамина.
Агонист серотонинового рецептора mCPP имеет значительное сродство к рецепторам 5-HT 2C. Пациенты с mCPP испытывают множественные побочные эффекты из-за неселективности в отношении рецепторов 5-HT 2A и 5-HT 2B. Отсутствие гипофагического (снижение потребления пищи) эффекта mCPP у мышей с нокаутом рецептора 5-HT 2C предполагает, что этот эффект опосредуется активацией рецептора 5-HT 2C. Повторное введение mCPP людям может привести к снижению потребления пищи и потере веса. mCPP используется в качестве прототипа исследовательского инструмента для открытия лекарств селективных агонистов рецепторов 5-HT 2C.
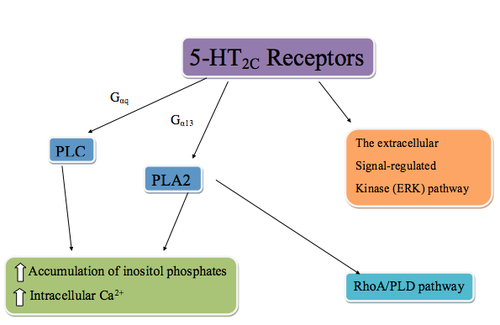 Рисунок 1 - Механизм действия. Гипотетический модель активации агонистом рецептора 5-HT 2C. Активация приводит к накоплению инозитолфосфата и увеличению внутриклеточного Ca. Активация рецептора также стимулирует путь ERK и путь RhoA / PLD.
Рисунок 1 - Механизм действия. Гипотетический модель активации агонистом рецептора 5-HT 2C. Активация приводит к накоплению инозитолфосфата и увеличению внутриклеточного Ca. Активация рецептора также стимулирует путь ERK и путь RhoA / PLD. Рецепторы 5-HT2C представляют собой рецепторы, связанные с G-белком, которые связаны с фосфолипазой C (PLC) через Gαq, фосфолипазу A2 (PLA2) и, возможно, Gα13. PLC метаболизирует фосфатидилинозитол-4,5-бисфосфат в инозитол-1,4,5-трифосфат (IP3). IP3 регулирует клеточный поток Ca, связываясь с рецепторами IP3, вызывая высвобождение Ca2 +. Кроме того, активация PLA2 также приводит к привлечению пути RhoA / PLD через RhoA, фермент, который регулирует широкий спектр клеточных функций через белок-мишень PLD (фосфолипаза D ).. Рецепторы 5-HT 2C могут также стимулировать путь регулируемой внеклеточными сигналами киназы (ERK), который активируется нейротрофинами и другими нейроактивными химическими веществами. Производство этих химических веществ влияет на дифференцировку нейронов, выживаемость, регенерацию, а также структурную и функциональную пластичность. Ранние исследования пути ERK показали, что стабилизаторы настроения для лечения маниакально-депрессивного заболевания стимулировали этот путь. Это привело к пониманию того, что стимуляция рецепторов 5-HT 2C может регулировать маниакально-депрессивные состояния аналогично стабилизаторам настроения.
5-HT 2C рецепторы расположены только в ЦНС, где их можно найти в нескольких местах. Наибольшая плотность экспрессии рецептора находится в пределах сосудистого сплетения. Другие местоположения головного мозга включают ядро единственного тракта, дорсомедиальный гипоталамус, паравентрикулярное ядро гипоталамуса и миндалевидное тело, все из которых связаны с регулированием приема пищи. Этот паттерн распределения может объяснить влияние, которое они оказывают на интегральную функцию в контроле многих физиологических и поведенческих реакций, таких как кормление, беспокойство, регулирование температуры, передвижение, сексуальное поведение и возникновение судорог.
 Рисунок 2. Схематическое изображение модели двух состояний, в которой 5-HT 2C рецептор находится в равновесии между активным состоянием (R *) и неактивным состоянием (R).
Рисунок 2. Схематическое изображение модели двух состояний, в которой 5-HT 2C рецептор находится в равновесии между активным состоянием (R *) и неактивным состоянием (R). 5-HT 2 рецепторы являются рецепторами, связанными с G-белком, которые могут регулировать клеточную передачу сигналов в отсутствие лиганда . Это можно объяснить с помощью модели с двумя состояниями (рис. 2), где рецептор находится в равновесии между двумя состояниями, активным состоянием (R *) и неактивным состоянием (R). Базальная эффекторная активность частично определяется абсолютным уровнем (R *), который будет увеличиваться с увеличением плотности рецепторов. Лиганды, которые предпочтительно связываются и стабилизируют R-состояние, называются обратными агонистами и снижают эффекторную активность. Агонисты предпочтительно связываются и стабилизируют состояние R *, тем самым увеличивая эффекторную активность. Нейтральные антагонисты проявляют одинаковое сродство к обеим конформациям и не изменяют равновесия между двумя состояниями, однако они занимают рецептор и могут блокировать действие как агонистов, так и обратных агонистов.
5-HT 2C и 5-HT 2A рецепторы имеют сходную гомологию аминокислотных последовательностей, с ~ 50% общей идентичностью последовательностей и ~ 80% внутри TM-доменов, что приводит к аналогичному фармакологическому профилю для двух рецепторов. Оба рецептора связывают одни и те же пути передачи клеточного сигнала, PLC и PLA2, которые приводят к накоплению инозитолфосфата и Са в постсинаптической клетке.
Рецепторы 5-HT 2C являются единственными G -белковые рецепторы, которые, как известно, подвергаются посттранскрипционному процессу редактирования РНК. Ген рецептора 5-HT 2C обнаружен на Х-хромосоме, Xq24. Этот генный продукт подвергается процессу редактирования РНК, что приводит к снижению аффинности связывания агониста, однако связывание антагониста остается неизменным. Этот процесс редактирования РНК генерирует 14 уникальных изоформ рецептора 5-HT 2C рецептора, которые различаются тремя аминокислотами во второй внутриклеточной петле.
Серотонин является одним из эндогенный неселективный агонист рецептора 5-HT 2C с константой связывания K i = 16,0 нМ. Когда серотонин связывается с рецепторами, наиболее важные контакты находятся в спиралях 3, 5 и 6 TM (рис. 3), тогда как другие четыре спирали TM не взаимодействуют напрямую с соединением серотонина. Когда происходит связывание серотонина, протонированный сайт первичного амина образует солевой мостик с остатком D134 в TM 3, а также образует водородную связь с остатком S138 в TM 3. ароматическое индольное кольцо образует сильное ван-дер-ваальсово взаимодействие с остатками F223 в TM 5 и F328 в TM 6. Кольцо плотно входит в карман рецептора, укладываясь между двумя фенилаланинами.. Амин индольной группы образует водородную связь с остатком S219 в TM 5, а гидроксидный заместитель индола образует водородные связи как с остатком S131 в TM 3, так и с I332 в TM 6. Также существует сильное ван-дер-ваальсово взаимодействие между индолом и I332 в TM 6.
 Рисунок 3. Краткое описание рецептора 5-HT 2C. Наиболее важные контакты при связывании серотонина связаны с остатками в спиралях 3, 5 и 6.
Рисунок 3. Краткое описание рецептора 5-HT 2C. Наиболее важные контакты при связывании серотонина связаны с остатками в спиралях 3, 5 и 6. 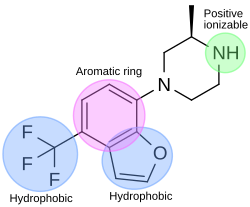 Рисунок 4. Наилучшее соответствие, сопоставленное с четырьмя характеристиками фармакофоров.
Рисунок 4. Наилучшее соответствие, сопоставленное с четырьмя характеристиками фармакофоров. В процессе открытия лекарств агониста 5-HT 2C, модуля фармакофор использовали для открытия новых лигандов рецептора 5-HT 2C. Фармакофор имеет четыре функции; одно ароматическое кольцо, два гидрофобных элемента и один положительно ионизируемый элемент. На Фиг.4 показан пример соединения, которое идеально подходит для фармакофора-агониста. Атом азота пиперазина соответствует положительному ионизируемому признаку, бензофурановая часть соответствует ароматическому кольцу и одному гидрофобному, а трифторметановая часть соответствует другому гидрофобному признаку фармакофора.
В виртуальном экране для новых агонистов, взаимосвязь структура-активность определялась по наиболее сильным идентифицированным соединениям («совпадениям»). Эти хиты содержали пиразоло [3,4-d] пиримидиновое ядро (показано на фиг. 5), которое важно для эффективности по отношению к рецепторам 5-HT 2C. Соединения с максимальной эффективностью содержат два заместителя, связанных со структурой ядра. Первый заместитель представляет собой пиперазиновое кольцо, содержащее небольшую гидрофобную группу; второй заместитель представляет собой фенильную часть, содержащую галоген- и / или кислородсодержащую боковую цепь (электроотрицательные группы), см. производные 1 и 2 на рисунке 5. Добавление ароматических групп к пиперазиновому кольцу снижает эффективность (производное 4 на рисунке 5) и отсутствие пиперазинового кольца или замещение другими алифатическими - или циклическими группами также снижает эффективность (производные 5 и 6 на рисунке 5).
![Пиразоло [ 3,4-d] пиримидиновое ядро ](http://upload.wikimedia.org/wikipedia/commons/thumb/8/8d/5-HT2C-hit-general.svg/157px-5-HT2C-hit-general.svg.png) Пиразоло [3,4-d] пиримидиновое ядро
Пиразоло [3,4-d] пиримидиновое ядро 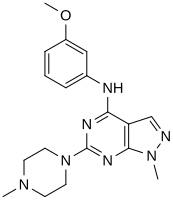 Производное 1
Производное 1 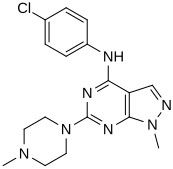 Производное 2
Производное 2 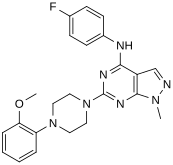 Производное 3
Производное 3  Производное 4
Производное 4 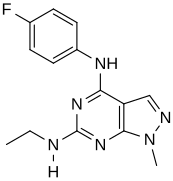 Производное 5 Рисунок 5. Производные пиразоло [3,4-d] пиримидина.
Производное 5 Рисунок 5. Производные пиразоло [3,4-d] пиримидина.  Рисунок 6. Лорказерин ((1R) -8-хлор-1-метил-2,3,4,5-тетрагидро-1H-3-бензазепин).
Рисунок 6. Лорказерин ((1R) -8-хлор-1-метил-2,3,4,5-тетрагидро-1H-3-бензазепин).  mCPP (мета-хлорфенилпиперазин)
mCPP (мета-хлорфенилпиперазин)  Мощное производное mCPP (4- (3-хлорфенил) -1,2,3,6-тетрагидропиридин) Рис. 7. mCPP и сильнодействующее производное.
Мощное производное mCPP (4- (3-хлорфенил) -1,2,3,6-тетрагидропиридин) Рис. 7. mCPP и сильнодействующее производное. Ряд производных 3-бензазепина, таких как Лорказерин (рис. 6) оценивали на предмет их активности и селективности в отношении 5-HT 2C рецепторов. Лорказерин является очень сильным агонистом, но его эффективность зависит от присутствия хлорзаместителя в положении 8.
Арилпиперазинсодержащие соединения, такие как mCPP (рис. 7), проявляют хорошую эффективность в отношении 5-HT 2C рецепторов, но не обладают достаточной селективностью в отношении рецепторов 5-HT 2C по сравнению с двумя другими подтипами рецепторов. Многие производные были исследованы в попытке повысить селективность. Производные, не содержащие арилпиперазинового ядра, такие как аналоги хлора 4-арил-1,2,3,6-тетрагидропиридина, более благоприятны по эффективности и селективности по сравнению с двумя другими рецепторами (рис. 7).
В 2016 году было опубликовано открытие новых агонистов рецепторов 5-HT 2C, связанных с белком G.
Ожирение - это глобальная эпидемическая проблема здравоохранения, и ей уделяется значительное внимание как серьезной опасности для населения. Ожирение - это хроническое патологическое и дорогостоящее заболевание аномального или чрезмерного накопления жира в организме.
Исследования показывают, что активация рецептора 5-HT 2C регулирует аппетит и потребление пищи, скорее всего, за счет насыщение через подавление аппетита путем активации 5-HT 2C. Следовательно, для лечения ожирения разрабатываются селективные агенты с высоким сродством к этому рецептору по сравнению с 5-HT 2B и 5-HT2 2A.
Лорказерин - единственный препарат, прошедший фазу III клинических испытаний и получивший одобрение Управления по контролю за продуктами и лекарствами США (FDA). Однако позже он был снят с продажи в феврале 2020 года из-за более высокого риска злокачественных новообразований в рандомизированном исследовании лорказерина. Ранее одобренные агенты были впоследствии удалены с рынка США.
Лорказерин является полным агонистом рецепторов 5-HT 2C и 5-HT 2B и частичным агонист рецепторов 5-HT 2A (75% максимального ответа, вызванного серотонином). Лорказерин является сильнодействующим и селективным агонистом 5-HT 2C с быстрым пероральным всасыванием, что показывает дозозависимое снижение потребления пищи и веса тела. Лорказерин влияет на массу тела, создавая отрицательный энергетический баланс за счет уменьшения потребления пищи (потребления энергии) без изменения расхода энергии и окисления субстрата . Лорказерин имеет высокое сродство к рецепторам 5-HT 2C, с 18-кратной селективностью по отношению к рецепторам 5-HT 2A и в 104 раза по сравнению с рецепторами 5-HT 2B <175.>рецепторы. Прогнозируемая концентрация в крови для стимуляции рецепторов 2A и 2B примерно в 1400 раз для 2B и в 250 раз для 2A, выше концентрации в крови, необходимой для стимуляции рецепторов 2C. Эта функциональная избирательность имеет решающее значение для предотвращения потенциальных побочных эффектов и предполагает, что теоретический риск сердечной вальвулопатии очень низок. Клинические испытания подтвердили эту теорию, поскольку они не выявили каких-либо побочных эффектов на сердечные клапаны или давление в легочной артерии, как у прежних препаратов от ожирения. Лорказерин в целом хорошо переносится, но наиболее частыми побочными эффектами являются головная боль, тошнота и головокружение.
Серотонин играет важную роль во многих физиологических состояниях. Антагонисты рецептора 5-HT 2 известны давно, но в последнее время агонисты рецептора 5-HT 2 становятся многообещающими агентами при разработке новых антипсихотических препаратов. Исторически сложилось так, что большинство фармакологических исследований антипсихотических препаратов сосредоточено на подтипе рецептора 5-HT 2A. Однако недавние исследования показывают, что агонистическая активность рецепторов 5-HT 2A может вызывать галлюцинации. Сравнение СИОЗС и агонистов рецептора 5-HT 2C показало, что агонисты уменьшали время неподвижности и увеличивали время плавания в FST (тест принудительного плавания ) у крыс. способом, сопоставимым с СИОЗС. В 1990-е гг. Рецепторы 5-HT 2C привлекали больше внимания, поскольку многие исследования показали, что селективные агонисты рецепторов 5-HT 2C могут быть более подходящими для лечения психотических симптомов.
Можно ожидать, что агонист 5-HT 2C уменьшит положительные симптомы шизофрении за счет уменьшения высвобождения дофамина в мезолимбическом пути дофамина. Вабиказерин (SCA-136) представляет собой агонист 5-HT 2C, который показал себя многообещающим в предварительных испытаниях для лечения шизофрении.
Вабиказерин имеет высокое сродство к рецепторам 5-HT 2C и низкое сродство к рецепторам 5-HT 2B и 5-HT 2A. Вабиказерин является полным агонистом с примерно в 4 раза большей селективностью в отношении 5-HT 2C по сравнению с этими родственными рецепторами с точки зрения аффинности связывания. Вабикаксерин является полным агонистом, стимулирующим рецептор 5-HT 2C ; это было обнаружено, когда класс слитых с тетрагидрохинолином диазепинов исследовался как возможные сильные агонисты рецептора 5-HT 2C.
По состоянию на 2012 год вабиказерин находится в клинических условиях испытания по лечению шизофрении. Длительное введение вабиказерина значительно уменьшило количество спонтанно активных мезокортиколимбических дофаминовых нейронов, не затрагивая нигростриатные дофаминовые нейроны, что согласуется с эффектами атипичных антипсихотических агентов. Результаты клинических исследований вабиказерина могут выявить, могут ли рецепторы 5-HT 2C быть возможными мишенями для лечения шизофрении.
Арипипразол также является частичным агонистом рецептора 5HT2C.
Сообщалось, что активация подтипа рецептора 5-HT 2C опосредует многочисленные эффекты, такие как эрекция полового члена. Результаты, основанные на многочисленных исследованиях, показывают, что несколько агонистов рецепторов 5-HT 2C, включая mCPP и YM348, вызывают эрекцию полового члена у крыс, но mCPP, по-видимому, имитирует оба вазодилатацию и сужение сосудов. Сосудорасширяющее действие опосредуется рецепторами 5-HT 1D, тогда как эффект сужения сосудов включает активацию рецептора 5-HT 2. YM-348 является высокоселективным 5 -HT 2C агонист, и результаты показывают, что YM348 может вызывать эрекцию полового члена и гиполокомоцию (вызываемую высокой дозой) у крыс, как и другие 5-HT 2C агонисты рецепторов. Эти эффекты полностью подавлялись селективным антагонистом рецептора 5-HT 2C, SB-242,084. Таким образом, результаты показывают, что YM348 является сильнодействующим и орально активным агонистом рецепторов 5-HT 2C.
Серотонин играет ключевую роль в механизмах, участвующих в мочеиспускание и воздержание. Было синтезировано много сильнодействующих соединений с высокой селективностью в отношении рецепторов 5-HT 2C, которые являются многообещающими кандидатами для дальнейшей разработки для лечения стрессового недержания мочи (SUI).
Многие экзогенные агенты были разработаны с момента открытия рецепторов 5-HT 2C. К настоящему времени небольшое количество агонистов с достаточной селективностью в отношении рецепторов 5-HT 2C по сравнению с другими подтипами было изучено в клинических испытаниях. Множество других агонистов рецепторов 5-HT 2C остаются в доклинической разработке, включая Ro60-0175, WAY-163,909 и обратный агонист SB-243,213. Доказательства подтверждают терапевтический потенциал модуляции рецептора 5-HT 2C при лечении различных патологических состояний, включая шизофрению, ожирение, недержание мочи и сексуальную дисфункцию.
| Название соединения | Химическое название | Способ действия | Компания | Фаза разработки | Показание | Ссылка |
|---|---|---|---|---|---|---|
| Н / Д | Агонист 5-HT2C | Проксимагер | Фаза III (2011) | Ожирение и диабет | ||
| Вабиказерин | (9aR, 12aS) - 4,5,6,7,9,9a, 10,11,12,12а-декагидроциклопента [c] [1,4] диазепино [6,7, 1-ij] хинолин | 5-HT2C агонист | Pfizer | Фаза I (28 февраля 2012 г.) | Шизофрения | |
| Лорказерин | 1R) -8-хлор-2,3, 4,5-тетрагидро-1-метил-1H-3-бензазепин | агонист 5-HT2C | Arena Pharmaceuticals | одобрен FDA (27 июня 2012 г.) | Ожирение |