 | |||
| |||
| Названия | |||
|---|---|---|---|
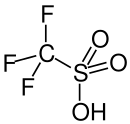
| Название IUPAC Трифторметансульфоновая кислота | |||
| Другие названия Трифликовая кислота | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.014.625 | ||
| PubChem CID | |||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКА
| |||
| Свойства | |||
| Химическая формула | CF3SO3H | ||
| Молярная масса | 150,07121 г / моль | ||
| Внешний вид | Бесцветная жидкость | ||
| Плотность | 1,696 г / мл | ||
| Точка плавления | -40 ° C (-40 ° F; 233 K) | ||
| Температура кипения | 162 ° C (324 ° F; 435 K) | ||
| Растворимость в воде | Смешиваемость | ||
| Кислотность (pK a) | -14,7 (± 2,0) | ||
| Основание конъюгата | Трифлат-анион | ||
| Опасности | |||
| Основные опасности | Сильная кислота | ||
| NFPA 704 (огненный алмаз) |  0 4 1 КИСЛОТА 0 4 1 КИСЛОТА | ||
| Кроме где указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на ink | |||
 Трифторметансульфоновая кислота
Трифторметансульфоновая кислота Трифторметансульфоновая кислота, это сокращенное название для трифторметансульфоновой кислоты, TFMS, TFSA, HOTf или TfOH, представляет собой сульфоновую кислоту с химической формулой CF 3SO3H. Это одна из самых сильных кислот. Трифликовая кислота в основном используется в исследованиях как катализатор для этерификации. Это гигроскопическая, бесцветная, слегка вязкая жидкость, растворимая в полярных растворителях.
Трифторметансульфоновая кислота промышленно производится посредством электрохимического фторирования ( ECF) метансульфоновой кислоты :
Полученный CF 3SO2F гидролизуется, и полученный трифлатная соль предварительно протонирована. Альтернативно, трифторметансульфоновая кислота образуется окислением трифторметил сульфенилхлорида :
Трифликовую кислоту очищают дистилляцией из трифликового ангидрида.
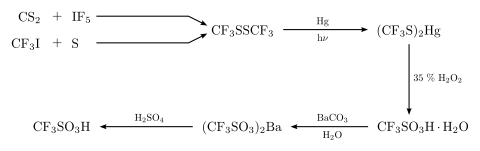
Трифторметансульфоновая кислота была впервые синтезирована в 1954 году Робертом Хаселдином и Киддом следующим образом реакция:
В лаборатории трифликовая кислота полезна при протонировании, поскольку основание конъюгата трифликовой кислоты ненуклеофильно. Он также используется в качестве кислотного титранта при неводном кислотно-основном титровании, поскольку он ведет себя как сильная кислота во многих растворителях (ацетонитрил, уксусная кислота и т. Д.), Где обычные минеральные кислоты ( такие как HCl или H 2SO4) только умеренно сильны.
При Ka = 5 × 10, pK a -14,7 ± 2,0 трифликовая кислота квалифицируется как суперкислота. Многие из своих полезных свойств он обязан своей высокой термической и химической стабильности. И кислота, и ее сопряженное основание CF3SO. 3, известное как трифлат, сопротивляются реакциям окисления / восстановления, тогда как многие сильные кислоты являются окисляющими, например хлорная или азотная кислота. Далее рекомендуется использование трифликовой кислоты, которая не сульфирует субстраты, что может быть проблемой с серной кислотой, фторсерной кислотой и хлорсульфоновой кислотой. Ниже приводится прототипное сульфирование, которому не подвергается HOTf:
Пары трифликовой кислоты во влажном воздухе образуют стабильный твердый моногидрат, CF 3SO3H · H 2 O, точка плавления 34 ° C.
Трифлатный лиганд является лабильным, что отражает его низкую основность. Трифторметансульфоновая кислота экзотермически реагирует с карбонатами, гидроксидами и оксидами металлов. Иллюстративным является синтез Cu (OTf) 2.
Хлоридные лиганды могут быть преобразованы в соответствующие трифлаты:
Это преобразование проводят в чистом HOTf при 100 ° C с последующим осаждением соли при добавлении эфира.
Трифликовая кислота реагирует с ацилгалогенидами с образованием смешанных трифлатных ангидридов, которые являются сильными ацилирующими агентами, например, в реакциях Фриделя – Крафтса.
Трифликовая кислота катализирует реакцию ароматических соединений с сульфонилхлоридами, вероятно, также через посредство смешанного ангидрида сульфоновой кислоты.
Трифликовая кислота способствует другим реакциям типа Фриделя – Крафтса, включая крекинг алканов и алкилирование алкенов, которые ch очень важны для нефтяной промышленности. Эти катализаторы на основе производных трифликовой кислоты очень эффективны при изомеризации углеводородов с прямой или слегка разветвленной цепью, которые могут повышать октановое число конкретного топлива на нефтяной основе.
Трифликовая кислота экзотермически реагирует со спиртами с образованием простых эфиров и олефинов.
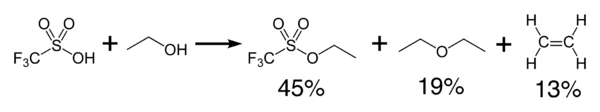
Дегидратация дает ангидрид кислоты, ангидрид трифторметансульфоновой кислоты, (CF 3SO2)2O.
Трифликовая кислота является одной из сильнейшие кислоты. Контакт с кожей вызывает тяжелые ожоги с замедленным разрушением тканей. При вдыхании вызывает смертельные спазмы, воспаление и отек.
Добавление трифликовой кислоты к полярным растворителям может быть опасно экзотермическим.