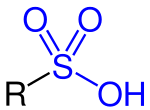
 Общая структура сульфоновой кислоты с функциональной группой, указанной синим цветом
Общая структура сульфоновой кислоты с функциональной группой, указанной синим цветом Сульфокислоты (или сульфокислоты) относится к члену класса сероорганических соединений с общей формулой R-S (= O) 2 -OH, где R представляет собой органический алкил или арил группу и S (= O) 2 (ОН) группа гидроксид сульфонила. В качестве заместителя он известен как сульфогруппа. Сульфоновая кислота может рассматриваться как серная кислота с одной гидроксильной группой, замещенной органическим заместителем. Исходное соединение (с органическим заместителем, заменен водородом) является родительской сульфокислотой, HS (= O) 2 (ОН), А таутомер из сернистой кислоты, S (= O) (ОН) 2. Соли или сложные эфиры сульфоновых кислот называются сульфонатами.
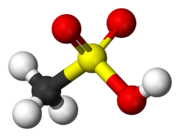 Шариковая модель метансульфоновой кислоты.
Шариковая модель метансульфоновой кислоты. Сульфоновые кислоты производятся путем сульфирования. Обычно сульфирующим агентом является триоксид серы. Широкомасштабным применением этого метода является производство алкилбензолсульфоновых кислот :
В этой реакции триоксид серы является электрофилом, а арен подвергается электрофильному ароматическому замещению. Прямое сульфирование также превращает метансульфоновую кислоту в метандисульфоновую кислоту.
Многие алкансульфоновые кислоты получают из бисульфита, который присоединяется к концевым алкенам или алкилируется алкилгалогенидами:
Сульфоновые кислоты можно получить окислением тиолов:
Такой путь лежит в основе биосинтеза таурина.
Многие сульфоновые кислоты получают гидролизом сульфонилгалогенидов и родственных предшественников. Таким образом, перфтороктансульфоновая кислота получается гидролизом сульфонилфторида, который, в свою очередь, образуется при электрофторировании октансульфоновой кислоты. Аналогичным образом сульфонилхлорид, полученный из полиэтилена, гидролизуется до сульфоновой кислоты. Эти сульфонилхлориды образуются в результате свободнорадикальных реакций хлора, диоксида серы и углеводородов с использованием реакции Рида.
Винилсульфоновая кислота получается гидролизом карбилсульфата (C 2 H 4 ( SO 3) 2), который, в свою очередь, получается добавлением триоксида серы к этилену.
Сульфоновые кислоты - сильные кислоты. Они обычно упоминаются как примерно в миллион раз сильнее, чем соответствующая карбоновая кислота. Например, п- толуолсульфоновая кислота и метансульфоновая кислота имеют значения p K = -2,8 и -1,9, соответственно, тогда как значения p K для бензойной кислоты и уксусной кислоты составляют 4,20 и 4,76 соответственно. Однако из-за высокой кислотности их значения p K a не могут быть измерены напрямую, и обычно приводимые значения следует рассматривать как косвенные оценки со значительной неопределенностью. Например, из различных источников сообщается, что pK a метансульфоновой кислоты составляет от -0,6 до -6,5. Известно, что сульфоновые кислоты реагируют с твердым хлоридом натрия ( солью ) с образованием сульфоната натрия и хлористого водорода. Это свойство подразумевает кислотность в пределах двух или трех порядков по сравнению с кислотностью HCl (г), чей p K a был недавно точно определен (p K a aq = -5,9).
Из-за своей полярности сульфоновые кислоты обычно представляют собой твердые кристаллические вещества или вязкие высококипящие жидкости. Они также обычно бесцветны и не окисляют, что делает их пригодными для использования в качестве кислотных катализаторов в органических реакциях. Их полярность в сочетании с их высокой кислотностью делает короткоцепочечные сульфоновые кислоты водорастворимыми, в то время как длинноцепочечные сульфоновые кислоты проявляют свойства, подобные детергентам.
Строение сульфоновых кислот поясняется прототипом метансульфоновой кислоты. Группа сульфоновой кислоты, RSO 2 OH, имеет тетраэдрический серный центр, что означает, что сера находится в центре четырех атомов: трех атомов кислорода и одного углерода. Общая геометрия серного центра напоминает форму серной кислоты.
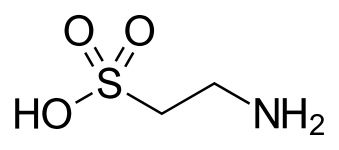
Таурин, желчная кислота и одна из немногих встречающихся в природе сульфоновых кислот (показаны в необычном таутомере ).

ПФОС, поверхностно-активное вещество и загрязнитель, вызывающий споры.

п- Толуолсульфоновая кислота, широко используемый реагент в органическом синтезе.

Нафион, полимерная сульфоновая кислота, используемая в топливных элементах.
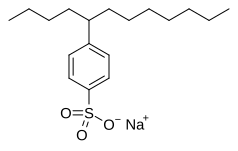
Додецилбензолсульфонат натрия, алкилбензолсульфонатное поверхностно-активное вещество, используемое в моющих средствах для стирки.

Коэнзим-М - кофактор, необходимый для биосинтеза метана, содержащегося в природном газе.
Хотя известны как алкил, так и арилсульфоновые кислоты, большинство применений связано с ароматическими производными.
Моющие и поверхностно-активные вещества - это молекулы, которые объединяют сильно неполярные и высокополярные группы. Традиционно популярными поверхностно-активными веществами являются мыла, получаемые из жирных кислот. С середины 20 века использование сульфоновых кислот превзошло использование мыла в развитых обществах. Например, около 2 миллиардов килограммов алкилбензолсульфонатов ежегодно производятся для различных целей. Сульфонаты лигнина, полученные сульфированием лигнина, входят в состав буровых растворов и добавок в определенные виды бетона.
Многие, если не большинство антрахиноновых красителей производятся или обрабатываются путем сульфирования. Сульфоновые кислоты, как правило, прочно связываются с белками и углеводами. По этой причине большинство «смываемых» красителей являются сульфоновыми кислотами (или имеют в них функциональную сульфонильную группу). п-Крезидинсульфоновая кислота используется для изготовления пищевых красителей.
Сульфоновые кислоты, являясь сильными кислотами, также используются в качестве катализаторов. Простейшими примерами являются метансульфоновая кислота, CH 3 SO 2 OH и п- толуолсульфоновая кислота, которые регулярно используются в органической химии в качестве липофильных кислот (растворимых в органических растворителях). Также можно использовать полимерные сульфоновые кислоты. Смола Dowex представляет собой производные сульфоновой кислоты полистирола и используется в качестве катализаторов и для ионного обмена ( умягчение воды ). Нафион, фторированная полимерная сульфоновая кислота, является компонентом протонообменных мембран в топливных элементах.
Препараты сульфамида, класс антибактериальных средств, производятся из сульфокислот.
 Сульфонаты являются основой большинства ионообменных смол, используемых для умягчения воды.
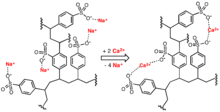
Сульфонаты являются основой большинства ионообменных смол, используемых для умягчения воды. В сульфитном процессе изготовления бумаги лигнин удаляется из лигноцеллюлозы путем обработки древесной стружки растворами сульфитных и бисульфит-ионов. Эти реагенты расщепляют связи между компонентами целлюлозы и лигнина, особенно внутри самого лигнина. Лигнин превращается в лигносульфонаты, полезные иономеры, которые растворимы и могут быть отделены от целлюлозных волокон.
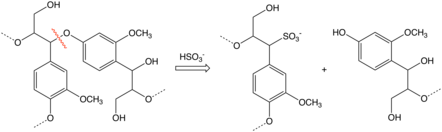 идеализированная схема деполимеризации лигнина сульфитным процессом.
идеализированная схема деполимеризации лигнина сульфитным процессом. Арилсульфоновые кислоты подвержены гидролизу, обратному реакции сульфирования. В то время как бензолсульфоновая кислота гидролизуется при температуре выше 200 ° C, большинство родственных производных гидролизуются легче. Таким образом, нагревание арилсульфоновых кислот в водной кислоте дает исходный арен. Эта реакция используется в нескольких сценариях. В некоторых случаях сульфоновая кислота служит в качестве водорастворимой защитной группы, что проиллюстрировано очисткой пара-ксилола через его производное сульфоновой кислоты. При синтезе 2,6-дихлорфенола фенол превращается в его производное 4-сульфоновой кислоты, которое затем селективно хлорируется в положениях, фланкирующих фенол. Гидролиз высвобождает группу сульфоновой кислоты.
Сульфоновые кислоты можно превратить в сложные эфиры. Этот класс органических соединений имеет общую формулу R-SO 2 -OR. Сложные эфиры сульфоновой кислоты, такие как метилтрифлат, считаются хорошими алкилирующими агентами в органическом синтезе. Такие сложные эфиры сульфоновой кислоты часто получают алкоголизом сульфонилхлоридов:
Сульфонилгалогенидные группы возникают, когда сульфонильная функциональная группа однократно связана с атомом галогена. У них есть общая формула R − SO 2 −X, где X - галогенид, почти всегда хлорид. Их получают хлорированием сульфоновых кислот с использованием тионилхлорида и родственных реагентов.
Хотя связь (арил) C-SO 3 - прочная, она может быть разорвана нуклеофильными реагентами. Историческое и непреходящее значение имеет α-сульфирование антрохинона с последующим замещением сульфонатной группы другими нуклеофилами, что не может быть установлено напрямую. Один из первых способов получения фенола включал основной гидролиз бензолсульфоната натрия, который можно легко получить из бензола.
Однако условия для этой реакции суровые, требующие наличия «плавленой щелочи» или расплавленного гидроксида натрия при 350 ° C для самой бензолсульфоновой кислоты. В отличие от механизма конденсированного щелочного гидролиза хлорбензола, который протекает через элиминирование-присоединение ( бензиновый механизм), бензолсульфоновая кислота претерпевает аналогичное превращение по механизму S N Ar, как показывает мечение 14 C, несмотря на отсутствие стабилизирующих заместителей. Сульфоновые кислоты с электроноакцепторными группами (например, с заместителями NO 2 или CN) гораздо легче подвергаются этому превращению.