 | |
| Имена | |
|---|---|
| Название IUPAC Натрий этоксид | |
| Другие названия Этанолат натрия, этилат натрия (устаревший) | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| Ссылка Beilstein | 3593646 |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.004.989 |
| Номер EC |
|
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
| 241>[Na +]. [O-] CC | |
| Свойства | |
| Химическая формула | C2H5ONa |
| Молярная масса | 68,05 г / моль |
| Внешний вид | белый. гигроскопичность |
| Плотность | 0,868 г / см ^ 3 (21 мас.% Раствора в этаноле) |
| Температура плавления | 260 ° C (500 ° F; 533 K) |
| Растворимость в воде | Реагирует |
| Растворимость | этанол и метанол |
| Кислотность (pK a) | 15,5 |
| Опасности | |
| Безопасность технический паспорт | Oxford MSDS |
| пиктограммы GHS |    |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H228, H251, H302, H314, H318 |
| Меры предосторожности GHS | P210, P235 + 410, P240, P241, P260, P264, P270, P280, P301 + 312, P301 + 330 + 331, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P321, P330, P363, P370 + 378, P405, P407, P413, P420, P501 |
| NFPA 704 (огненный алмаз) |  2 2 1 2 2 1 |
| Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Этоксид натрия - органическое соединение остроумие h формула C 2H5ONa. Это белое твердое вещество, хотя нечистые образцы выглядят желтыми или коричневыми. Он растворяется в полярных растворителях, таких как этанол. Обычно используется в качестве сильного основания.
Сообщалось о нескольких процедурах с безводным твердым веществом. Вместо этого материал обычно готовят в растворе с этанолом. Он коммерчески доступен и в виде раствора в этаноле. Его легко получить в лаборатории путем обработки металла натрия абсолютным этанолом :
Альтернативой, Более дешевый способ предполагает реакцию гидроксида натрия с безводным этанолом. Эта реакция страдает неполным превращением в алкоксид, но для менее строгих применений полное превращение неважно.
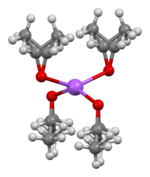
Кристаллическая структура этоксида натрия была определена с помощью рентгеновской кристаллографии. Он состоит из слоев чередующихся центров Na и O с неупорядоченными этильными группами, покрывающими верх и низ каждого слоя. Этиловые слои упаковываются спина к спине, образуя пластинчатую структуру. Реакция натрия и этанола иногда приводит к образованию других продуктов, таких как дисольват NaOEt · 2EtOH. Его кристаллическая структура была определена, хотя структура других фаз в системе Na / EtOH остается неизвестной.
 |  |  |
Этоксид натрия обычно используется в качестве основания в конденсации Клайзена и синтезе эфира малоновой кислоты. Этоксид натрия может депротонировать α-положение молекулы сложного эфира, образуя енолят, или молекула сложного эфира может подвергаться нуклеофильному замещению, называемому переэтерификацией. Если исходным материалом является этиловый эфир, переэтерификация не имеет значения, поскольку продукт идентичен исходному материалу. На практике сольватирующая смесь спирт / алкоксид должна соответствовать алкокси-компонентам реагирующих сложных эфиров, чтобы минимизировать количество различных продуктов.
Многие алкоксиды получают метатезисом солей из этоксида натрия.
Твердые образцы этилата натрия постепенно темнеют при хранении на сухом воздухе из-за окисления. Во влажном воздухе он быстро гидролизуется до гидроксида натрия. Конверсия не очевидна, и типичные образцы NaOEt загрязнены NaOH. Помимо четко видимого разложения, твердый этоксид натрия также имеет значительную нестабильность на воздухе без явных изменений внешнего вида, например распадается на множество других солей натрия при контакте с воздухом. Эту нестабильность можно предотвратить хранением этоксида натрия в инертной (N 2) атмосфере. Сообщалось, что недавно полученные коммерческие партии этоксида натрия демонстрируют различные уровни разложения и являются основным источником невоспроизводимости при использовании в реакциях Сузуки.
Этоксид натрия является сильным основанием, и поэтому вызывает коррозию.