 | |
| Имена | |
|---|---|
| Другие имена Фтористый натрий, SBF Фторид натрия | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.014.190 |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
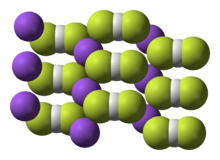
| Химическая формула | NaHF 2 |
| Внешний вид | белое твердое вещество |
| Плотность | 2,08 г / см |
| Температура плавления | 160 ° C (320 ° F; 433 K) (разлагается) |
| Если не указано иное, данные приводятся для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Бифторид натрия представляет собой неорганическое соединение w с формулой NaHF 2. Это соль катиона натрия (Na) и аниона бифторида (HF 2). Это белое водорастворимое твердое вещество, которое разлагается при нагревании. Бифторид натрия негорюч, гигроскопичен и имеет резкий запах. Бифторид натрия находит множество применений в промышленности.
Бифторид натрия диссоциирует до плавиковой кислоты и фторида натрия :
Обратное этой реакции используют для удаления HF из элементарного фтора (F 2), полученного электролизом. Это равновесие проявляется, когда соль растворяется и когда твердое вещество нагревается. Характерно для других бифторидов, он реагирует с кислотами с образованием HF. Иллюстративным является его взаимодействие с бисульфатом с образованием сульфата натрия и фтороводорода.
Сильные основания бифторид депротоната. Например, гидроксид кальция дает фторид кальция.
Бифторид натрия получают путем нейтрализации отходов фтористого водорода, который является результатом производства суперфосфатных удобрений. Типичные основания - это карбонат натрия и гидроксид натрия. Процесс происходит в два этапа, как показано на примере гидроксида:
Бифторид натрия реагирует с водой или влажной кожей с образованием плавиковой кислоты. Он также выделяет фтористоводородную кислоту и газообразный водород при нагревании до газообразного состояния. Химическое вещество может разлагаться при контакте с сильными кислотами, сильными основаниями, металлом, водой или стеклом. Бифторид натрия также вступает в бурные реакции с хромилхлоридом, азотной кислотой, красным фосфором, пероксидом натрия, диэтилсульфоксидом и диэтилцинк.
Основная роль бифторида натрия заключается в качестве предшественника фторида натрия, миллионы тонн которого производятся ежегодно.
Соединение также находит применение в чистке, используя сродство фторида к оксидам железа и кремния. Например, составы бифторида натрия используются для очистки кирпича, камня, керамики и кладки. Он также используется для рисования стекла. Еще одно применение бифторида натрия - химическая промышленность. Другие применения соединения включают гальванизацию ванн и борьбу с вредителями. Биологические применения бифторида натрия включают сохранение зоологических и анатомических образцов.
Другие применения бифторида натрия включают нейтрализаторы ополаскивателя для стирки.
Бифторид натрия играет роль в процессе, который используется для пластин металлических банок.
Бифторид натрия также способствует осаждению ионы кальция в процессе никеля гальваники. Соединение также способствует повышению коррозионной стойкости некоторых магниевых сплавов.
Бифторид натрия вызывает коррозию и раздражает при контакте с кожей и может вызвать образование пузырей и воспаление. Проглатывание чрезвычайно опасно. Попадание соединения в глаза может привести к слепоте и повреждению роговицы. Проглатывание пыли бифторида натрия может вызвать жжение, кашель и чихание в результате раздражения желудочно-кишечного тракта и дыхательных путей. Попадание соединения в глаза может вызвать покраснение, зуд и слезотечение. В тяжелых случаях воздействие бифторида натрия может привести к смерти. Эффекты отравления бифторидом натрия становятся заметными через 0–24 часа.
Повторное или длительное воздействие бифторида натрия может привести к флюорозу. Бифторид натрия не является канцерогенным.
Бифторид натрия не биоаккумулируется. Обычно он остается в среде только в течение нескольких дней.