| Интернексин белок промежуточного филамента, альфа | |
|---|---|
| Идентификаторы | |
| Символ | INA |
| Альт. символы | NEF5 |
| ген NCBI | 9118 |
| HGNC | 6057 |
| OMIM | 605338 |
| RefSeq | NM_032727 |
| UniProt | Q16352 |
| Прочие данные | |
| Locus | Chr. 10 q24 |
Интернексин, альфа-интернексин, представляет собой промежуточную нить класса IV приблизительно 66 кДа. Первоначально белок был очищен из зрительного нерва и спинного мозга крысы. Белок соединяется с другими субъединицами нейрофиламента, как это было первоначально обнаружено, однако в некоторых зрелых нейронах он может быть единственным экспрессируемым нейрофиламентом. Белок присутствует в развивающихся нейробластах и в центральной нервной системе взрослых. Белок является основным компонентом сети промежуточных филаментов в небольших интернейронах и гранулярных клетках мозжечка, где он присутствует в параллельных волокнах.
Альфа -интернексин имеет центральную гомологичную из примерно 310 аминокислотных остатков, которые образуют высококонсервативную альфа-спиральную область. Центральный стержневой домен отвечает за структуру coiled-coil и фланкирован аминоконцевой головной областью и карбоксиконцевой хвостовой частью. Этот стержневой домен также участвует в структуре сборки 10 нм филаментов. Области головы и хвоста содержат сегменты, которые очень гомологичны структуре NF-M. Головная область является высокоосновной и содержит много полимеров серина и треонина, тогда как хвостовая область имеет различные мотивы последовательности, такие как область, богатая глутаматом. Альфа-домен состоит из гептадных повторов из гидрофобных остатков, которые способствуют образованию структуры спиральной спирали. Структура альфа-интернексина является высококонсервативной у крыс, мышей и людей.
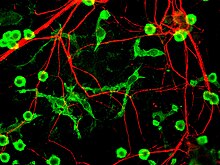 Смешанные культуры нейронов / глии из головного мозга крыс p18, окрашенные антителом к альфа-интернексину, которые выявляют в красном цвете нейронные отростки и тела клеток. Клетки также были помечены зеленым цветом для коронина 1a, маркера микроглии.
Смешанные культуры нейронов / глии из головного мозга крыс p18, окрашенные антителом к альфа-интернексину, которые выявляют в красном цвете нейронные отростки и тела клеток. Клетки также были помечены зеленым цветом для коронина 1a, маркера микроглии. Альфа-интернексин может образовывать гомополимеры, в отличие от гетерополимера формы нейрофиламентов. Это образование предполагает, что α-интернексин и три нейрофиламента образуют отдельные системы филаментов. Альфа-интернексин может не только образовывать гомополимеры, но и образовывать сеть протяженных филаментов в отсутствие других промежуточных белков филаментов и эффективно совместно собираться с любой субъединицей типа IV или типа III in vitro. В Ching et al. Предлагается модель сборки промежуточных волокон. Эта модель включает в себя следующие этапы:
Тесная связь между белками триплета нейрофиламентов и α-интернексином совершенно очевидна. α-интернексин функционально взаимозависим с белками триплета нейрофиламентов. Если генетически удалить NF-M и / или NF-H у мышей, транспорт и присутствие α-интернексина в аксонах центральной нервной системы резко снизятся. Они не только функционально схожи, но и скорости оборота этих четырех белков схожи.
Он экспрессируется на ранних стадиях развития в нейробласте вместе с α-интернексином и периферин. По мере продолжения развития в нейроны нейрофиламент триплетные белки (NF-L: нейрофиламент с низкой молекулярной массой , NF-M: со средней молекулярной массой нейрофиламента и NF-H: с высокой молекулярной массой нейрофиламента) выражаются в увеличении порядка молекулярной массы по мере уменьшения экспрессии α-интернексина. В фазе развития нейробласта α-интернексин обнаруживается в нейробластах нервной трубки и нервного гребня.
Во взрослых клетках α-интернексин в большом количестве экспрессируется в центральной нервной системе, в цитоплазме нейронов вместе с нейрофиламентом. триплетные белки. Они выражены в относительно фиксированном стехиометрическом отношении к нейрофиламентам.
Альфа-интернексин - это филамент мозга и центральной нервной системы, который участвует в развитии нейронов и был предложено играть роль в аксональном разрастании. Гефилтин и ксефилтин, гомологи α-интернексина у рыбок данио и Xenopus laevis, соответственно, высоко экспрессируются во время роста сетчатки и оптического аксона. регенерации и, следовательно, помогли предположить, что альфа-интернексин и отросток аксонов могут быть связаны. На основании этого предположения были проведены исследования по созданию более прочного моста между ними. Согласно исследованиям с нокаутом на мышах, ингибирование альфа-интернексина не оказало видимого эффекта на развитие нервной системы, что предполагает, что альфа-интернексин не влияет на рост аксонов, однако исследование с нокаутом не исключило малозаметного различия, которые мог вызвать белок. Мало того, что α-интернексин связан с разрастанием аксонов, он может регулировать стабильность или диаметр аксонов посредством изменений в филаментах и их составе субъединицы. Кроме того, интернексин может участвовать в поддержании или формировании дендритных шипов. Было много предположений относительно функции α-интернексина, но в настоящее время не существует конкретных доказательств, полностью подтверждающих или опровергающих эти предположения.
α-интернексин также участвует в некоторых дегенеративных заболеваниях, таких как болезнь Альцгеймера, боковой амиотрофический склероз, деменция. с тельцами Леви, болезнь Паркинсона, невропатии, тропический спастический парапарез и миелопатия, связанная с HTLV-1. При миелопатии HTLV-1 трансактиватор Tax, экспрессируемый HTLV-1, взаимодействует с α-интернексином в культуре клеток, что приводит к резкому снижению транскактивации Tax и образованию промежуточных филаментов.