 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC (2 E, 4 E, 6 E, 8 E) -3,7-Диметил-9- (2,6,6-триметилциклогекс-1-ен-1-ил) нона-2,4,6,8-тетраеналь | |
Другие имена
| |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100,003,760 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | С 20 Н 28 О |
| Молярная масса | 284,443 г моль -1 |
| Появление | Оранжевые кристаллы из петролейного эфира |
| Температура плавления | От 61 до 64 ° C (от 142 до 147 ° F, от 334 до 337 K) |
| Растворимость в воде | Почти нерастворим |
| Растворимость в жире | Растворимый |
| Родственные соединения | |
| Родственные соединения | ретинол ; ретиноевая кислота ; бета-каротин ; дегидроретинальный ; 3-гидроксиретинал; 4-гидроксиретинал |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
Ретиналь (также известный как ретинальдегид) представляет собой полиеновый хромофор. Сетчатка, связанная с белками, называемыми опсинами, представляет собой химическую основу зрительной фототрансдукции, стадии визуального восприятия (зрения) при обнаружении света.
Некоторые микроорганизмы используют сетчатку глаза для преобразования света в метаболическую энергию.
Есть много форм витамина А - все они превращаются в сетчатку, что невозможно без них. Сам по себе сетчатка считается формой витамина А при употреблении в пищу животными. Количество различных молекул, которые могут быть преобразованы в сетчатку, варьируется от вида к виду. Сетчатка первоначально назывались Ретиненом и переименована после того, как было обнаружено, что витамин А альдегид.
Позвоночные животные глотают сетчатку непосредственно из мяса или производят сетчатку из каротиноидов - либо из α-каротина, либо из β-каротина, оба из которых являются каротинами. Они также производят его из β-криптоксантина, типа ксантофилла. Эти каротиноиды должны быть получены из растений или других фотосинтезирующих организмов. Никакие другие каротиноиды не могут быть преобразованы животными в сетчатку. Некоторые плотоядные животные вообще не могут преобразовывать каротиноиды. Другие основные формы витамина А - ретинол и частично активная форма, ретиноевая кислота - могут вырабатываться из сетчатки.
Беспозвоночные, такие как насекомые и кальмары, используют гидроксилированные формы сетчатки в своих зрительных системах, которые возникают в результате преобразования других ксантофиллов.
Живые организмы производят сетчатку (RAL) путем необратимого окислительного расщепления каротиноидов.
Например:
катализируется бета-каротин 15,15'-монооксигеназой или бета-каротин 15,15'-диоксигеназой.
Подобно тому, как каротиноиды являются предшественниками сетчатки, сетчатка является предшественником других форм витамина А. Ретиналь взаимопревращается с ретинолом (ROL), транспортной формой и формой хранения витамина А:
катализируется ретинола дегидрогеназы (RDHs) и алкоголь дегидрогеназы (ADHS).
Ретинол называют витамином А, спиртом или, чаще, просто витамином А. Ретиналь также может окисляться до ретиноевой кислоты (РА):
катализируется дегидрогеназами сетчатки, также известными как дегидрогеназы ретинальдегида (RALDH), а также оксидазами сетчатки.
Ретиноевая кислота, которую иногда называют кислотой витамина А, является важной сигнальной молекулой и гормоном у позвоночных животных.
Сетчатка - конъюгированный хромофор. В человеческом глазе, сетчатка начинается в 11- цис -retinal конфигурации, которая - при захвате фотона правильной длины волны - выпрямляется в общероссийский трансе -retinal конфигурации. Это изменение конфигурации воздействует на белок опсин в сетчатке, который запускает каскад химических сигналов, который может привести к восприятию света или изображений человеческим мозгом. Спектр поглощения хромофора зависит от его взаимодействия с белком опсина, с которым он связан, так что разные комплексы ретиналь-опсин будут поглощать фотоны с разными длинами волн (т. Е. С разными цветами света).
 Белок опсин окружает молекулу сетчатки, ожидая обнаружения фотона. Как только сетчатка захватывает фотон, изменение конфигурации сетчатки отталкивается от окружающего белка опсина. Опсин может посылать химический сигнал в мозг человека, сигнализируя об обнаружении света. Затем ретиналь повторно загружается в свою 11- цис- конфигурацию за счет фосфорилирования АТФ, и цикл начинается снова.
Белок опсин окружает молекулу сетчатки, ожидая обнаружения фотона. Как только сетчатка захватывает фотон, изменение конфигурации сетчатки отталкивается от окружающего белка опсина. Опсин может посылать химический сигнал в мозг человека, сигнализируя об обнаружении света. Затем ретиналь повторно загружается в свою 11- цис- конфигурацию за счет фосфорилирования АТФ, и цикл начинается снова. 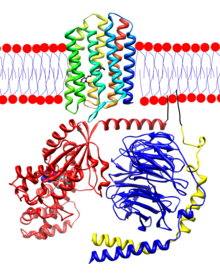 GPCR- родопсин животного (цвет радуги) встроен в липидный бислой (красные головы и синие хвосты) с трансдуцином под ним. G t α окрашен в красный цвет, G t β - в синий, а G t γ - в желтый. Существует связанное ВВП молекула в G т -субъединицы и связанные сетчатки (черная) в родопсине. N-конец - конец родопсина красного цвета, а С-конец синего цвета. Закрепление трансдуцина на мембране показано черным цветом.
GPCR- родопсин животного (цвет радуги) встроен в липидный бислой (красные головы и синие хвосты) с трансдуцином под ним. G t α окрашен в красный цвет, G t β - в синий, а G t γ - в желтый. Существует связанное ВВП молекула в G т -субъединицы и связанные сетчатки (черная) в родопсине. N-конец - конец родопсина красного цвета, а С-конец синего цвета. Закрепление трансдуцина на мембране показано черным цветом. Опсинов представляют собой белки и ретинальные связывания зрительных пигментов найдены в фоторецепторных клеток в сетчатке глаз. Опсин состоит из семи трансмембранных альфа-спиралей, соединенных шестью петлями. В стержневых клетках молекулы опсина встроены в мембраны дисков, которые полностью находятся внутри клетки. N-концевая головка молекулы проходит во внутреннюю части диска, и С-конце хвост простирается в цитоплазму клетки. В колбочковых клетках диски определяются плазматической мембраной клетки, так что головка N-конца выходит за пределы клетки. Сетчатка ковалентно связывается с лизином на трансмембранной спирали, ближайшей к С-концу белка, посредством связи основания Шиффа. Образование связи основания Шиффа включает удаление атома кислорода из сетчатки и двух атомов водорода из свободной аминогруппы лизина, что дает H 2 O. Ретинилиден - это двухвалентная группа, образованная удалением атома кислорода из сетчатки, поэтому опсины были названы ретинилиденовые белки.
Опсины представляют собой прототипы рецепторов, связанных с G-белком (GPCR). Бычий родопсин, опсин палочек крупного рогатого скота, был первым GPCR, для которого была определена его рентгеновская структура. Бычий родопсин содержит 348 аминокислотных остатков. Хромофор сетчатки связывается по Lys 296.
Хотя млекопитающие используют сетчатку исключительно в качестве хромофора опсина, другие группы животных дополнительно используют четыре хромофора, тесно связанные с сетчаткой: 3,4-дидегидроретиналь (витамин A 2), (3 R) -3-гидроксиретиналь, (3 S) -3-. гидроксиретинал (как витамин A 3), так и (4 R) -4-гидроксиретинал (витамин A 4). Многие рыбы и земноводные используют 3,4-дидегидроретиналь, также называемый дегидроретиналом. За исключением двукрылых подотряда Cyclorrhapha (так называемые высшие мухи), все исследованные насекомые используют ( R) - энантиомер 3-гидроксиретиналя. ( R) -энантиомер следует ожидать, если 3-гидроксиретиналь продуцируется непосредственно из каротиноидов ксантофилла. Циклоррафаны, включая Drosophila, используют (3 S) -3-гидроксиретинал. Было обнаружено, что кальмары-светлячки используют (4 R) -4-гидроксиретинал.
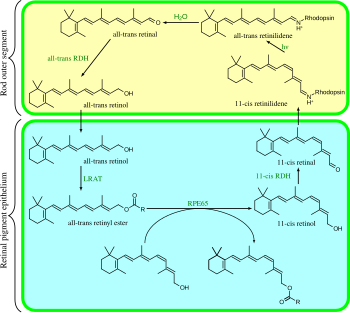 Визуальный цикл
Визуальный цикл Зрительный цикл - это круговой ферментативный путь, который является передним концом фототрансдукции. Восстанавливает 11- цис- ретиналь. Например, зрительный цикл стержневых клеток млекопитающих выглядит следующим образом:
Шаги 3, 4, 5 и 6 происходят во внешних сегментах стержневой ячейки ; Шаги 1, 2 и 7 происходят в клетках пигментного эпителия сетчатки (RPE).
Изомерогидролазы RPE65 гомологичны бета-каротинмонооксигеназам; гомологичный фермент ninaB у Drosophila обладает как каротиноид-оксигеназной активностью, формирующей сетчатку, так и активностью полностью транс- к 11- цис- изомеразе.
All- trans -retinal также является важным компонентом микробных опсинов, таких как бактериородопсин, каналродопсин и галородопсин. В этих молекулах свет заставляет полностью транс- ретиналь превращаться в 13- цис- ретиналь, который затем возвращается обратно в полностью транс- ретиналь в темном состоянии. Эти белки не связаны эволюционно с опсинами животных и не являются GPCR; тот факт, что они оба используют сетчатку, является результатом конвергентной эволюции.
Американский биохимик Джордж Уолд и другие наметили визуальный цикл к 1958 году. За свою работу Уолд вместе с Халданом Кеффером Хартлайном и Рагнаром Гранитом получил долю Нобелевской премии по физиологии и медицине 1967 года.